Clear Sky Science · sv
Lipidasymmetri störd av XKR8 orkestrerar neutrofilers extracellulära nätbildning och hämmar svampinfektion
Hur våra förstalinjeförsvarare utlöser en dold fälla
När bakterier eller andra mikroorganismer invaderar är neutrofiler—en typ av vita blodkroppar—en av kroppens snabbaste förstärkningar, och de kan kasta ut klibbiga nät av DNA för att fånga in smittämnen. Dessa strukturer, kallade neutrofilers extracellulära nät eller NETs, är kraftfulla allierade i kampen mot infektion men kan också skada kroppens egna vävnader om de frigörs vid fel tillfälle. Denna studie avslöjar en överraskande ”huvudströmbrytare” i neutrofilens yttre membran som hjälper avgöra när dessa DNA-nät kastas ut, och visar hur den brytaren skyddar lungorna mot farliga svampangripare.
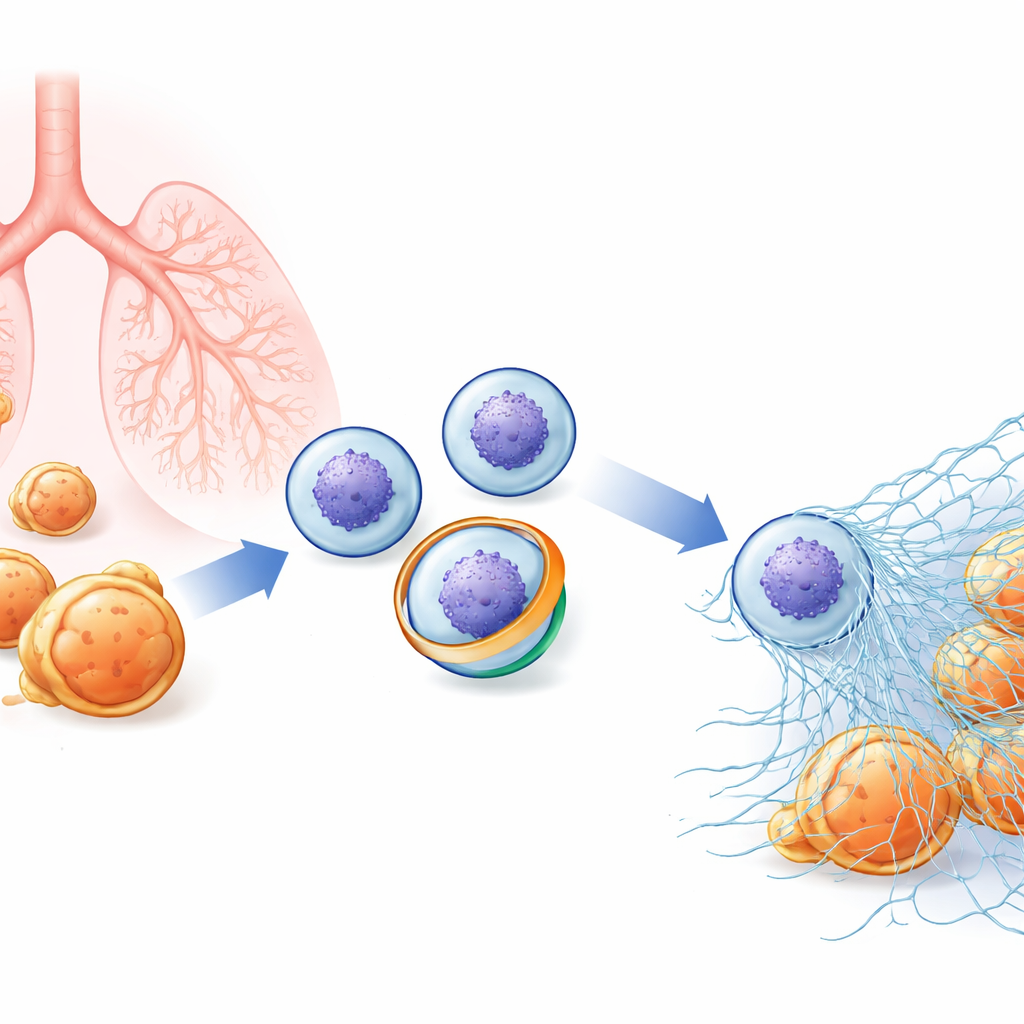
Ett dolt nät inne i immuncellerna
Neutrofiler patrullerar blodet redo att slå mot bakterier och svampar. Förutom att fagocytera mikrober kan de explodera utåt och släppa lös dekondenserat kromatin (materialet som bygger upp kromosomerna) täckt av antimikrobiella enzymer. Dessa klibbiga fibrer bildar NETs som trasslar in patogener så att de kan dödas lokalt. Eftersom NETs är så potenta måste deras frisättning vara noggrant reglerad: för lite och infektioner kan spåra ur; för mycket och samma nät kan driva autoimmun sjukdom, lungskaador och blodproppar. Forskare misstänkte att subtila förändringar i neutrofilens yttre membran kan vara ett tidigt steg i beslutet om en cell ska genomgå denna dramatiska ”NETos”, men de centrala molekylära aktörerna var tidigare okända.
En membranbrytare kallad XKR8
Forskarna koncentrerade sig på ett protein som heter XKR8, som finns i särskilt höga nivåer i neutrofiler. XKR8 är en så kallad ”scramblase” – ett protein som kan vända lipider mellan membranets inre och yttre lager och därigenom sudda ut den normala asymmetrin mellan sidorna. I andra sammanhang, såsom programmerad celldöd, är XKR8 känt för att exponera en lipidsignal på cellytan som markerar döende celler för borttransport. Här visade författarna att under NET-bildning uppträder exponeringen av denna lipidsignal innan membranet blir läckande och innan DNA släpps ut, vilket markerar de neutrofiler som är på väg att bilda NETs. När de avlägsnade XKR8 från mus- och humana neutrofiler kunde cellerna inte längre genomföra detta tidiga scramble-steg och misslyckades nästan helt med att bilda NETs som svar på många kemiska och mikrobiella stimuli.
Från membranomfördelning till kalciumsurge
Det är känt att NET-bildning beror på en stigning i kalcium inne i neutrofiler, vilket aktiverar enzymer som luckrar upp kromatin och tillåter DNA att strömma ut. Forskarna upptäckte att XKR8 sitter i hjärtat av denna process. Efter ett oxidativt utbrott inne i neutrofilerna klyver och aktiverar en exekutörsenzym kallat caspas-3 XKR8. När XKR8 väl är omskakad redistribuerar det snabbt flera lipidtyper över membranet, inte bara en enskild ”ät mig”-signal. Med hjälp av fluorescerande sensorer visade teamet att denna omfördelning förändrar membranets fysiska spänning. I sin tur öppnar denna mekaniska belastning en uppsättning mekanosensoriska kalciumkanaler inbäddade i membranet, vilket tillåter kalciumjoner att strömma in i cellen precis under det fönster när NET-bildning pågår. Om forskarna blockerade dessa kanaler uteblev NETs i stor utsträckning; om de stimulerade kanalerna med särskilda aktivatorer kunde de återställa NET-bildning även i celler som saknade XKR8.
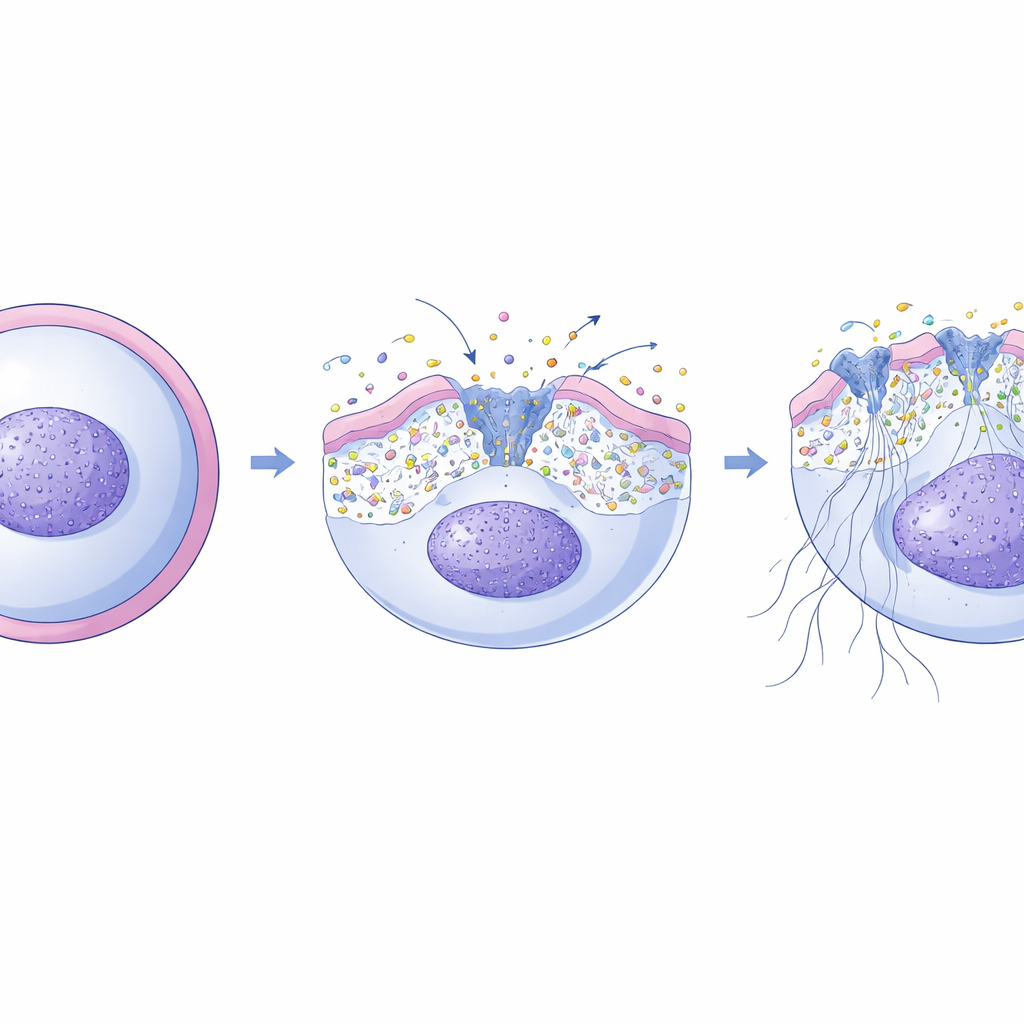
När fällor uteblir: lungskaada och svampinfektion
För att förstå vad denna membranbrytare innebär i levande djur studerade teamet möss som antingen saknade XKR8 helt eller bar en muterad version som inte kan klyvas av caspas-3. I modeller för akut lungskaada framkallad av bakteriella komponenter utvecklade normala möss rikliga NETs i lungorna, höga nivåer av fritt DNA i lungvätskan och tydliga vävnadsskador. Möss med nedsatt XKR8-aktivitet rekryterade samma antal neutrofiler men producerade långt färre NETs och drabbades av mindre lungskaada, vilket tyder på att XKR8-brytaren är en viktig drivkraft för skadlig NET-frisättning i detta sammanhang. I kontrast, när lungorna infekterades med svampen Candida albicans stod möss utan fungerande XKR8-brytare inför stora nackdelar: de bildade betydligt färre NETs, bar tyngre svampbörda i lungor och andra organ, blödde mer in i luftutrymmen och dog oftare av överväldigande infektion. Noterbart är att en substans som aktiverar en av de mekanosensoriska kalciumkanalerna delvis räddade svampkontrollen hos möss vars neutrofiler saknade XKR8.
En central spak med två sidor
Detta arbete avslöjar en enhetlig mekanism där många olika fara-signaler konvergerar på en enda membranbaserad beslutspunkt i neutrofiler. Oxidativa utbrott leder till caspas-3-aktivering, som slår på XKR8 för att scrambla membranlipider, förändra membranspänningen och öppna kalciumkanaler, vilket kulminerar i utsläppet av NETs. För den lekmanna läsaren är budskapet att vårt immunförsvar använder en fint avvägd ”lipidspak” på neutrofilernas yta för att bestämma när DNA-näten ska kastas ut. Att luta spaken åt ena hållet hjälper till att rensa stora svampangripare; att luta den för ofta eller vid fel tidpunkt kan förvärra steril inflammation som lungskaada eller artrit. Eftersom denna väg står i skärningspunkten mellan skydd och skada kan riktade åtgärder mot caspas-3–XKR8–kalcium-axeln ge nya strategier för att antingen tygla skadliga NETs eller förstärka fördelaktiga, beroende på kliniskt behov.
Citering: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Nyckelord: neutrofilers extracellulära nät, XKR8 scramblase, medfödd immunitet, svampinfektion i lunga, akut lungskaada