Clear Sky Science · fr
La perturbation de l’asymétrie lipidique par XKR8 orchestre la formation de filets extracellulaires de neutrophiles et inhibe l’infection fongique
Comment nos défenseurs de première ligne déclenchent un piège caché
Lorsque des agents pathogènes envahissent, l’un des réacteurs les plus rapides du corps est le neutrophile, un globule blanc capable de projeter des toiles collantes d’ADN pour capturer les microbes. Ces structures, appelées filets extracellulaires de neutrophiles, ou NETs, sont des alliés puissants contre l’infection mais peuvent aussi endommager nos propres tissus si elles sont libérées au mauvais moment. Cette étude révèle un surprenant « interrupteur maître » dans la membrane externe du neutrophile qui contribue à décider quand ces toiles d’ADN sont lancées, et montre comment cet interrupteur protège les poumons contre des envahisseurs fongiques dangereux.
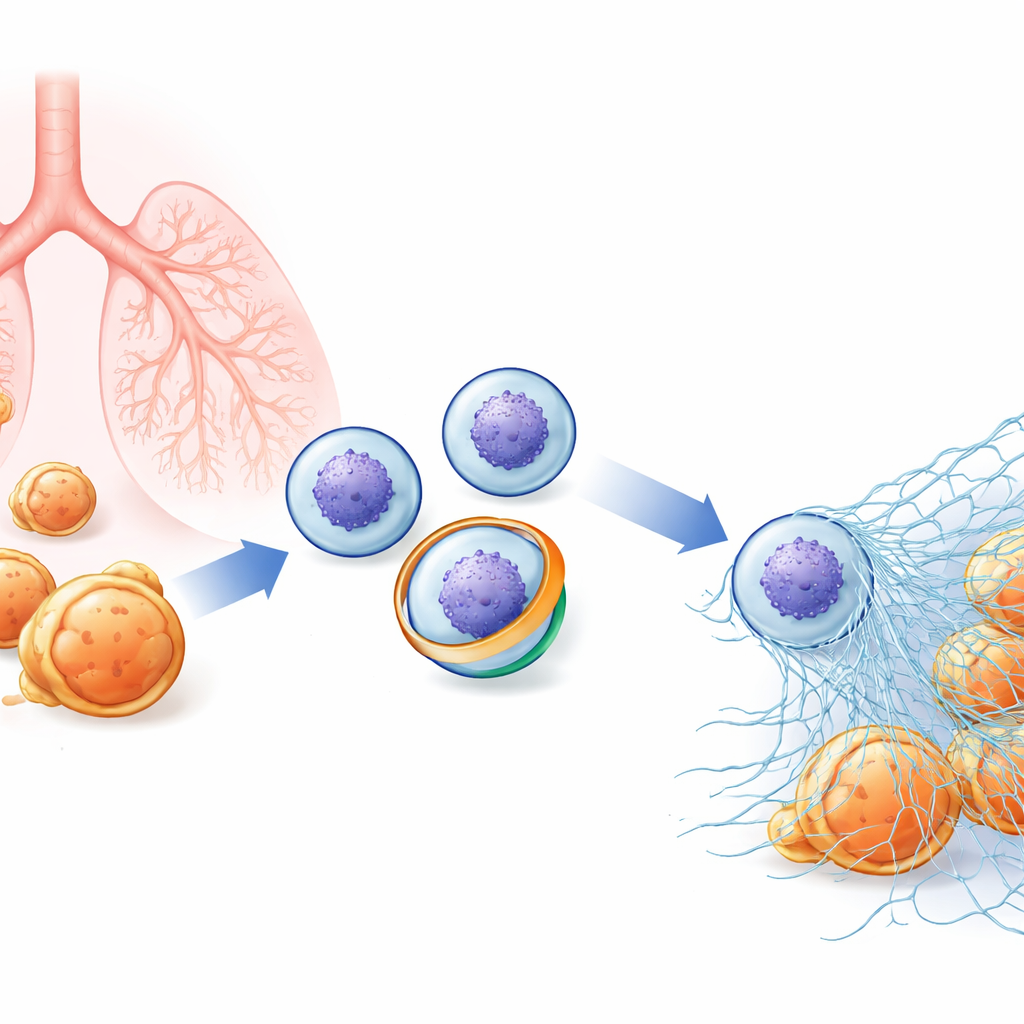
Une toile cachée à l’intérieur des cellules immunitaires
Les neutrophiles patrouillent dans le sang prêts à attaquer bactéries et champignons. Outre l’ingestion des microbes, ils peuvent exploser vers l’extérieur, libérant de la chromatine décondensée (la matière qui compose les chromosomes) enrobée d’enzymes antimicrobiennes. Ces fibres collantes forment des NETs qui emmêlent les agents pathogènes afin qu’ils puissent être tués localement. Parce que les NETs sont si puissants, leur libération doit être strictement contrôlée : trop peu et les infections peuvent s’aggraver ; trop, et ces mêmes toiles peuvent alimenter des maladies auto-immunes, des lésions pulmonaires et des caillots sanguins. Les chercheurs soupçonnaient que des changements subtils dans la membrane externe du neutrophile pourraient être une étape précoce dans la décision qu’une cellule subisse cette « NETose » dramatique, mais les acteurs moléculaires clés étaient inconnus.
Un interrupteur membranaire nommé XKR8
L’équipe s’est focalisée sur une protéine appelée XKR8, présente à des niveaux particulièrement élevés dans les neutrophiles. XKR8 est une « scramblase » – une protéine capable d’inverser la distribution des lipides entre les couches interne et externe de la membrane cellulaire, effaçant l’asymétrie habituelle entre les deux faces. Dans d’autres contextes, comme la mort cellulaire programmée, XKR8 expose un signal lipidique à la surface cellulaire qui marque les cellules mourantes pour leur élimination. Ici, les auteurs montrent que pendant la formation des NETs, l’exposition de ce signal lipidique survient avant que la membrane ne devienne perméable et avant la libération d’ADN, signalant les neutrophiles destinés à former des NETs. Lorsqu’ils ont supprimé XKR8 chez des neutrophiles de souris et d’humain, les cellules n’ont plus pu effectuer cette étape précoce de mélange lipidique et ont presque totalement perdu la capacité de former des NETs en réponse à de nombreux déclencheurs chimiques et microbiens.
Du remaniement membranaire à la montée calcique
La formation des NETs dépend d’une élévation du calcium intracellulaire dans les neutrophiles, qui active des enzymes desserrant la chromatine et permettant à l’ADN de s’échapper. Les chercheurs ont découvert que XKR8 se situe au cœur de ce processus. Après une explosion oxydative à l’intérieur du neutrophile, une enzyme d’exécution appelée caspase-3 clive et active XKR8. Une fois activé, XKR8 redistribue rapidement plusieurs types de lipides à travers la membrane, pas seulement un unique signal « mange-moi ». À l’aide de sondes fluorescentes, l’équipe a montré que ce remaniement modifie la tension physique de la membrane. À son tour, ce stress mécanique ouvre un ensemble de canaux calciques mécanosensibles incorporés dans la membrane, permettant aux ions calcium de pénétrer dans la cellule précisément pendant la fenêtre où la formation des NETs est en cours. Si les chercheurs bloquaient ces canaux, les NETs étaient largement abolies ; s’ils stimulaient les canaux avec des activateurs spécifiques, ils pouvaient restaurer la formation des NETs même dans des cellules dépourvues de XKR8.
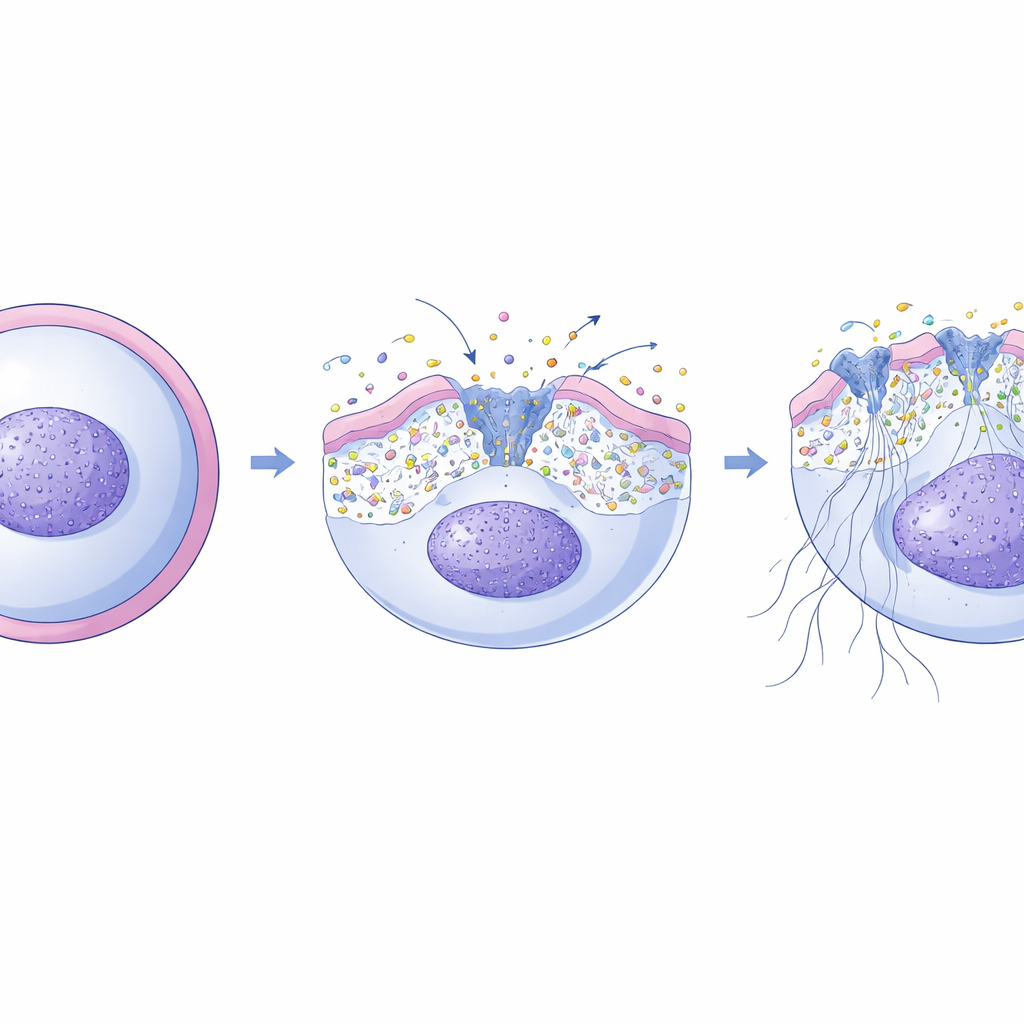
Quand les pièges échouent : lésion pulmonaire et infection fongique
Pour comprendre ce que cet interrupteur membranaire signifie chez l’animal vivant, l’équipe a étudié des souris génétiquement modifiées soit pour ne pas exprimer XKR8, soit pour porter une version mutée qui ne peut pas être clivée par la caspase-3. Dans des modèles de lésion pulmonaire aiguë déclenchée par des composants bactériens, les souris normales développaient des NETs abondants dans leurs poumons, de hauts niveaux d’ADN libre dans le liquide pulmonaire et des dommages tissulaires marqués. Les souris avec une activité XKR8 altérée recrutaient le même nombre de neutrophiles mais produisaient beaucoup moins de NETs et subissaient moins de lésions pulmonaires, ce qui suggère que l’interrupteur XKR8 est un moteur majeur de la libération nocive de NETs dans ce contexte. En revanche, lorsque les poumons étaient infectés par le champignon Candida albicans, les souris sans interrupteur XKR8 fonctionnel étaient sérieusement désavantagées : elles formaient beaucoup moins de NETs, présentaient des charges fongiques plus lourdes dans les poumons et d’autres organes, saignaient davantage dans les espaces aériens et mouraient plus souvent d’une infection incontrôlée. Notamment, un médicament activant l’un des canaux calciques mécanosensibles a partiellement rétabli le contrôle fongique chez des souris dont les neutrophiles étaient dépourvus de XKR8.
Un levier central à deux visages
Ce travail révèle un mécanisme unificateur par lequel de nombreux signaux de danger convergent vers un point de décision membranaire unique dans les neutrophiles. Les explosions oxydatives mènent à l’activation de la caspase-3, qui met en marche XKR8 pour brouiller les lipides membranaires, modifier la tension de la membrane et ouvrir les canaux calciques, aboutissant au lancement des NETs. Pour le lecteur non spécialiste, le message est que notre système immunitaire utilise un « levier lipidique » finement réglé à la surface des neutrophiles pour décider quand déployer des toiles d’ADN. Incliner ce levier dans un sens aide à éliminer de grands envahisseurs fongiques ; l’incliner trop souvent ou au mauvais moment peut aggraver des inflammations stériles telles que les lésions pulmonaires ou l’arthrite. Parce que cette voie se trouve à la croisée de la protection et du dommage, cibler l’axe caspase-3–XKR8–calcium pourrait offrir de nouvelles stratégies pour soit freiner des NETs nuisibles, soit stimuler des NETs bénéfiques, selon le besoin clinique.
Citation: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Mots-clés: filets extracellulaires de neutrophiles, scramblase XKR8, immunité innée, infection fongique pulmonaire, lésion pulmonaire aiguë