Clear Sky Science · es
La alteración de la asimetría lipídica por XKR8 orquesta la formación de trampas extracelulares de neutrófilos e inhibe la infección fúngica
Cómo nuestros defensores de primera línea activan una trampa oculta
Cuando los gérmenes invaden, uno de los respondedores más rápidos del cuerpo es el neutrófilo, un glóbulo blanco que puede lanzar redes pegajosas de ADN para atrapar microbios. Estas estructuras, llamadas trampas extracelulares de neutrófilos, o NETs, son aliados potentes en la lucha contra la infección, pero también pueden dañar nuestros propios tejidos si se liberan en el momento equivocado. Este estudio descubre un sorprendente “interruptor maestro” en la membrana externa del neutrófilo que ayuda a decidir cuándo se tejen estas redes de ADN, y muestra cómo ese interruptor protege los pulmones frente a invasores fúngicos peligrosos.
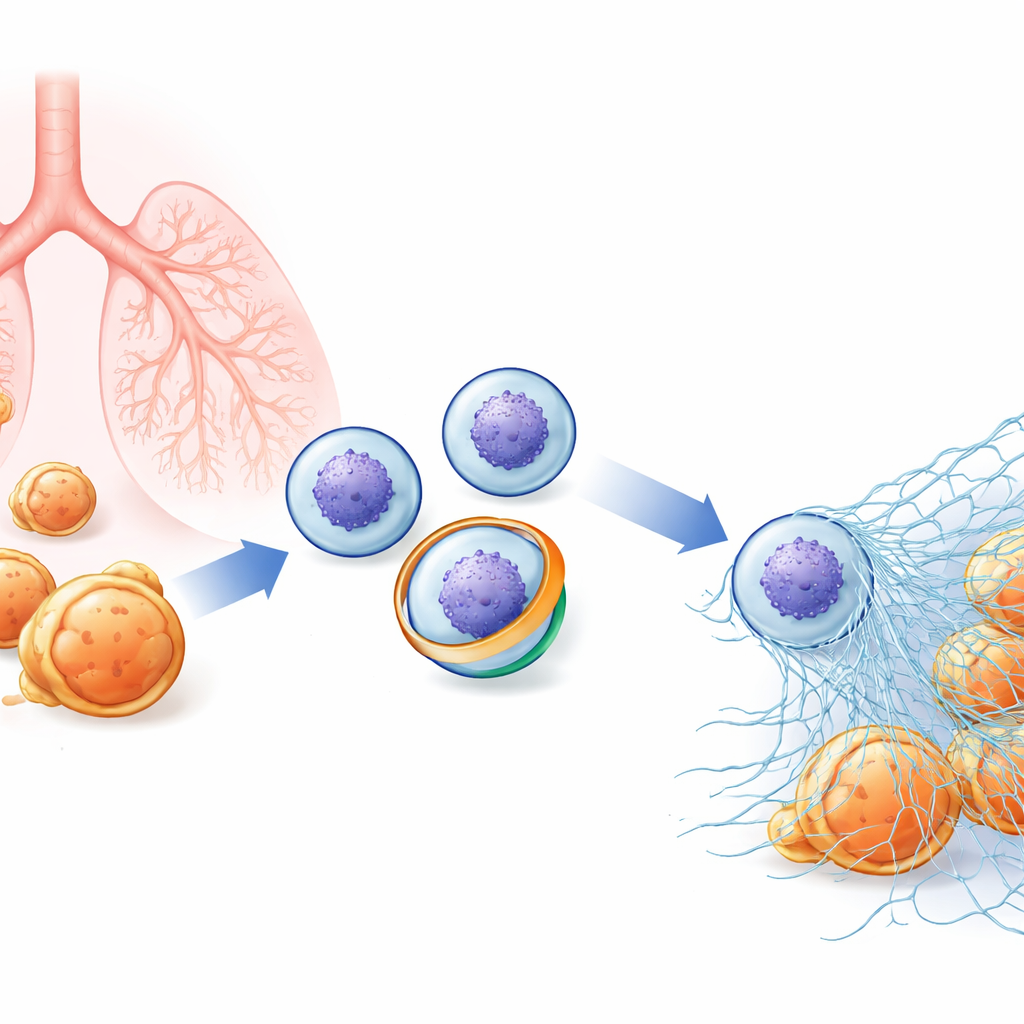
Una red oculta dentro de las células inmunitarias
Los neutrófilos patrullan la sangre listos para atacar bacterias y hongos. Además de fagocitar microbios, pueden estallar hacia el exterior, liberando cromatina descondensada (el material que forma los cromosomas) recubierta de enzimas antimicrobianas. Estas fibras pegajosas forman NETs que enredan a los patógenos para que puedan ser eliminados localmente. Dado que las NETs son tan potentes, su liberación debe estar estrictamente controlada: muy poca permite que las infecciones se descontrolen; demasiada puede alimentar enfermedades autoinmunes, lesión pulmonar y coágulos sanguíneos. Los investigadores sospechaban que cambios sutiles en la membrana externa del neutrófilo podrían ser un paso temprano para decidir si una célula sufrirá esta dramática “NETosis”, pero los jugadores moleculares clave eran desconocidos.
Un interruptor de membrana llamado XKR8
El equipo se centró en una proteína denominada XKR8, que se encuentra en niveles especialmente altos en los neutrófilos. XKR8 es una «scramblasa»: una proteína que puede voltear lípidos entre las capas interna y externa de la membrana celular, borrando la asimetría habitual entre ambos lados. En otros contextos, como la muerte celular programada, se sabe que XKR8 expone una señal lipídica en la superficie celular que marca a las células moribundas para su eliminación. Aquí, los autores mostraron que durante la formación de NETs, la exposición de esa señal lipídica aparece antes de que la membrana se vuelva permeable y antes de que se libere el ADN, señalando a aquellos neutrófilos destinados a formar NETs. Cuando eliminaron XKR8 de neutrófilos de ratón y humanos, las células ya no pudieron realizar este paso temprano de reordenamiento y casi dejaron de formar NETs en respuesta a muchos desencadenantes químicos y microbianos.
Del reordenamiento de la membrana a la avalancha de calcio
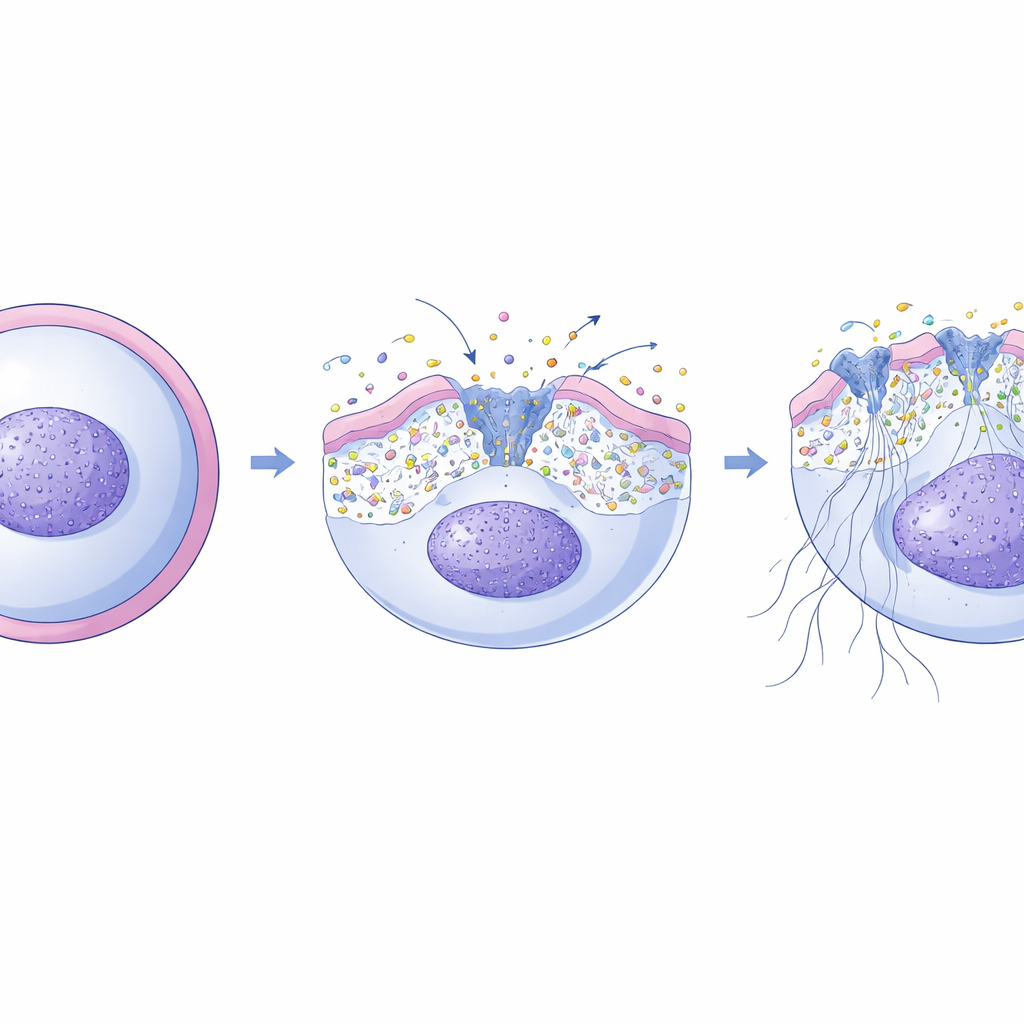
Se sabe que la formación de NETs depende de un aumento de calcio dentro de los neutrófilos, que activa enzimas que aflojan la cromatina y permiten que el ADN se derrame. Los investigadores descubrieron que XKR8 está en el centro de este proceso. Tras una ráfaga oxidativa dentro del neutrófilo, una enzima ejecutora llamada caspasa-3 corta y activa a XKR8. Una vez encendido, XKR8 redistribuye rápidamente varios tipos de lípidos a través de la membrana, no solo una única señal de «cómeme». Usando sondas fluorescentes, el equipo mostró que este reordenamiento cambia la tensión física de la membrana. A su vez, ese estrés mecánico abre un conjunto de canales de calcio mecanosensibles incrustados en la membrana, permitiendo que iones de calcio entren en la célula precisamente durante la ventana en que se está produciendo la formación de NETs. Si los investigadores bloqueaban estos canales, las NETs se veían mayormente abolidas; si estimulaban los canales con activadores específicos, podían restaurar la formación de NETs incluso en células carentes de XKR8.
Cuando las trampas fallan: lesión pulmonar e infección fúngica
Para entender qué significa este interruptor de membrana en animales vivos, el equipo estudió ratones modificados genéticamente para carecer totalmente de XKR8 o para portar una versión mutada que no puede ser cortada por la caspasa-3. En modelos de lesión pulmonar aguda desencadenada por componentes bacterianos, los ratones normales desarrollaron abundantes NETs en sus pulmones, altos niveles de ADN libre en el líquido pulmonar y un daño tisular marcado. Los ratones con actividad de XKR8 deteriorada reclutaron el mismo número de neutrófilos pero produjeron muchas menos NETs y sufrieron menos daño pulmonar, lo que sugiere que el interruptor XKR8 es un factor principal en la liberación nociva de NETs en ese contexto. En contraste, cuando los pulmones se infectaron con el hongo Candida albicans, los ratones sin un interruptor XKR8 funcional estaban en seria desventaja: formaron muchas menos NETs, acumularon mayores cargas fúngicas en pulmones y otros órganos, sangraron más en los espacios aéreos y murieron con más frecuencia por la infección abrumadora. Cabe destacar que un fármaco que activa uno de los canales de calcio mecanosensibles rescató en parte el control fúngico en ratones cuyos neutrófilos carecían de XKR8.
Una palanca central con dos caras
Este trabajo revela un mecanismo unificante por el cual muchas señales de peligro convergen en un único punto de decisión basado en la membrana de los neutrófilos. Las ráfagas oxidativas conducen a la activación de la caspasa-3, que enciende XKR8 para reordenar los lípidos de la membrana, cambiar la tensión de la membrana y abrir los canales de calcio, culminando en el lanzamiento de NETs. Para un lector no especializado, el mensaje es que nuestro sistema inmunitario usa una «palanca lipídica» finamente ajustada en la superficie de los neutrófilos para decidir cuándo lanzar redes de ADN. Inclinar esa palanca en una dirección ayuda a eliminar grandes invasores fúngicos; inclinarla con demasiada frecuencia o en el momento equivocado puede empeorar la inflamación estéril, como la lesión pulmonar o la artritis. Debido a que esta vía se sitúa en la encrucijada entre protección y daño, dirigir el eje caspasa-3–XKR8–calcio podría ofrecer nuevas estrategias para contener NETs dañinas o potenciar las beneficiosas, según la necesidad clínica.
Cita: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Palabras clave: trampas extracelulares de neutrófilos, scramblasa XKR8, inmunidad innata, infección fúngica pulmonar, lesión pulmonar aguda