Clear Sky Science · ja
XKR8による脂質非対称性の破綻が好中球外罠形成を統御し真菌感染を抑制する
一次防御隊が隠れた罠を仕掛ける仕組み
病原体が侵入すると、体の最速級の応答者の一つが好中球です。好中球は粘着性のあるDNAの網を放出して微生物を絡め取ることができます。これらは好中球外罠(neutrophil extracellular traps, NETs)と呼ばれ、感染と闘う強力な味方ですが、誤ったタイミングで放出されると自身の組織を損なうことがあります。本研究は、好中球の外膜に存在する驚くべき“マスタースイッチ”がいつDNAの網を展開するかを決める手助けをし、このスイッチが危険な真菌の侵入から肺を守る仕組みを明らかにします。
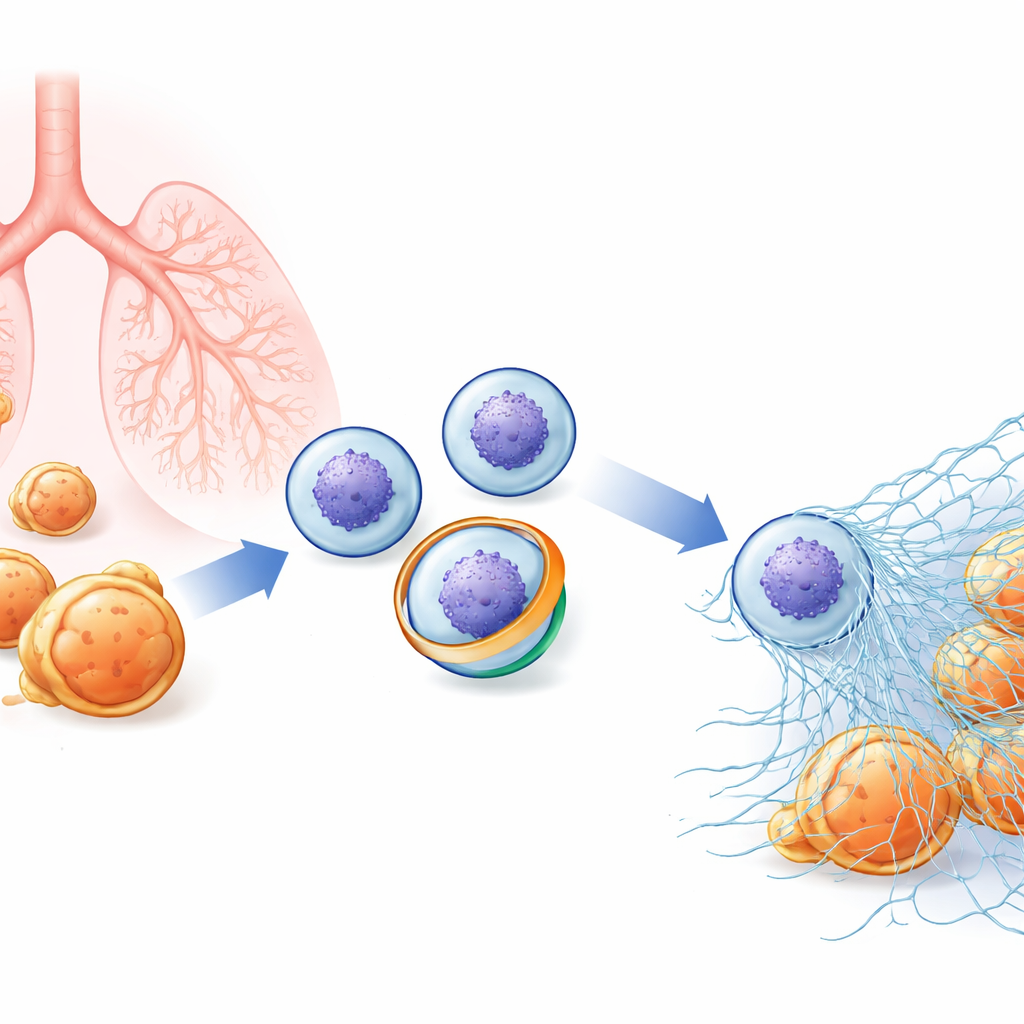
免疫細胞の内側にある隠れた網
好中球は血液中を巡回し、細菌や真菌を攻撃する準備をしています。微生物を貪食することに加え、好中球は外側に爆発的に展開して、抗菌酵素に被われた脱凝縮したクロマチン(染色体を構成する物質)を放出することがあります。これらの粘着性の繊維はNETを形成し、病原体を絡め取って局所で殺菌できるようにします。NETは非常に強力なため、その放出は厳密に制御される必要があります:少なすぎれば感染が制御できなくなり、多すぎれば同じ網が自己免疫疾患、肺障害、血栓を引き起こすことがあります。研究者たちは、好中球の外膜に生じる微妙な変化がこの劇的な“NETosis”が起こるかどうかを決める初期段階かもしれないと考えていましたが、重要な分子の正体は不明でした。
XKR8と呼ばれる膜スイッチ
研究チームは好中球で特に高発現しているXKR8というタンパク質に着目しました。XKR8はスクランブラーであり、細胞膜の内面と外面の間で脂質を入れ替え、通常の両面の非対称性を消すことができます。他の文脈、例えばプログラムされた細胞死では、XKR8は死滅する細胞を除去するための表面上の脂質シグナルを露出させることが知られています。本研究では、NET形成中にこの脂質シグナルの露出が膜の透過性が高まる前、DNAが放出される前に起こり、NETを形成する運命にある好中球を示すことを示しました。マウスとヒトの好中球からXKR8を除去すると、細胞はこの初期のスクランブルを実行できず、多くの化学的および微生物性の刺激に対してほとんどNETを作れなくなりました。
膜の再配列からカルシウムの急増へ
NET形成は好中球内のカルシウム上昇に依存しており、これがクロマチンを緩めてDNAを放出させる酵素を活性化します。研究者たちはXKR8がこの過程の中心に位置することを発見しました。好中球内での酸化バーストの後、実行役の酵素であるカスパーゼ-3がXKR8を切断して活性化します。スイッチが入ると、XKR8は単一の“食べて”シグナルだけでなく複数種類の脂質を迅速に膜の両面で再配列します。蛍光プローブを用いた実験から、この再配列が膜の物理的張力を変化させることが示されました。その結果として、この機械感受性のカルシウムチャネル群が膜で開き、カルシウムイオンがNET形成が進行しているその正確な窓の間に細胞内へ流入します。研究者らがこれらのチャネルを阻害するとNETはほぼ消失し、逆に特別な活性化剤でチャネルを刺激するとXKR8を欠く細胞でもNET形成を回復させることができました。
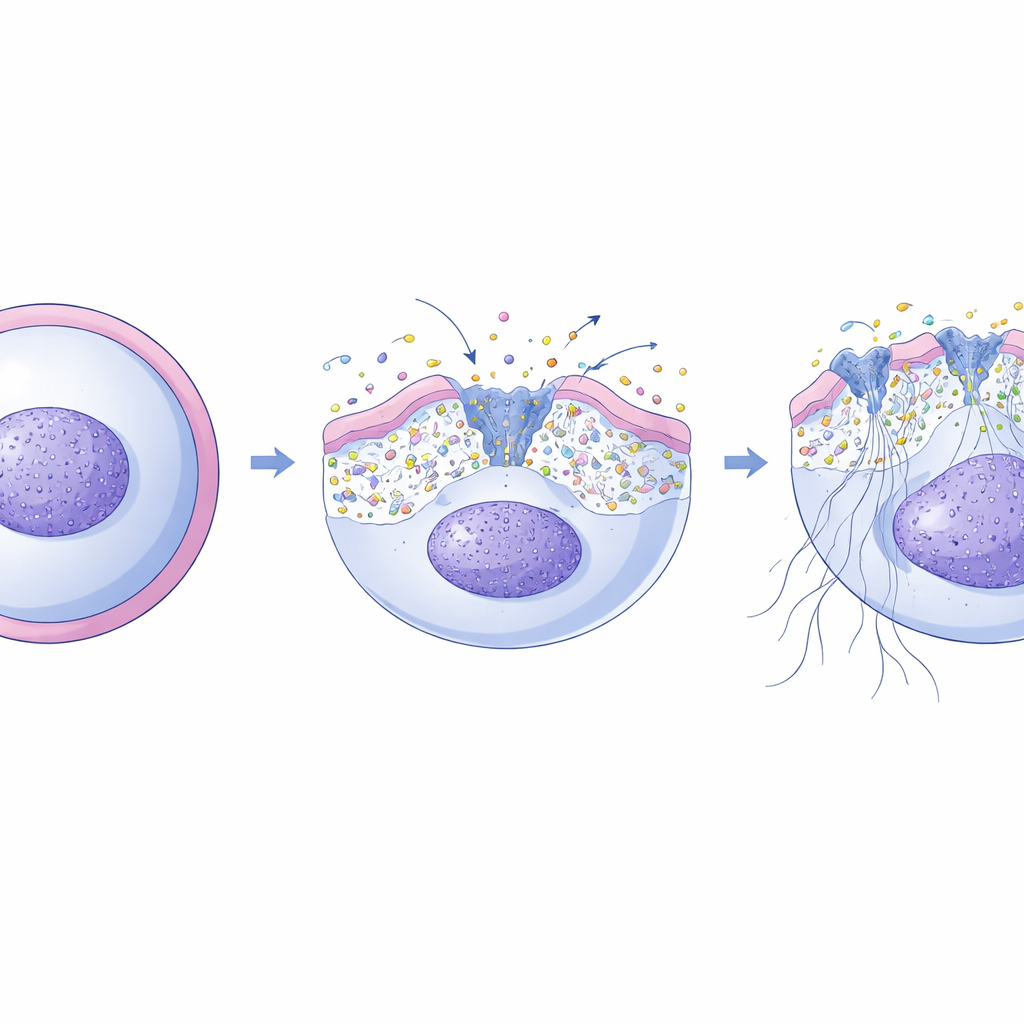
罠が機能しないとき:肺障害と真菌感染
この膜スイッチが生体内でどのような意味を持つかを調べるために、研究チームはXKR8を完全に欠くか、カスパーゼ-3によって切断されない変異型を持つように操作したマウスを用いました。細菌成分で誘発される急性肺障害モデルでは、正常マウスは肺内で豊富なNET、肺液中の高レベルの遊離DNA、および著しい組織損傷を示しました。XKR8活性が低下したマウスは同数の好中球を動員しましたが、生成されるNETははるかに少なく、肺損傷も軽度でした。これはこのXKR8スイッチがこの状況で有害なNET放出の主要な駆動因子であることを示唆します。対照的に、肺が Candida albicans に感染した場合、機能するXKR8スイッチを欠くマウスは深刻な不利な立場に立たされました:彼らははるかに少ないNETを形成し、肺や他の臓器により多くの真菌負荷を抱え、肺胞内への出血が多く、致命的な感染で死亡する頻度が高くなりました。注目すべきは、機械感受性カルシウムチャネルの一つを活性化する薬剤が、好中球にXKR8を欠くマウスにおいて真菌制御を部分的に回復させたことです。
二面性を持つ一つの中心レバー
この研究は、多様な危険信号が好中球の単一の膜に基づく意思決定点に収束する統一的なメカニズムを明らかにしました。酸化バーストはカスパーゼ-3を活性化し、それがXKR8をオンにして膜脂質をスクランブルし、膜張力を変化させ、カルシウムチャネルを開き、最終的にNETの発射につながります。一般読者向けのメッセージは、私たちの免疫系が好中球表面の精密に調節された“脂質レバー”を使ってDNAの網をいつ展開するかを決めているということです。レバーをある方向に倒せば大型の真菌侵入を除去するのに役立ちますが、過度にあるいは誤ったタイミングで倒すと、肺障害や関節炎のような無菌性炎症を悪化させる可能性があります。この経路は保護と損傷の交差点に位置するため、カスパーゼ-3—XKR8—カルシウム軸を標的にすることで、有害なNETを抑えるか有益なNETを強化するか、臨床のニーズに応じた新しい戦略を提供できる可能性があります。
引用: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
キーワード: 好中球外罠, XKR8スクランブラー, 自然免疫, 真菌性肺感染, 急性肺障害