Clear Sky Science · ar
اضطراب التماثل الدهني بواسطة XKR8 ينظم تكوّن مصائد العدلات خارج الخلايا ويُثبِّط العدوى الفطرية
كيف يفاجئ مدافعونا الأوّليون بمصيدة مخفية
عندما تغزو الجراثيم، يُعَدّ العدّل (النيتروفيل) واحداً من أسرع الخلايا استجابةً في الجسم؛ وهو خلية دم بيضاء يمكنها أن تُطلق شبكات لزجة من الحمض النووي لالتقاط الميكروبات. تُسمّى هذه البنى مصائد العدلات خارج الخلايا، أو NETs، وهي حلفاء قويون في مكافحة العدوى لكن يمكن أن تُلحِق أيضاً تلفاً بأنسجتنا إذا أفرِج عنها في وقت غير مناسب. يكشف هذا البحث عن "مفتاح تحكّم" مفاجئ في الغشاء الخارجي للعدّل يساعد على اتخاذ قرار متى تُنسَق هذه الشُّبَكات من الحمض النووي، ويبيّن كيف يحمي هذا المفتاح الرئتين من غزاة فطريين خطِرين.
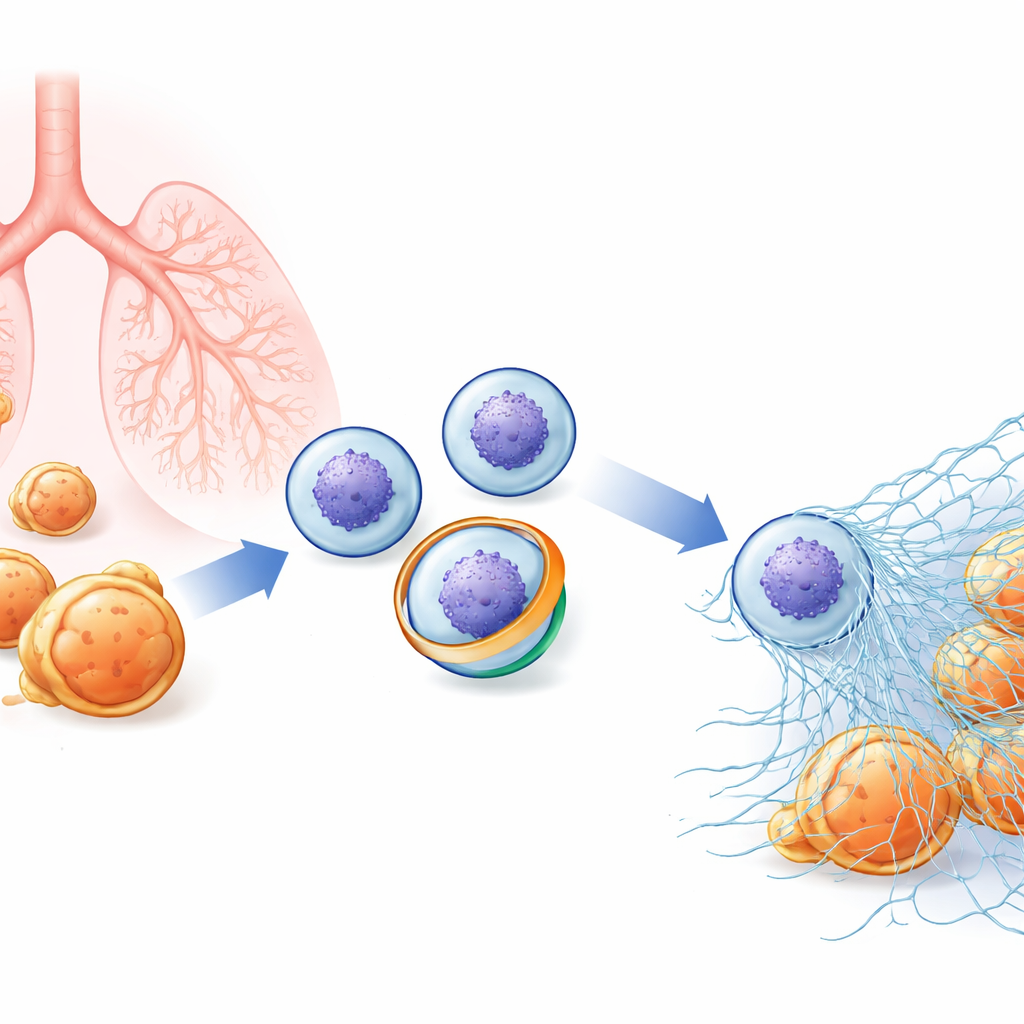
شبكة مخفية داخل خلايا الجهاز المناعي
تتجول العدلات في الدم مستعدة لِمهاجمة البكتيريا والفطريات. إلى جانب ابتلاع الميكروبات، يمكنها أن تنفجر إلى الخارج مطلقةً الكروماتين المفكك (المادة التي تُكوِّن الكروموسومات) المغطّى بإنزيمات مضادة للميكروبات. تُشكّل هذه الألياف اللاصقة مصائد NETs التي تُشتّت المُمْرضات لتُقتل محلياً. وبما أن NETs فعّالة للغاية، يجب أن يكون إطلاقها محكماً بشدة: فالقليل جداً قد يؤدي إلى تفاقم العدوى، والكثير جداً قد يغذي أمراضاً مناعية ذاتية وإصابة رئوية وتجلطات دموية. شكّ الباحثون أن تغيّرات دقيقة في الغشاء الخارجي للعدّل قد تكون خطوة مبكرة في تقرير ما إذا كانت الخلية ستخضع لهذا الحدث الدرامي المسمى "NETosis"، لكن اللاعبين الجزيئيين الرئيسيين كانوا مجهولين.
مفاتيح الغشاء المسماة XKR8
ركّز الفريق على بروتين اسمه XKR8، يُعثر عليه بمستويات عالية بشكل خاص في العدلات. XKR8 هو "ممحِّل" — بروتين يمكنه قلب الدهون بين الطبقات الداخلية والخارجية لغشاء الخلية، ممحوّاً التفاوت الاعتيادي بين الجانبين. في سياقات أخرى، مثل موت الخلية المبرمج، يُعرف أن XKR8 يكشف إشارة دهنية على سطح الخلية تميّز الخلايا المحتضرة لإزالتها. هنا أظهر المؤلفون أنه أثناء تكوّن NETs، تظهر هذه الإشارة الدهنية قبل أن يصبح الغشاء مسالاً وقبل إطلاق الحمض النووي، ما يميّز تلك العدلات المهيَّأة لتشكيل NETs. عندما أزالوا XKR8 من عدلات الفئران والبشر، لم تعد الخلايا قادرة على تنفيذ خطوة التقليب المبكرة هذه وفشلت تقريباً في تكوين NETs استجابةً للعديد من المحفّزات الكيميائية والميكروبية.
من إعادة ترتيب الغشاء إلى موجة من الكالسيوم
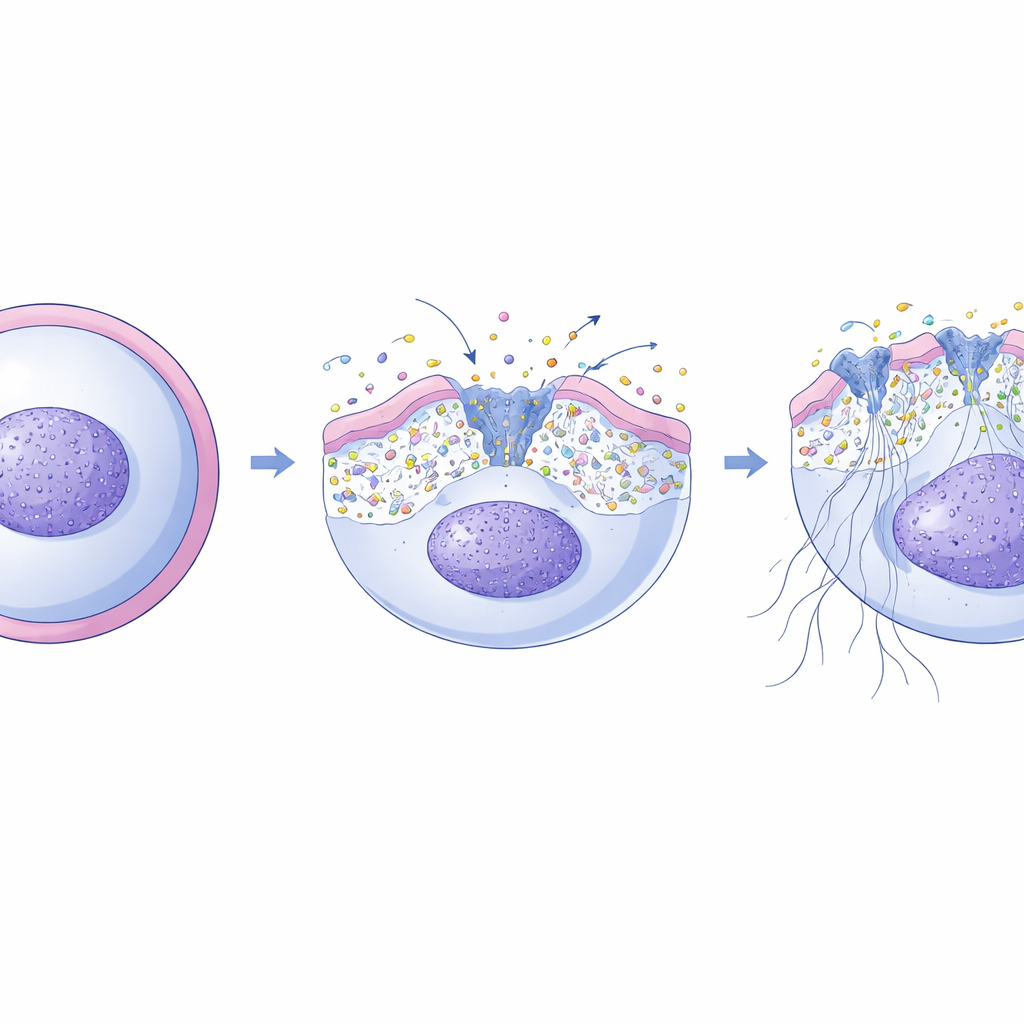
من المعروف أن تكوّن NET يتوقف على ارتفاع مستوى الكالسيوم داخل العدلات، مما يُفعّل إنزيمات تُرخي الكروماتين وتسمح بخروج الحمض النووي. اكتشف الباحثون أن XKR8 في صميم هذه العملية. بعد اندفاع أكسدة داخل العدّل، يقوم إنزيم منفّذ يُدعى كاسبيز-3 بقطع وتنشيط XKR8. وبمجرد تشغيله، يعيد XKR8 بسرعة توزيع عدة أنواع من الدهون عبر الغشاء، وليس مجرد إشارة "كُلْني" واحدة. باستخدام مجسّات فلورية، أظهر الفريق أن هذا التبديل يغيّر توتر الغشاء الفيزيائي. بدوره، يفتح هذا التوتر الميكانيكي مجموعة من قنوات الكالسيوم الحساسة للضغط الموجودة في الغشاء، ما يسمح لأيونات الكالسيوم بالتدفّق إلى داخل الخلية بالوقت الذي يتم فيه تكوّن NETs بدقة. إذا قام الباحثون بحجب هذه القنوات، تلاشت NETs إلى حد كبير؛ وإذا نَبّهوا القنوات بمنشطات خاصة، استطاعوا استعادة تكوّن NETs حتى في الخلايا التي تفتقر إلى XKR8.
عندما تفشل المصائد: إصابة الرئة والعدوى الفطرية
لفهم معنى هذا المفتاح الغشائي في الحيوانات الحية، درس الفريق فئراناً مُهندَسة إما تفتقر تماماً إلى XKR8 أو تحمل نسخة طافرة لا يمكن لكاسبيز-3 أن يقطعها. في نماذج إصابة الرئة الحادة الناجمة عن مكوّنات بكتيرية، طوّرت الفئران الطبيعية NETs وفيرة في رئتيها، ومستويات مرتفعة من الحمض النووي الحر في سائل الرئة، وتلف نسيجي واضح. الفئران ذات نشاط XKR8 المعيب جَنَبت نفس عدد العدلات لكنها أنتجت NETs أقل بكثير وتعرّضت لإصابة رئوية أقل، ما يشير إلى أن مفتاح XKR8 هو محرك رئيسي لإطلاق NETs الضارة في هذا السياق. بالمقابل، عندما أُصيبت الرئتان بفطر Candida albicans، كانت الفئران التي تفتقر إلى مفتاح XKR8 في وضعية محفوفة بالمخاطر: كونها شكّلت NETs أقل بكثير، حملت أعباء فطرية أعلى في رئتيها وأعضاء أخرى، نزفت أكثر إلى المساحات الهوائية، وماتت بمعدلات أعلى جرّاء العدوى الغالبة. ومن الجدير بالذكر أن دواءً ينشّط إحدى قنوات الكالسيوم الحساسة للضغط أعاد جزئياً السيطرة على الفطريات في الفئران التي كانت عدلاتها تفتقد XKR8.
رافعة مركزية بوجهين
يكشف هذا العمل عن آلية موحِّدة تتلاقى عندها إشارات خطر متعددة على نقطة قرار غشائية واحدة في العدلات. تؤدي الاندفاعات التأكسدية إلى تفعيل كاسبيز-3، الذي يشغّل XKR8 لقلب دهون الغشاء، وتغيير توتره، وفتح قنوات الكالسيوم، مما يبلغ ذروة إطلاق NETs. للقراء غير المختصين، الرسالة أن جهازنا المناعي يستخدم "رافعة دهنية" مضبوطة بدقة على سطح العدلات ليقرر متى يرمي شبكات الحمض النووي. إمالة هذه الرافعة في اتجاه واحد تساعد على إزالة الغزاة الفطريين الكبار؛ أما إمالتها كثيراً أو في الوقت الخاطئ فيمكن أن تفاقم الالتهابات المعقمة مثل إصابة الرئة أو التهاب المفاصل. وبما أن هذا المسار يقف عند مفترق طرق الحماية والضرر، قد يوفّر استهداف محور كاسبيز-3–XKR8–الكالسيوم استراتيجيات جديدة إما لكبح NETs الضارة أو لتعزيز NETs المفيدة، بحسب الحاجة السريرية.
الاستشهاد: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
الكلمات المفتاحية: مصائد العدلات خارج الخلايا, ممحِّل XKR8, المناعة الفطرية, عدوى الرئة الفطرية, إصابة الرئة الحادة