Clear Sky Science · tr
CSN5i-3, COP9 sinyalosomunun ortosterik moleküler yapıştırıcı inhibitörüdür
Neden Yeni Bir İlaç Türü Önemli?
Birçok modern ilaç, aşırı etkin enzimleri kapatarak çalışır, fakat sıklıkla çok sayıda hedefe dokunur ve yan etkilere yol açar. Bu çalışma, küçük bir molekülün hücresel kontrol makinesinin ana elemanlarından biri olan COP9 sinyalosomunu çok daha hassas bir şekilde kapatmasının şaşırtıcı bir yolunu ortaya koyuyor. Hem geleneksel bir bloke edici hem de bir “moleküler yapıştırıcı” gibi davranarak CSN5i-3 bileşiği, daha güvenli ve daha seçici ilaçlar tasarlamak için yeni bir stratejiye işaret ediyor.
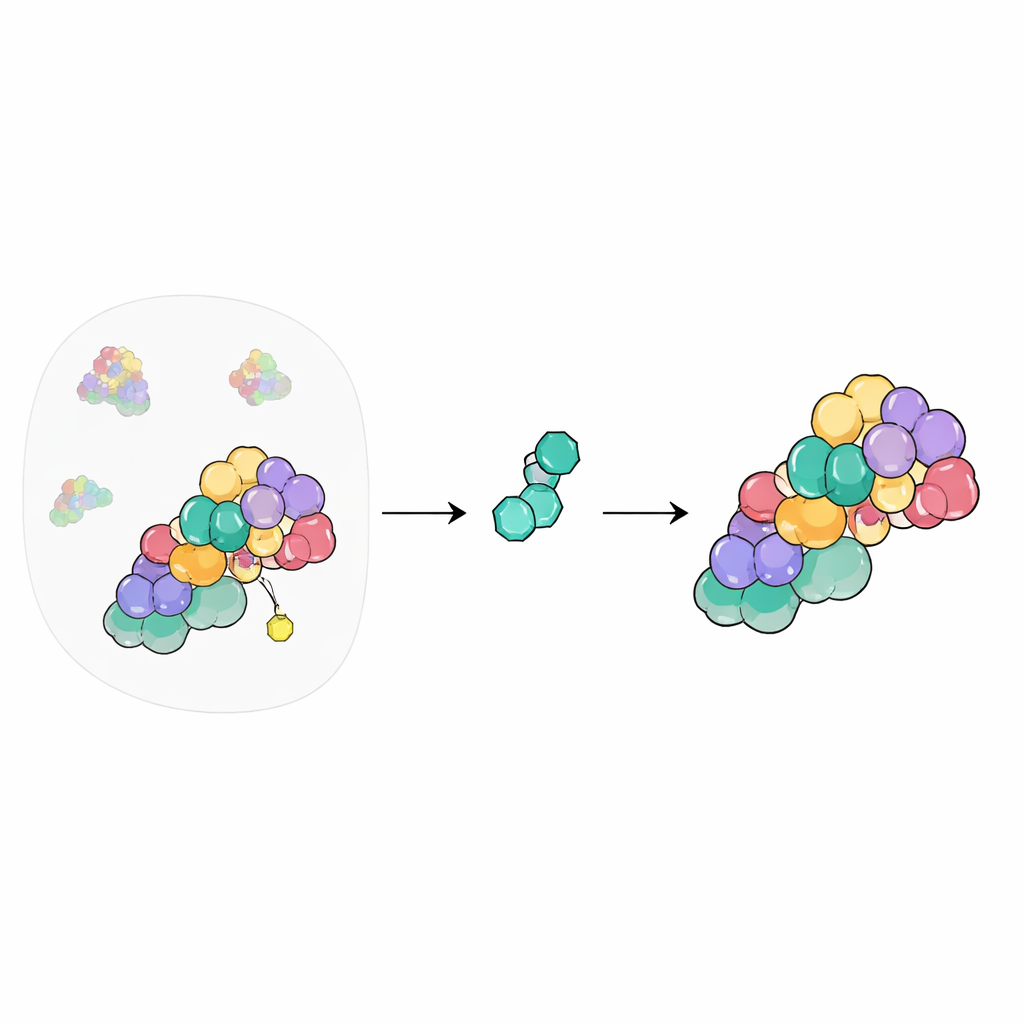
Hücrenin Geri Dönüşüm Santrali
Hücrelerimizde, istenmeyen veya hasarlı proteinleri yok edilmek üzere işaretleyen devasa bir makine ağı bulunur. Bu sistemin merkezinde cullin–RING ligazlar vardır; proteinleri bertaraf etmek için gereken araçları bir araya getiren iskeletlerdir. Bunların etkinliği, küçük bir protein olan NEDD8’in eklenip çıkarılmasıyla açılıp kapanır. COP9 sinyalosomu (CSN), bu kapatma anahtarı olarak görev yapar; NEDD8’i cullinlerden keserek sistemin resetlenmesini sağlar. Bu anahtarın yüzlerce hücresel sürece değmesi nedeniyle, kimyagerler uzun zamandır CSN’i ilaçlarla kontrol etmek istiyorlardı, ancak bunu güvenli yapmak zorludur.
Büyük Etkiye Sahip Küçük Bir Molekül
CSN5i-3 bileşiği, CSN’nin kesme alt birimi CSN5’in çalışır alanını tıpkı bir şişedeki mantar gibi tıkamak üzere tasarlanmıştı. Basit testlerde, bu bölgeye bağlanması yalnızca orta düzeydedir, mikromolar aralıkta, ki bu normalde güçlü bir ilaç olmazdı. Buna karşın hücresel reaksiyonlarda CSN5i-3, bağlanma gücünün gösterdiğinden yaklaşık bin kat daha güçlü olarak nanomolar seviyelerde CSN’yi kapatıyor. Önceki çalışmalar ayrıca bileşiğin “kompetitör olmayan” yani substrat zaten yerindeyken enzime bağlanmayı tercih eden bir inhibitör gibi davrandığına işaret etmişti; bu durum doğrudan aktif bölge bloklayıcıları için nadir görülür. Bu tuhaflıklar, daha ince bir mekanizmanın işbaşında olabileceğini gösteriyordu.
Moleküler Kucaklaşmayı Görmek
Bunu anlamak için yazarlar, CSN’yi birkaç durumda görselleştirmek amacıyla yüksek çözünürlüklü kriyo–elektron mikroskopisi kullandılar: yalnızken, NEDD8 ile modifiye olmuş cullin partnerleriyle ve CSN5i-3 varlığında veya yokluğunda. Önce, NEDD8’in kuyruğu ve cullin bağlanma noktasının CSN5’in oluğuna sıkıca yerleştiği bir “kesim öncesi” durum yakaladılar; bu yapı, NEDD8’den cullin’e ve yardımcı bir protein olan RBX üzerinden CSN’nin geri kalanına uzanan bir dizi protein–protein temasla tutulan bir düzen gösteriyordu. Bu yapı, CSN’nin farklı cullinleri nasıl tanıyıp doğru geometrinin korunmasını sağlayarak NEDD8–cullin bağını nasıl kırdığını açıklıyor.
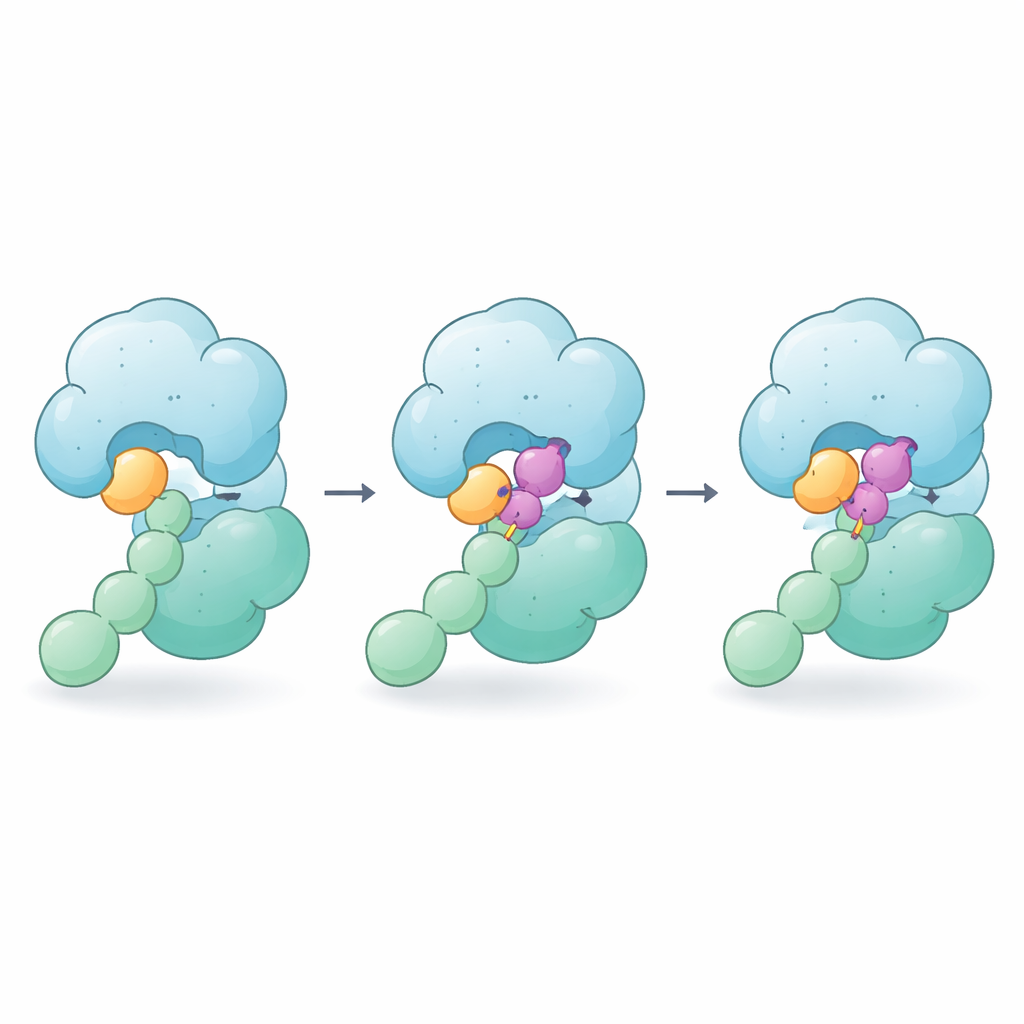
Yapıştırıcı Kesmeden Nasıl Tutuyor?
CSN5i-3 eklenince, NEDD8–cullin bağının yerleşeceği aynı oluğa girerek klasik bir tıkaç gibi davranıyor. Ancak görüntüler molekülün daha fazlasını yaptığını gösteriyor: bir ucu NEDD8’in kuyruğuna yaslanırken diğeri cullin’in yakın bölgesine baskı yapıyor. Etkilen, CSN5i-3, NEDD8 ile CSN5 arasındaki zayıf teması güçlendiren bir köprü haline geliyor. Biyofiziksel ölçümler, bileşik varlığında serbest NEDD8’in aniden CSN’ye güçlü şekilde bağlandığını ve tüm enzim–substrat kompleksinin çok daha stabil hale geldiğini gösteriyor. Yazarlar bu davranışı “ortosterik moleküler yapıştırıcı” olarak adlandırıyorlar çünkü ilaç normal aktif sitede (ortosterik) oturuyor ama aynı zamanda enzim ile substratı birbirine yapıştırıyor.
Hücre Genelinde Yayılan Etkiler
CSN’yi NEDD8 ile süslenmiş partnerlerine kilitleyerek CSN5i-3, bu komplekslerin hücrelerde ne kadar süre kaldığını değiştiriyor. Çapraz bağlama ve kütle spektrometrisi kullanarak ekip, hangi proteinlerin tedavi öncesi ve sonrası CSN ile ilişkili kaldığını haritaladı. Bileşiğin varlığında cullinlerin ve birçok adaptörünün daha sık CSN’ye bağlı bulunduğunu tespit ettiler; bu durum yapıştırıcı etkisinin neden olduğu reaksiyon “trafik sıkışıklıklarıyla” tutarlı. Dikkat çekici biçimde bazı substrat reseptörleri daha az stabil hale gelip yıkılırken, diğerleri CSN ile birlikte tuzağa düşüyor. Bu sonuç çeşitliliği, bireysel reseptörlerin CSN ile nasıl temas ettiklerine dair ince farkların, bir ortosterik moleküler yapıştırıcı uygulandığında korunup korunmayacaklarını veya ortadan kaldırılacaklarını belirleyebileceğini öne sürüyor.
Geleceğin İlaçları İçin Anlamı
Uzman olmayanlar için ana mesaj, CSN5i-3’ün bir ilacın aynı anda hem tıkaç hem de yapıştırıcı olabileceğini göstermesidir. Hedefine kendi başına çok sıkı bağlanması gerekmeksizin, molekül tuzağa yardımcı olduğu substratın gücünü ödünç alarak gerçek dünyada yüksek etkinlik sağlıyor; temel bağlanma afinitesi mütevazı olsa da. Yapıştırıcı teması belirli substratları tanıyacak şekilde ayarlanabildiğinden, bu yaklaşım teoride zararlı enzim eylemlerini engelleyen ama diğerlerini koruyan ilaçlar tasarlamak için kullanılabilir; böylece yan etkiler azaltılabilir. Yazarlar “ortosterik moleküler yapıştırıcı inhibitörleri”ni kesme veya proteinleri modifiye etme süreçlerine dahil birçok enzim için uygulanabilecek yeni bir bileşik sınıfı olarak öneriyor; bu da hücrenin en yoğun makinelerini daha seçici kontrol etme yolunu açıyor.
Atıf: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Anahtar kelimeler: moleküler yapıştırıcı, COP9 sinyalosomu, protein yıkımı, enzim inhibitörleri, ilaç keşfi