Clear Sky Science · de
CSN5i-3 ist ein orthosterischer molekularer Klebstoff-Inhibitor des COP9-Signaloms
Warum eine neue Wirkstoffklasse wichtig ist
Viele moderne Medikamente wirken, indem sie überaktive Enzyme abschalten, treffen dabei aber oft zu viele Ziele und führen zu Nebenwirkungen. Diese Studie enthüllt eine überraschende Art, wie ein kleines Molekül eine zentrale zelluläre Schaltzentrale — das COP9-Signalom — deutlich präziser außer Gefecht setzen kann. Indem es sowohl als herkömmlicher Blocker als auch als „molekularer Klebstoff“ wirkt, weist die Verbindung CSN5i-3 auf eine neue Strategie zur Entwicklung sichererer, selektiverer Arzneimittel hin.
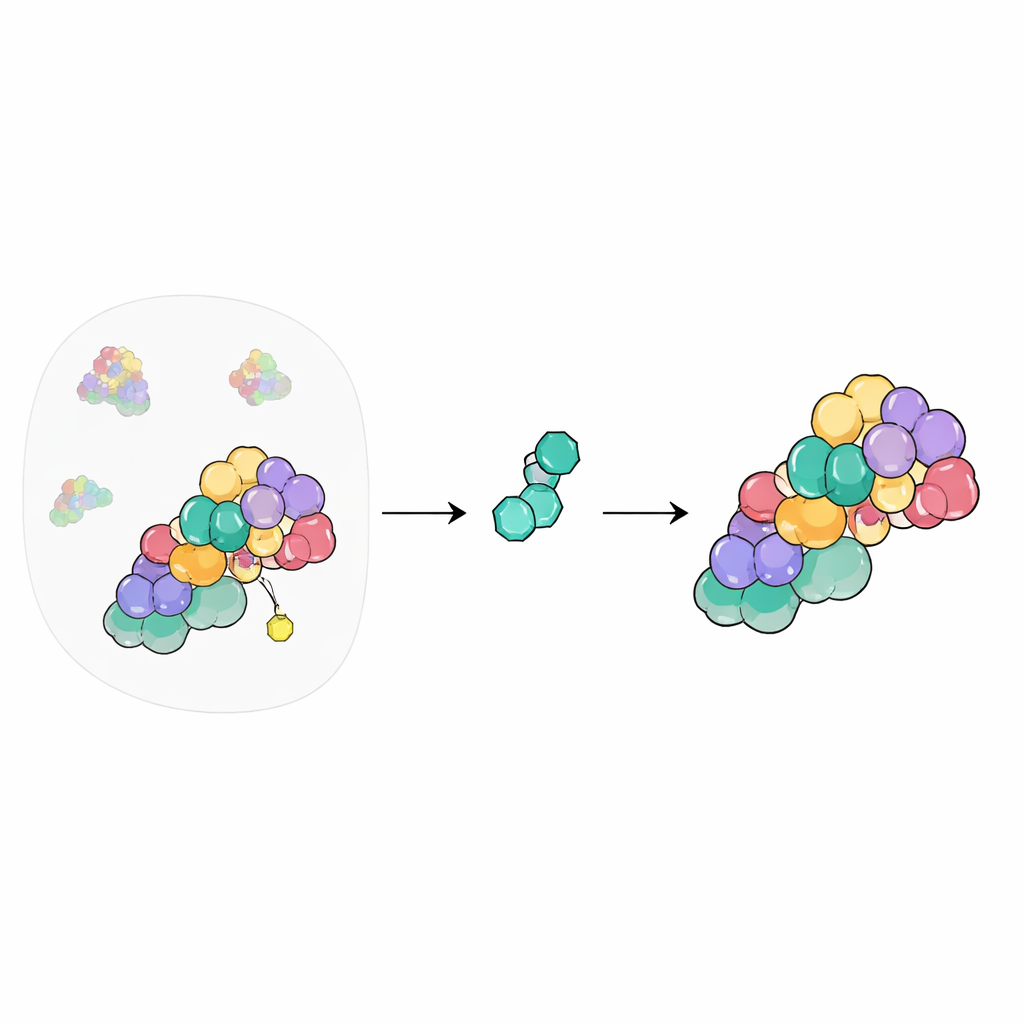
Die Recycling-Schaltzentrale der Zelle
In unseren Zellen markiert ein großes Netzwerk von Maschinen unerwünschte oder beschädigte Proteine, damit sie abgebaut werden können. Im Zentrum dieses Systems stehen cullin–RING-Ligasen, Gerüste, die die benötigten Werkzeuge zusammenbringen, um Proteine zur Entsorgung zu kennzeichnen. Ihre Aktivität wird durch das Anhängen und Entfernen eines kleinen Proteins namens NEDD8 ein- und ausgeschaltet. Das COP9-Signalom (CSN) fungiert als Aus-Schalter, indem es NEDD8 von den Cullinen entfernt, sodass das System zurückgesetzt werden kann. Da diese Schaltzentrale Hunderte zellulärer Prozesse berührt, möchten Chemiker das CSN schon lange mit Medikamenten steuern — das sicher zu tun ist jedoch schwierig.
Ein kleines Molekül mit großer Überraschung
Die Verbindung CSN5i-3 wurde so entworfen, dass sie die Arbeitsstelle der schneidenden Untereinheit CSN5 wie ein Korken verschließt. In einfachen Tests bindet sie diese Stelle nur mäßig gut, im Mikromolarbereich, was normalerweise keinen stark wirksamen Wirkstoff erwarten ließe. Doch in zellulären Reaktionen schaltet CSN5i-3 das CSN in Nanomolar-Bereichen aus — etwa tausendmal stärker, als ihre Bindungsstärke vermuten lässt. Frühere Arbeiten deuteten außerdem darauf hin, dass sie sich wie ein „unkompetitiver“ Inhibitor verhält und lieber an das Enzym bindet, wenn das Substrat bereits gebunden ist — ein Muster, das für direkte Wirkstättenkiller selten ist. Diese Auffälligkeiten deuteten auf einen subtileren Mechanismus hin.
Die molekulare Umarmung sichtbar machen
Um dies zu verstehen, nutzten die Autoren hochauflösende Kryo-Elektronenmikroskopie, um CSN in mehreren Zuständen zu visualisieren: allein, mit seinen NEDD8-ubiquitierten Cullin-Partnern und mit oder ohne CSN5i-3. Zuerst fingen sie einen „vor dem Schnitt“-Zustand ein, in dem der Schwanz von NEDD8 und der Anheftungspunkt am Cullin eng in der Rinne von CSN5 positioniert sind, gehalten von einer Kette von Protein–Protein-Kontakten, die sich von NEDD8 über den Cullin und ein Helferprotein namens RBX bis zum Rest des CSN erstreckt. Diese Struktur erklärt, wie CSN seine Ziele über viele verschiedene Culline hinweg erkennt und zugleich die richtige Geometrie beibehält, um die NEDD8–Cullin-Verbindung zu trennen.
Wie der Klebstoff hält, ohne zu schneiden
Wenn CSN5i-3 zugegeben wird, klemmt es sich in dieselbe Rinne, in der sonst die NEDD8–Cullin-Bindung sitzen würde, und wirkt damit weiterhin als klassischer Blocker. Die Bilder zeigen jedoch, dass das Molekül mehr tut: Ein Ende liegt an dem Schwanz von NEDD8 an, während das andere auf die nahegelegene Region des Cullins drückt. Tatsächlich wird CSN5i-3 zu einer Brücke, die die schwachen Kontakte zwischen NEDD8 und CSN5 verstärkt. Biophysikalische Messungen zeigen, dass in Gegenwart der Verbindung freies NEDD8 plötzlich fest an CSN bindet und der gesamte Enzym–Substrat-Komplex viel stabiler wird. Die Autoren nennen dieses Verhalten „orthosterischer molekularer Klebstoff“, weil das Medikament in der normalen aktiven Stelle (orthosterisch) sitzt und zugleich Enzym und Substrat zusammenklebt.
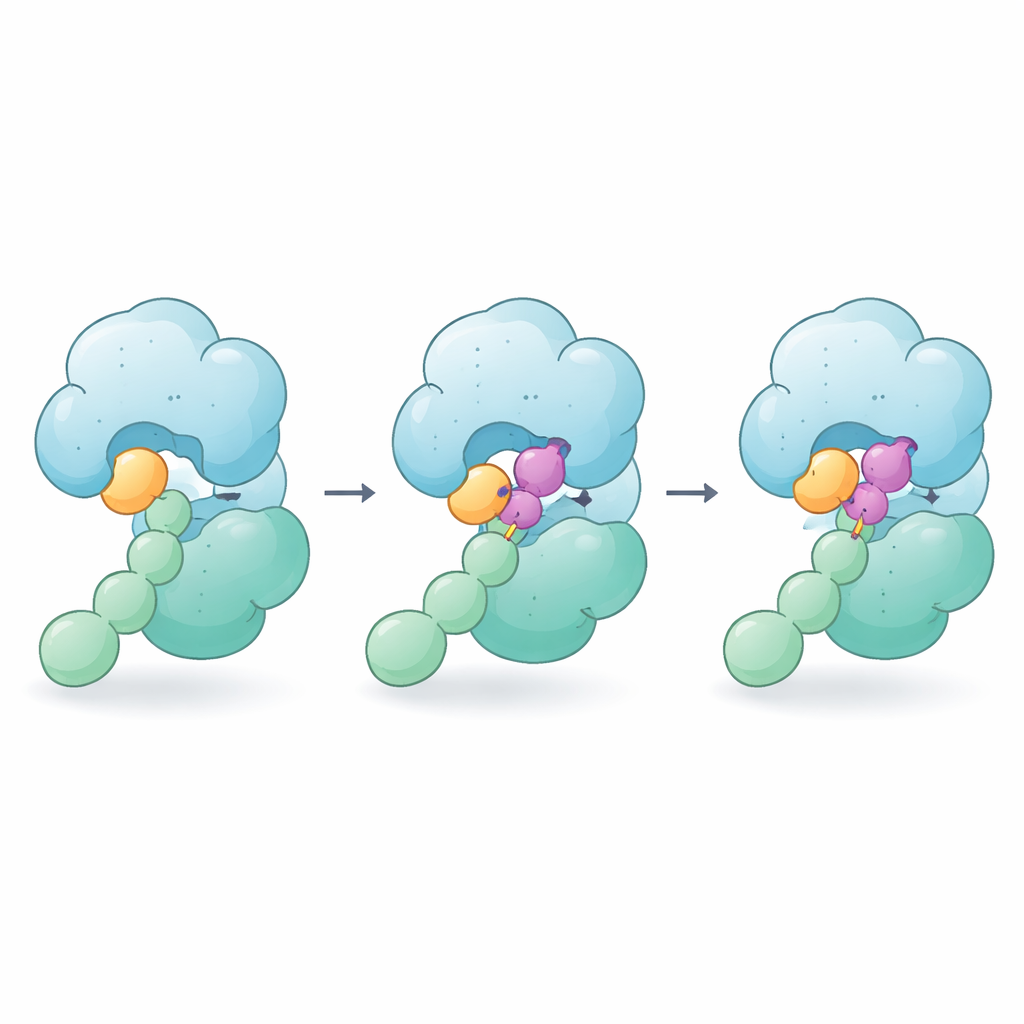
Auswirkungen in der ganzen Zelle
Indem CSN5i-3 das CSN an seine NEDD8-verzierten Partner festbindet, verändert es die Verweildauer dieser Komplexe in der Zelle. Mit Hilfe von Quervernetzung und Massenspektrometrie kartierte das Team, welche Proteine vor und nach der Behandlung mit dem Wirkstoff an CSN gebunden bleiben. Sie fanden, dass Culline und viele ihrer Adapter öfter an CSN gebunden sind, wenn die Verbindung vorhanden ist, was mit einem Reaktions-„Stau“ durch den Klebstoffeffekt übereinstimmt. Auffällig ist, dass einige Substrat-Rezeptoren weniger stabil werden und abgebaut werden, während andere zusammen mit CSN eingeschlossen bleiben. Diese Vielfalt an Ergebnissen legt nahe, dass subtile Unterschiede darin, wie einzelne Rezeptoren das CSN berühren, entscheiden können, ob sie geschützt oder eliminiert werden, wenn ein orthosterischer molekularer Klebstoff angewendet wird.
Was das für künftige Medikamente bedeutet
Die Hauptaussage für Nichtfachleute ist, dass CSN5i-3 zeigt, wie ein Wirkstoff zugleich Korken und Klebstoff sein kann. Statt selbst extrem stark an sein Ziel binden zu müssen, leiht sich das Molekül Stabilität von genau dem Substrat, das es einzufangen hilft, und erreicht so hohe Wirksamkeit im realen Kontext trotz nur mäßiger Grundaffinität. Da die Klebstoffkontakte so abgestimmt werden können, dass sie bestimmte Substrate erkennen, könnte dieser Ansatz theoretisch genutzt werden, um Medikamente zu entwerfen, die schädliche Enzymwirkungen blockieren und andere verschonen — was Nebenwirkungen reduziert. Die Autoren schlagen „orthosterische molekulare Klebstoff-Inhibitoren“ als neue Verbindungsklasse vor, die auf viele Enzyme angewendet werden könnten, die Proteine schneiden oder modifizieren, und eröffnen damit einen Weg zu selektiverer Kontrolle der aktivsten zellulären Maschinen.
Zitation: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Schlüsselwörter: molekularer Klebstoff, COP9-Signalom, Proteinabbau, Enzymhemmer, Arzneimittelentwicklung