Clear Sky Science · pt
CSN5i-3 é um inibidor tipo “cola molecular” ortostérico do complexo COP9 signalosome
Por que um novo tipo de medicamento importa
Muitos medicamentos modernos atuam desligando enzimas hiperativas, mas frequentemente atingem alvos demais e causam efeitos colaterais. Este estudo revela uma maneira sorprendente pela qual uma pequena molécula pode desativar com muito mais precisão uma máquina celular de controle central, o COP9 signalosome. Agindo tanto como um bloqueador convencional quanto como uma “cola molecular”, o composto CSN5i-3 aponta para uma nova estratégia de projetar fármacos mais seguros e seletivos.
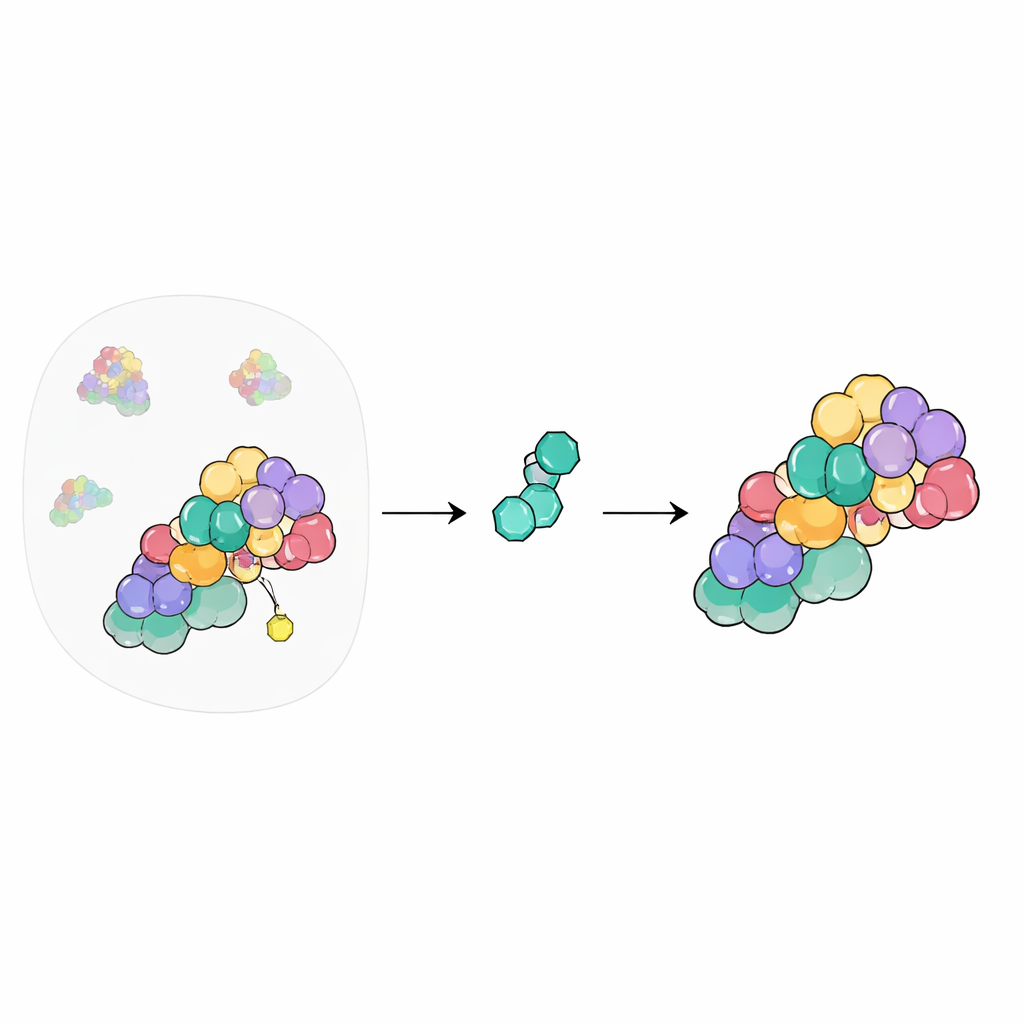
O painel de controle da reciclagem celular
Dentro das nossas células, uma enorme rede de máquinas marca proteínas indesejadas ou danificadas para que possam ser destruídas. No centro desse sistema estão as cullin–RING ligases, estruturas que reúnem as ferramentas necessárias para sinalizar proteínas para descarte. Sua atividade é ligada e desligada pela adição e remoção de uma pequena proteína chamada NEDD8. O COP9 signalosome (CSN) funciona como o botão de desligar, removendo NEDD8 das cullinas para que o sistema possa ser reiniciado. Como esse painel de controle influencia centenas de processos celulares, químicos têm buscado há muito tempo controlar o CSN com fármacos, mas fazê-lo de forma segura é desafiador.
Uma pequena molécula com uma grande reviravolta
O composto CSN5i-3 foi projetado para tamponar o sítio de trabalho da subunidade catalítica do CSN, a CSN5, como uma rolha numa garrafa. Em testes simples, ele se liga a esse sítio apenas moderadamente, na faixa micromolar, o que normalmente não gera um fármaco potente. No entanto, em reações celulares CSN5i-3 desativa o CSN em níveis nanomolares — cerca de mil vezes mais forte do que sua afinidade sugeriria. Trabalhos anteriores também indicaram que ele se comporta como um inibidor “incompetitivo”, preferindo se ligar à enzima apenas quando o substrato já está presente, um padrão raramente visto em bloqueadores diretos do sítio ativo. Essas estranhezas sugeriam que algo mais sutil estava ocorrendo.
Vendo o abraço molecular
Para entender isso, os autores usaram microscopia crioeletrônica de alta resolução para visualizar o CSN em vários estados: isolado, com seus parceiros cullin modificados por NEDD8, e com CSN5i-3 presente ou ausente. Primeiro capturaram um estado “pré‑corte” no qual a cauda de NEDD8 e o ponto de ligação na cullina estão bem posicionados no sulco da CSN5, mantidos no lugar por uma cadeia de contatos proteína–proteína que se estende de NEDD8 através da cullina e de uma proteína auxiliar chamada RBX até o restante do CSN. Essa estrutura explica como o CSN reconhece seus alvos em muitas cullinas diferentes, mantendo a geometria correta para romper a ligação NEDD8–cullina.
Como a cola mantém sem cortar
Quando CSN5i-3 é adicionado, ele se encaixa no mesmo sulco onde estaria a ligação NEDD8–cullina, funcionando assim como um bloqueador clássico. Mas as imagens revelam que a molécula faz mais: uma extremidade se aninha contra a cauda de NEDD8 enquanto a outra pressiona a região próxima da cullina. Na prática, CSN5i-3 torna-se uma ponte que reforça os contatos fracos entre NEDD8 e a CSN5. Medidas biofísicas mostram que, na presença do composto, NEDD8 livre passa a se ligar fortemente ao CSN, e todo o complexo enzima–substrato torna-se muito mais estável. Os autores chamam esse comportamento de “cola molecular ortostérica” porque o fármaco ocupa o sítio ativo habitual (ortostérico) e ao mesmo tempo cola enzima e substrato.
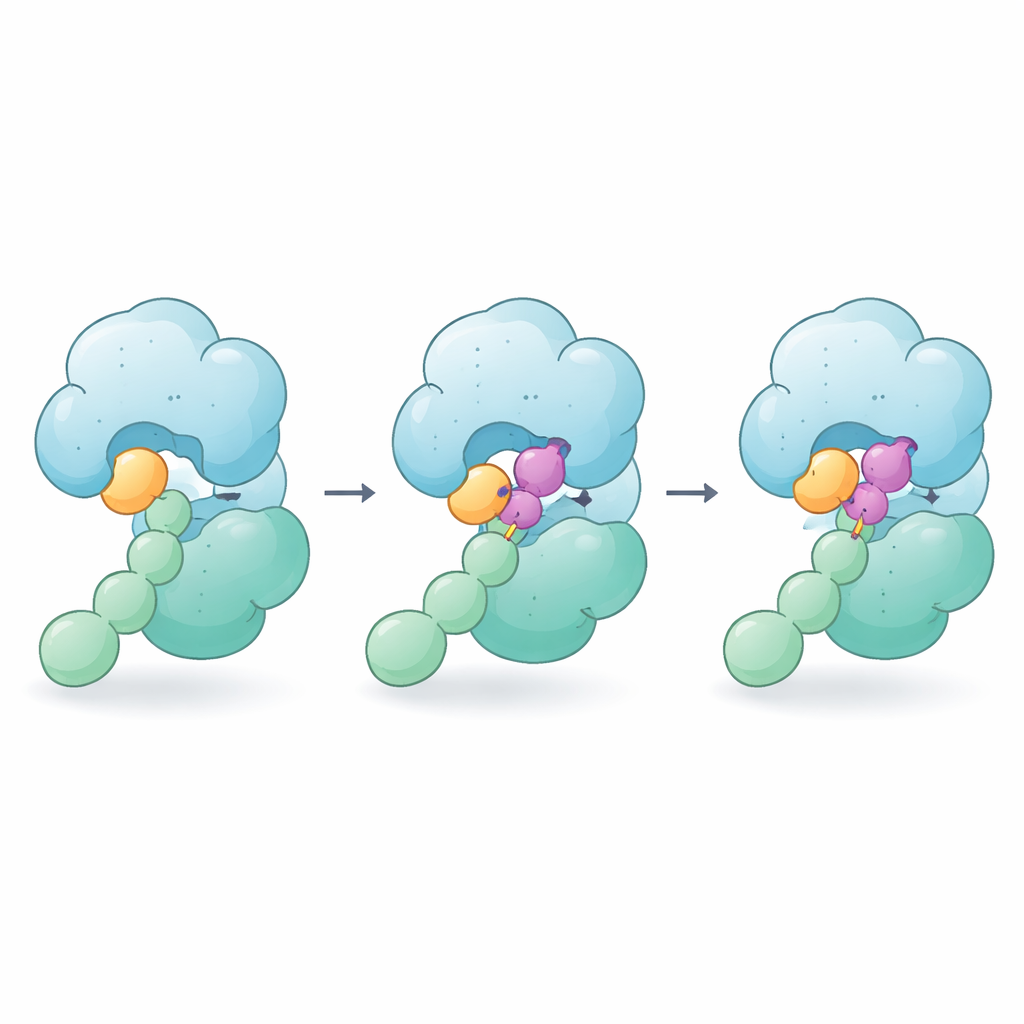
Efeitos em cadeia pela célula
Ao travar o CSN em seus parceiros decorados por NEDD8, CSN5i-3 altera o tempo de permanência desses complexos nas células. Usando crosslinking e espectrometria de massas, a equipe mapeou quais proteínas permanecem associadas ao CSN antes e depois do tratamento. Eles descobriram que cullinas e muitos de seus adaptadores são encontrados com mais frequência ligados ao CSN quando o composto está presente, consistente com “engarrafamentos” da reação causados pelo efeito cola. De forma notável, alguns receptores de substrato tornam‑se menos estáveis e são degradados, enquanto outros ficam aprisionados junto ao CSN. Essa diversidade de desfechos sugere que diferenças sutis na forma como receptores individuais tocam o CSN podem determinar se são protegidos ou eliminados quando uma cola molecular ortostérica é aplicada.
O que isso significa para medicamentos futuros
A mensagem chave para não especialistas é que CSN5i-3 mostra como um fármaco pode ser ao mesmo tempo uma rolha e uma cola. Em vez de precisar se ligar extremamente fortemente ao alvo por si só, a molécula empresta força do próprio substrato que ajuda a prender, alcançando alta potência no mundo real a partir de afinidade básica modesta. Como os contatos de cola podem ser ajustados para reconhecer substratos particulares, essa abordagem poderia, em princípio, ser usada para projetar medicamentos que bloqueiem ações enzimáticas prejudiciais poupando outras, reduzindo efeitos colaterais. Os autores propõem “inibidores cola molecular ortostéricos” como uma nova classe de compostos aplicável a muitas enzimas envolvidas em cortar ou modificar proteínas, abrindo caminho para um controle mais seletivo das máquinas mais ativas da célula.
Citação: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Palavras-chave: cola molecular, COP9 signalosome, degradação de proteínas, inibidores de enzimas, descoberta de fármacos