Clear Sky Science · nl
CSN5i-3 is een orthosterische moleculaire lijmremmer van het COP9-signalosoom
Waarom een nieuw soort geneesmiddel ertoe doet
Veel hedendaagse medicijnen werken door overactieve enzymen uit te schakelen, maar ze raken vaak te veel doelen en veroorzaken bijwerkingen. Deze studie onthult een verrassende manier waarop een kleine molecule een belangrijke cellulaire regelmachine, het COP9-signalosoom, veel preciezer kan stilleggen. Door zowel te fungeren als een conventionele blokker als een “moleculaire lijm” wijst de verbinding CSN5i-3 op een nieuwe strategie voor het ontwerpen van veiligere, selectievere geneesmiddelen.
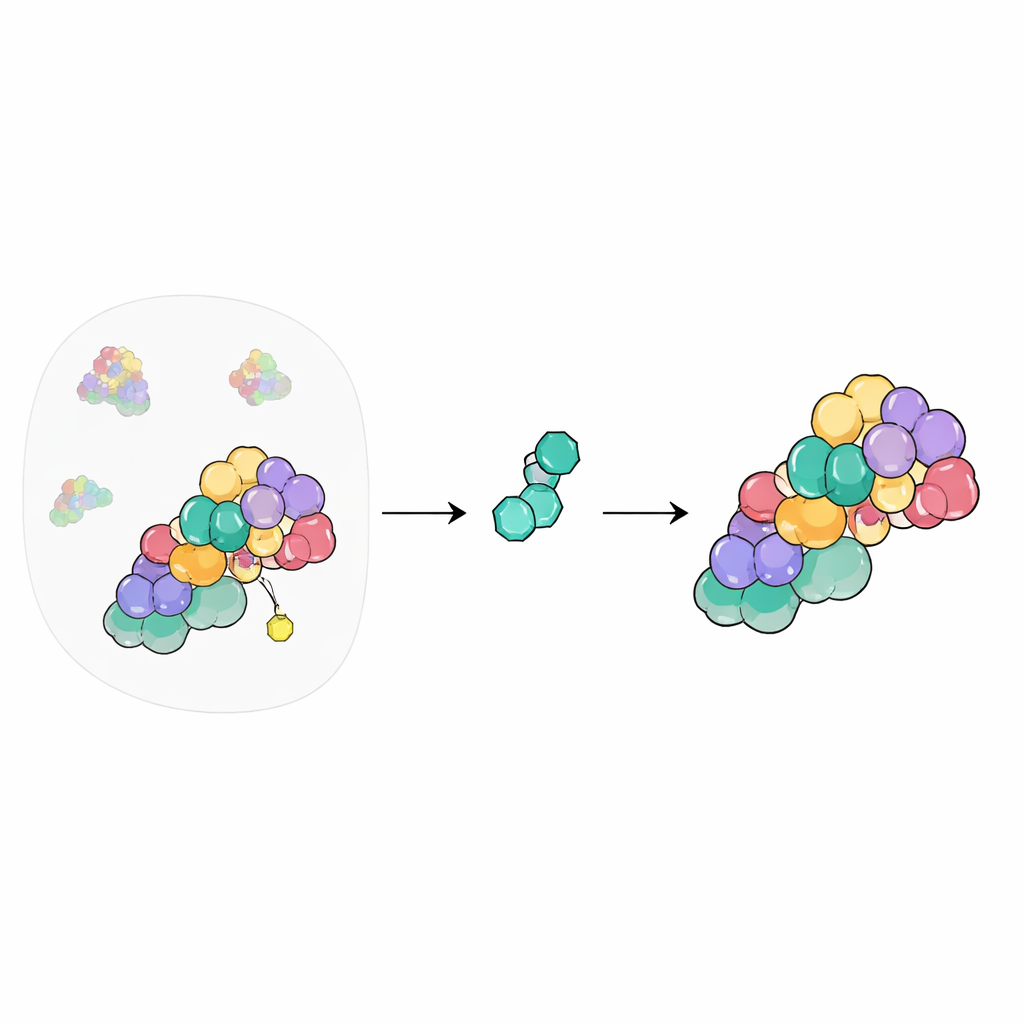
Het recycle‑schakelbord van de cel
Binnenin onze cellen tagt een enorm netwerk van machines ongewenste of beschadigde eiwitten zodat ze vernietigd kunnen worden. Centraal in dit systeem staan cullin–RING-ligases, steigers die de hulpmiddelen samenbrengen die nodig zijn om eiwitten voor verwijdering te markeren. Hun activiteit wordt aan- en uitgezet door het vastmaken en wegnemen van een klein eiwit genaamd NEDD8. Het COP9-signalosoom (CSN) werkt als de uit‑schakelaar, door NEDD8 van cullines af te knippen zodat het systeem kan resetten. Omdat dit schakelbord honderden cellulaire processen raakt, willen chemici al langer CSN met geneesmiddelen kunnen sturen, maar dat veilig doen is een uitdaging.
Een kleine molecule met een grote wending
De verbinding CSN5i-3 is ontworpen om de werkende plaats van CSN’s knippende subeenheid, CSN5, te verstoppen, als een kurk in een fles. In eenvoudige testen bindt het deze plaats slechts matig goed, in het micromolaire bereik, wat normaal geen krachtige remmer oplevert. Toch schakelt CSN5i-3 in cellulaire reacties CSN uit op nanomolaire niveaus—ongeveer duizend keer sterker dan je op basis van de bindingssterkte zou verwachten. Eerder werk wees ook al in de richting van een “onconcurrerende” remmer, die bij voorkeur aan het enzym bindt als het substraat al aanwezig is, een patroon dat zelden wordt gezien bij directe actieve‑plaatsblokkers. Deze eigenaardigheden suggereerden dat er iets subtielers aan de hand is.
De moleculaire omarming zien
Om dit te begrijpen gebruikten de auteurs cryo‑elektronenmicroscopie met hoge resolutie om CSN in verschillende toestanden vast te leggen: alleen, met zijn NEDD8‑gemodificeerde cullinpartners, en met of zonder CSN5i-3. Ze vingen eerst een “pre‑knip” toestand waarin de staart van NEDD8 en het bevestigingspunt op de cullin nauw in de groef van CSN5 liggen, op hun plaats gehouden door een keten van eiwit‑eiwitcontacten die zich uitstrekt van NEDD8 via de cullin en een helperproteïne genaamd RBX naar de rest van CSN. Deze structuur verklaart hoe CSN zijn doelen herkent over vele verschillende cullines terwijl het de juiste geometrie behoudt om de NEDD8–cullin‑verbinding te verbreken.
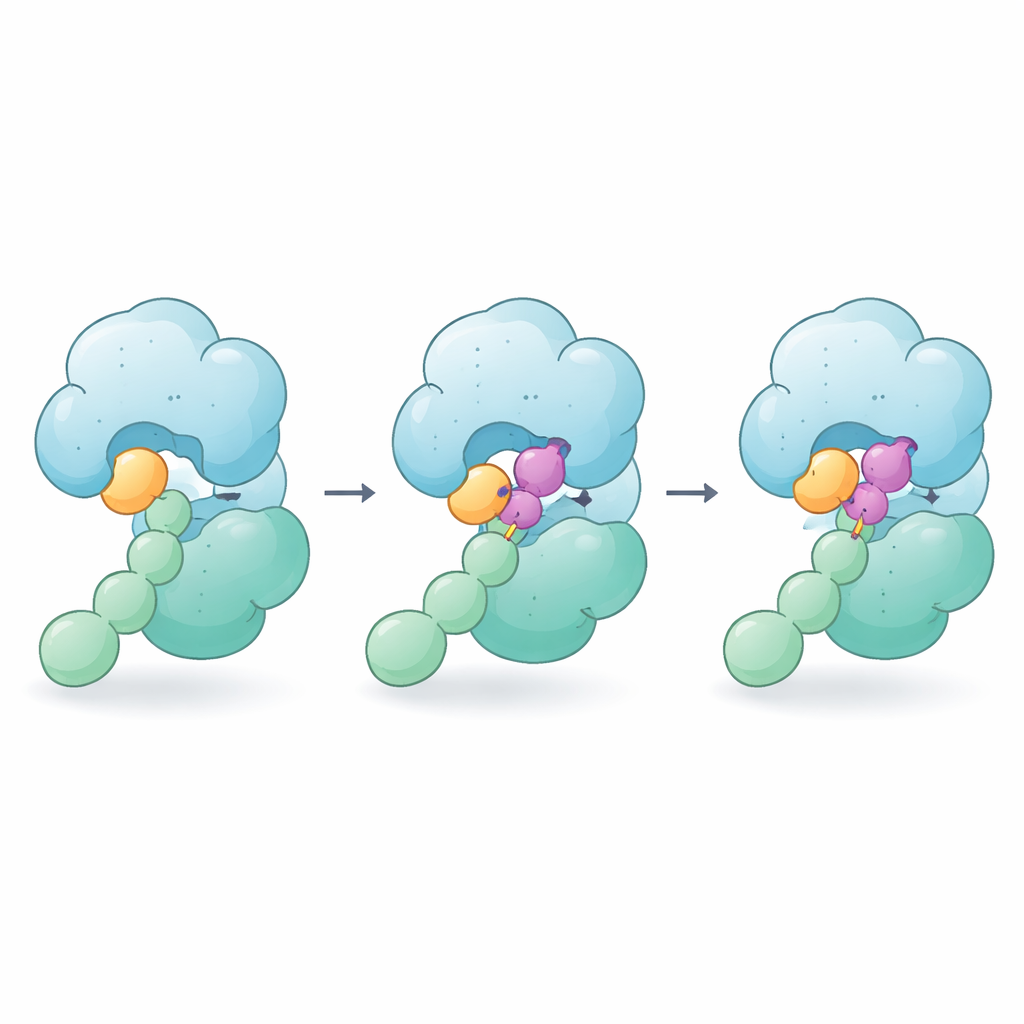
Hoe de lijm vasthoudt zonder te snijden
Als CSN5i-3 wordt toegevoegd, klemt het zich in dezelfde groef waar de NEDD8–cullin‑binding zou zitten, dus het werkt nog steeds als een klassieke blokker. Maar de beelden tonen dat het molecuul meer doet: het ene uiteinde nestelt zich tegen de staart van NEDD8 terwijl het andere drukt op het nabijgelegen gebied van de cullin. In feite wordt CSN5i-3 een brug die de zwakke contacten tussen NEDD8 en CSN5 versterkt. Biofysische metingen laten zien dat, in aanwezigheid van de verbinding, vrij NEDD8 plotseling sterk aan CSN bindt, en het hele enzym–substraatcomplex veel stabieler wordt. De auteurs noemen dit gedrag “orthosterische moleculaire lijm” omdat het middel in de normale actieve plaats (orthosterisch) zit en tegelijkertijd enzym en substraat aan elkaar lijmt.
Rimpel effecten door de cel
Door CSN vast te zetten op zijn NEDD8‑gedecoreerde partners verandert CSN5i-3 hoe lang deze complexen in cellen blijven hangen. Met crosslinking en massaspectrometrie bracht het team in kaart welke eiwitten met CSN geassocieerd blijven voor en na behandeling. Ze vonden dat cullines en veel van hun adaptoren vaker gebonden werden aangetroffen aan CSN wanneer de verbinding aanwezig is, in overeenstemming met reactieverkeer‑“files” veroorzaakt door het lijmeffect. Opvallend is dat sommige substraatreceptoren minder stabiel worden en afgebroken worden, terwijl andere samen met CSN vast komen te zitten. Deze diversiteit aan uitkomsten suggereert dat subtiele verschillen in hoe individuele receptoren CSN raken kunnen bepalen of ze beschermd blijven of worden geëlimineerd wanneer een orthosterische moleculaire lijm wordt toegepast.
Wat dit betekent voor toekomstige medicijnen
De kernboodschap voor niet‑specialisten is dat CSN5i-3 laat zien hoe een geneesmiddel tegelijk een stop en een lijm kan zijn. In plaats van extreem sterk aan zijn doel te hoeven binden, leent het molecuul kracht van het substraat dat het helpt te vangen, en bereikt zo hoge praktische potentie vanuit een bescheiden basale affiniteit. Omdat de lijmcontacten kunnen worden afgestemd op specifieke substraten, zou deze benadering in principe kunnen worden gebruikt om geneesmiddelen te ontwerpen die schadelijke enzymactiviteiten blokkeren terwijl andere ongemoeid blijven, waardoor bijwerkingen verminderen. De auteurs stellen “orthosterische moleculaire lijmremmers” voor als een nieuwe klasse van verbindingen die op veel enzymen betrokken bij het knippen of modificeren van eiwitten toepasbaar zouden kunnen zijn, en zo een weg openen naar selectiever beheer van de drukste machines van de cel.
Bronvermelding: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Trefwoorden: moleculaire lijm, COP9-signalosoom, eiwitafbraak, enzymremmers, geneesmiddelenontwikkeling