Clear Sky Science · sv
CSN5i-3 är en ortosterisk molekylär limhämmare av COP9-signalosomen
Varför en ny sorts läkemedel spelar roll
Många moderna läkemedel fungerar genom att stänga av överaktiva enzymer, men de träffar ofta för många mål och ger biverkningar. Denna studie avslöjar ett överraskande sätt för ett litet molekyl att stänga av en central cellulär kontrollmaskin, COP9-signalosomen, på ett mycket mer precist sätt. Genom att agera både som en konventionell blockerare och som ett ”molekylärt lim” pekar föreningen CSN5i-3 mot en ny strategi för att utforma säkrare, mer selektiva läkemedel.
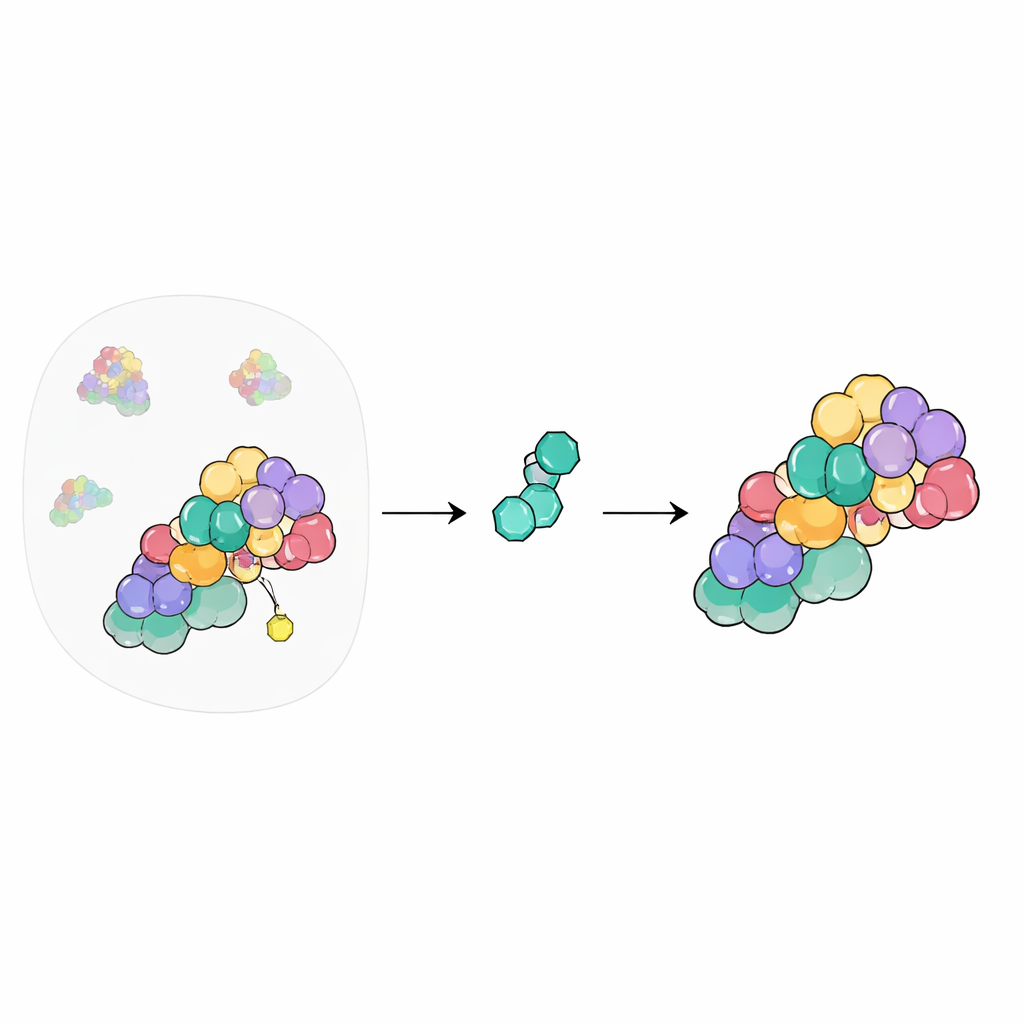
Cellens återvinningscentral
Inne i våra celler taggar ett stort nätverk av maskiner oönskade eller skadade proteiner så att de kan förstöras. I centrum för detta system finns cullin–RING-ligaset, skelett som för samman verktyg som behövs för att märka proteiner för bortskaffande. Deras aktivitet slås på och av genom att fästa och ta bort ett litet protein som kallas NEDD8. COP9-signalosomen (CSN) fungerar som avstängningsknappen genom att avklippa NEDD8 från culliner så att systemet kan återställas. Eftersom denna kontrollpunkt berör hundratals cellulära processer har kemister länge velat styra CSN med läkemedel, men det är utmanande att göra det på ett säkert sätt.
En liten molekyl med en stor vändning
Föreningen CSN5i-3 designades för att täppa till arbetsstället på CSN:s klyvande underenhet CSN5, som en kork i en flaska. I enkla tester binder den denna plats endast måttligt bra, i mikromolärt område, vilket normalt inte skulle göra den till ett potent läkemedel. Ändå slår CSN5i-3 ner CSN i cellprov vid nanomolära nivåer—ungefär tusen gånger starkare än vad dess bindningsstyrka skulle antyda. Tidigare arbete antydde också att den beter sig som en ”okonkurrerande” hämmare och föredrar att binda enzymet först när substratet redan sitter där, ett mönster som sällan ses för direkta aktivsitesblockerare. Dessa egendomligheter föreslog att något mer subtilt var i görningen.
Att se det molekylära omfamnandet
För att förstå detta använde författarna högupplöst kryo-elektronmikroskopi för att visualisera CSN i flera tillstånd: ensam, med sina NEDD8-modifierade cullinpartners och med eller utan CSN5i-3 närvarande. De fångade först ett ”för‐klipps”-tillstånd där svansen av NEDD8 och fästpunkten på cullinen är tätt positionerade i fåra hos CSN5, hållna på plats av en kedja av protein–protein-kontakter som sträcker sig från NEDD8 genom cullinen och ett hjälpprotein kallat RBX till resten av CSN. Denna struktur förklarar hur CSN känner igen sina mål över många olika culliner samtidigt som den behåller rätt geometri för att bryta NEDD8–cullin-länken.
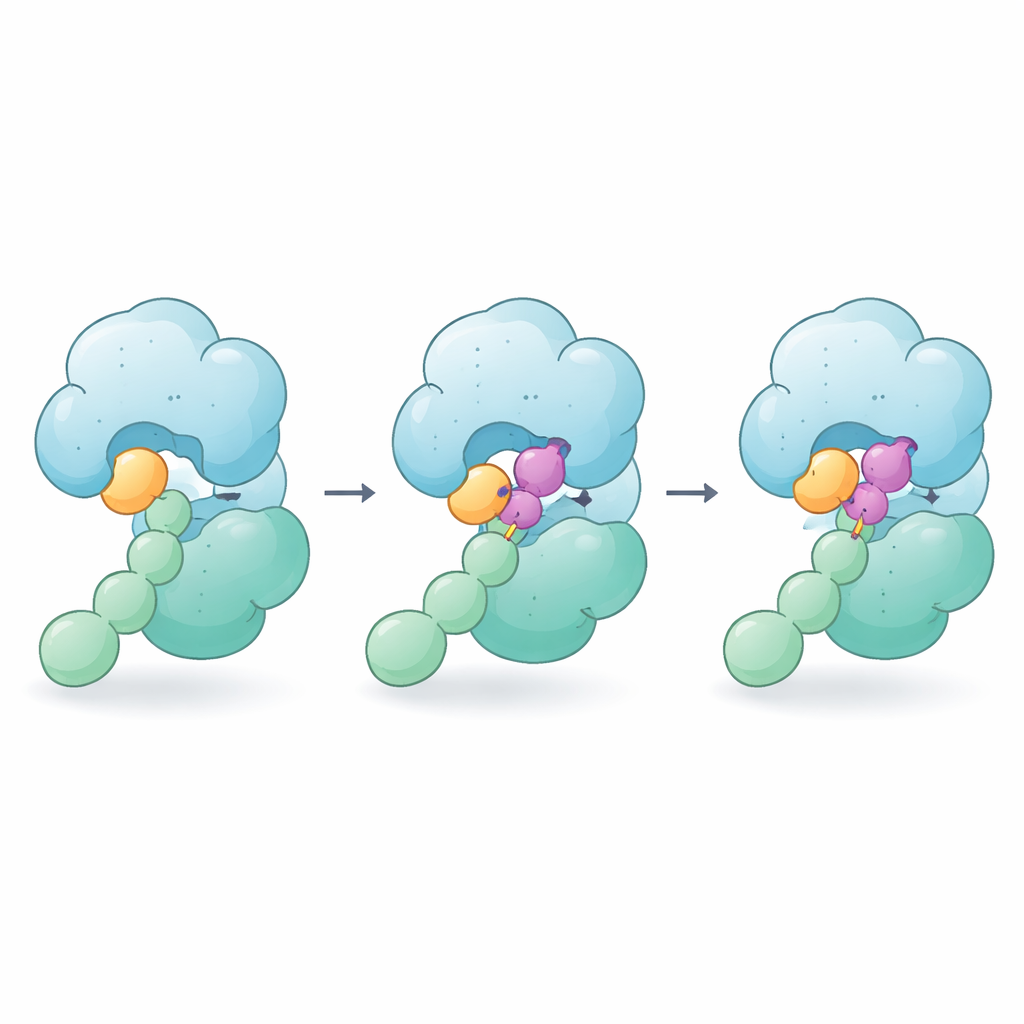
Hur limmet håller utan att klippa
När CSN5i-3 tillsätts kilas den in i samma fåra där NEDD8–cullin-bindningen skulle sitta, så den fungerar fortfarande som en klassisk blockerare. Men bilderna visar att molekylen gör mer: ena änden ligger intill NEDD8-svansen medan den andra trycker mot det närliggande området på cullinen. I praktiken blir CSN5i-3 en bro som förstärker de svaga kontakterna mellan NEDD8 och CSN5. Biofysiska mätningar visar att i närvaro av föreningen binder fri NEDD8 plötsligt starkt till CSN, och hela enzym–substratkomplexet blir mycket mer stabilt. Författarna kallar detta beteende ”ortosteriskt molekylärt lim” eftersom läkemedlet sitter i det normala aktivstället (ortosteriskt) samtidigt som det limmar ihop enzym och substrat.
Kaskadeffekter i hela cellen
Genom att låsa CSN på dess NEDD8-dekorerade partners ändrar CSN5i-3 hur länge dessa komplex dröjer kvar i cellerna. Genom korslänkning och masspektrometri kartlade teamet vilka proteiner som förblir associerade med CSN före och efter behandling. De fann att culliner och många av deras adaptorer oftare hittades bundna till CSN när föreningen var närvarande, i linje med reaktions-”trafikstockningar” orsakade av limeffekten. Slående nog blir vissa substratreceptorer mindre stabila och degraderas, medan andra fastnar tillsammans med CSN. Denna mångfald av utfall tyder på att subtila skillnader i hur individuella receptorer rör vid CSN kan avgöra om de skyddas eller elimineras när ett ortosteriskt molekylärt lim appliceras.
Vad detta innebär för framtida läkemedel
Huvudbudskapet för icke-specialister är att CSN5i-3 visar hur ett läkemedel kan vara både en plugg och ett lim på samma gång. Istället för att behöva binda sitt mål extremt hårt på egen hand lånar molekylen styrka från just det substrat den hjälper till att fånga, och uppnår hög verklig potens från blygsam grundaffinitet. Eftersom limeffekterna kan justeras för att känna igen särskilda substrat kan denna strategi, i princip, användas för att utforma läkemedel som blockerar skadliga enzymaktioner samtidigt som andra lämnas i fred, vilket minskar biverkningar. Författarna föreslår ”ortosteriska molekylära limhämmare” som en ny klass av föreningar som kan tillämpas på många enzymer involverade i att klippa eller modifiera proteiner, och öppnar en väg mot mer selektiv kontroll av cellens mest aktiva maskiner.
Citering: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Nyckelord: molekylärt lim, COP9-signalosom, proteinnedbrytning, enzymhämmare, läkemedelsupptäckt