Clear Sky Science · es
CSN5i-3 es un inhibidor adhesivo molecular ortostérico del complejo COP9 signalosome
Por qué importa un nuevo tipo de fármaco
Muchos medicamentos modernos actúan desactivando enzimas sobreactivas, pero con frecuencia afectan demasiados blancos y provocan efectos secundarios. Este estudio revela una forma sorprendente en que una pequeña molécula puede apagar con mucha más precisión una máquina de control celular clave, el COP9 signalosome. Al actuar tanto como un bloqueador convencional como una «adhesivo molecular», el compuesto CSN5i-3 apunta a una nueva estrategia para diseñar fármacos más seguros y selectivos.
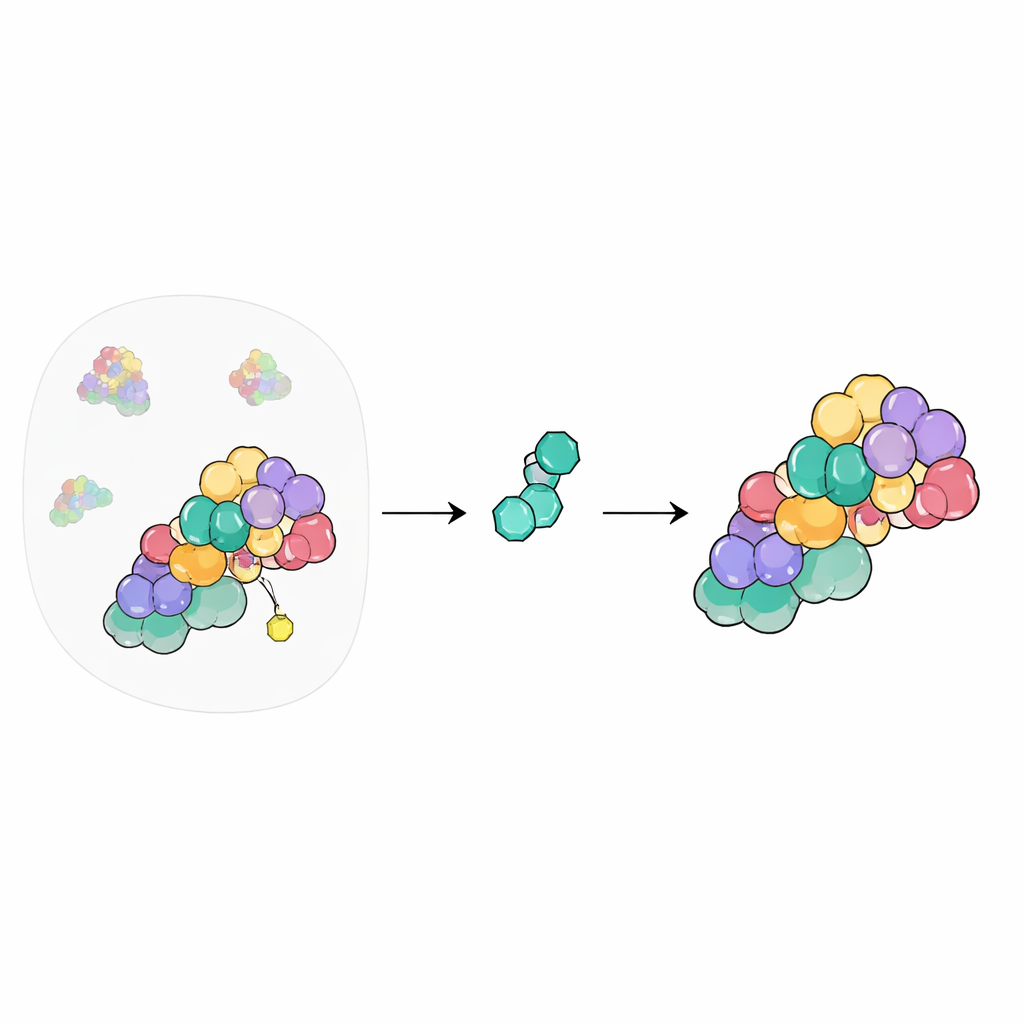
La central de reciclaje de la célula
En el interior de nuestras células, una enorme red de máquinas etiqueta proteínas no deseadas o dañadas para que puedan ser destruidas. En el centro de este sistema están las ligasas cullin–RING, andamiajes que reúnen las herramientas necesarias para marcar proteínas para su eliminación. Su actividad se enciende y apaga mediante la unión y eliminación de una pequeña proteína llamada NEDD8. El COP9 signalosome (CSN) actúa como el interruptor de apagado, recortando NEDD8 de los cullines para que el sistema pueda reiniciarse. Dado que este panel de control afecta a cientos de procesos celulares, los químicos han querido durante mucho tiempo controlar el CSN con fármacos, pero lograrlo de forma segura es un reto.
Una pequeña molécula con un giro importante
El compuesto CSN5i-3 fue diseñado para taponar el sitio activo de la subunidad cortadora del CSN, CSN5, como un corcho en una botella. En pruebas simples, se une a ese sitio solo de forma moderada, en el rango micromolar, lo que normalmente no bastaría para un fármaco potente. Sin embargo, en reacciones celulares CSN5i-3 apaga el CSN a niveles nanomolares—alrededor de mil veces más potente de lo que su afinidad sugeriría. Trabajos previos también sugirieron que se comporta como un inhibidor “incompetitivo”, prefiriendo unirse a la enzima solo cuando el sustrato ya está en su lugar, un patrón raramente observado en bloqueadores directos del sitio activo. Estas rarezas sugerían que ocurría algo más sutil.
Viendo el abrazo molecular
Para entenderlo, los autores usaron microscopía crioelectrónica de alta resolución para visualizar el CSN en varios estados: solo, con sus socios cullin modificados por NEDD8 y con CSN5i-3 presente o ausente. Primero capturaron un estado «pre‑corte» en el que la cola de NEDD8 y el punto de unión del cullin están bien posicionados en la ranura de CSN5, sostenidos por una cadena de contactos proteína‑proteína que se extiende desde NEDD8 a través del cullin y una proteína auxiliar llamada RBX hacia el resto del CSN. Esta estructura explica cómo el CSN reconoce sus objetivos a lo largo de muchos cullines distintos mientras mantiene la geometría adecuada para romper el enlace NEDD8–cullin.
Cómo la adhesión se mantiene sin cortar
Cuando se añade CSN5i-3, se encaja en la misma ranura donde se situaría el enlace NEDD8–cullin, por lo que sigue funcionando como un bloqueador clásico. Pero las imágenes revelan que la molécula hace más: un extremo se apoya contra la cola de NEDD8 mientras que el otro presiona la región próxima del cullin. En efecto, CSN5i-3 se convierte en un puente que refuerza los débiles contactos entre NEDD8 y CSN5. Mediciones biofísicas muestran que, en presencia del compuesto, NEDD8 libre de repente se une fuertemente al CSN y todo el complejo enzima‑sustrato se vuelve mucho más estable. Los autores denominan a este comportamiento «adhesivo molecular ortostérico» porque el fármaco se sitúa en el sitio activo normal (ortostérico) y, además, pega la enzima y el sustrato.
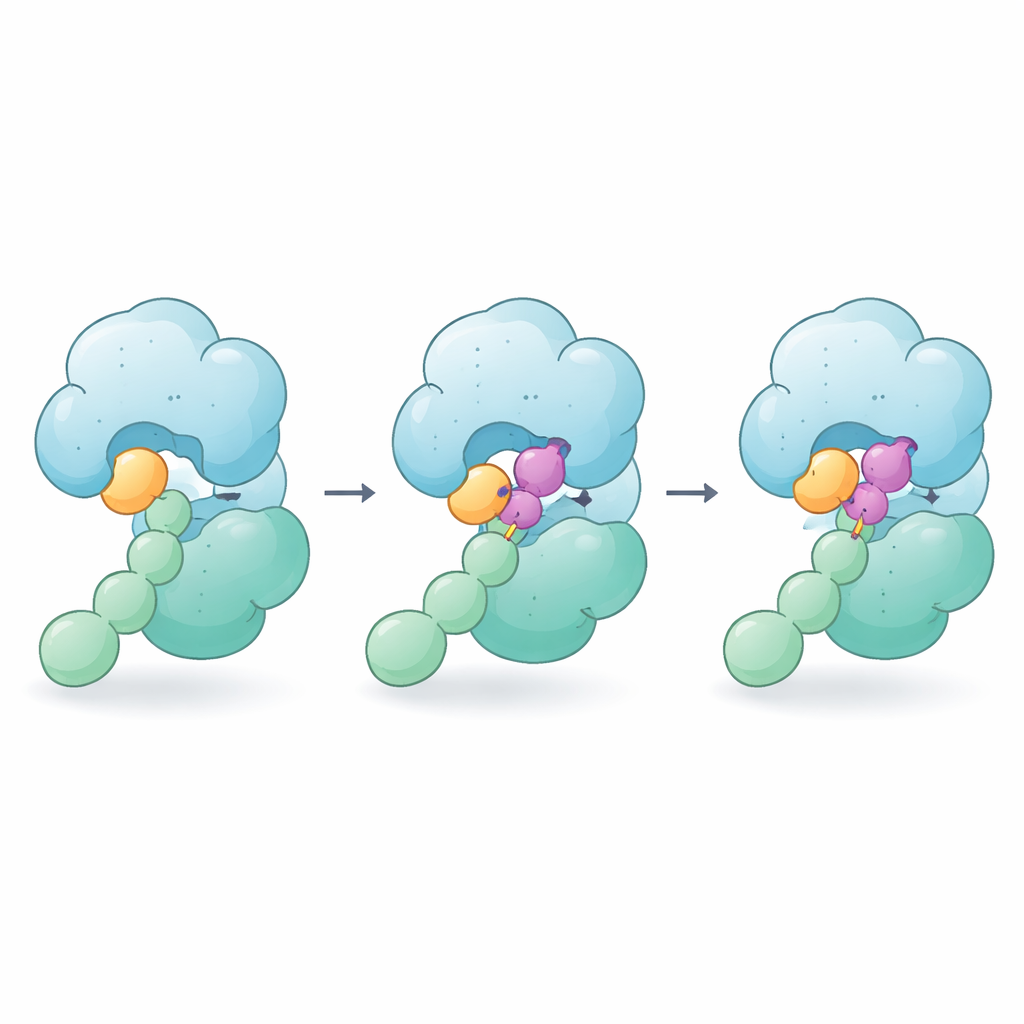
Efectos en cadena en toda la célula
Al fijar el CSN a sus socios decorados con NEDD8, CSN5i-3 cambia el tiempo que estos complejos duran en las células. Usando cross‑linking y espectrometría de masas, el equipo mapeó qué proteínas permanecen asociadas al CSN antes y después del tratamiento. Encontraron que los cullines y muchos de sus adaptadores se encuentran con mayor frecuencia unidos al CSN cuando el compuesto está presente, coherente con «atascos» de reacción causados por el efecto adhesivo. De forma llamativa, algunos receptores de sustrato se vuelven menos estables y son degradados, mientras que otros quedan atrapados junto al CSN. Esta diversidad de resultados sugiere que diferencias sutiles en cómo receptores individuales contactan al CSN pueden determinar si son protegidos o eliminados cuando se aplica un adhesivo molecular ortostérico.
Qué significa esto para futuros medicamentos
El mensaje clave para no especialistas es que CSN5i-3 muestra cómo un fármaco puede ser a la vez un tapón y un adhesivo. En lugar de necesitar unirse a su diana extremadamente fuerte por sí mismo, la molécula toma prestada la fuerza del propio sustrato que ayuda a atrapar, logrando una alta potencia en la realidad a partir de una afinidad básica modesta. Dado que los contactos adhesivos pueden ajustarse para reconocer sustratos particulares, este enfoque podría, en principio, usarse para diseñar medicamentos que bloqueen acciones enzimáticas dañinas mientras respetan otras, reduciendo efectos secundarios. Los autores proponen los «inhibidores adhesivos moleculares ortostéricos» como una nueva clase de compuestos que podrían aplicarse a muchas enzimas implicadas en el corte o modificación de proteínas, abriendo un camino hacia un control más selectivo de las máquinas más activas de la célula.
Cita: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Palabras clave: adhesivo molecular, COP9 signalosome, degradación de proteínas, inhibidores enzimáticos, descubrimiento de fármacos