Clear Sky Science · he
CSN5i-3 הוא מדכא דבק מולקולרי אורטוסטרי של ה-COP9 signalosome
למה סוג חדש של תרופה חשוב
תרופות רבות מודרניות פועלות על ידי כיבוי אנזימים פעילים יתר על המידה, אך לעיתים קרובות הן פוגעות ביותר מדי מטרות וגורמות לתופעות לוואי. במחקר זה מתגלה דרך מפתיעה במהלכה מולקולה קטנה יכולה לכבות בצורה מדויקת יותר מכונה בקרה סלולרית מרכזית — ה-COP9 signalosome. על ידי פעולה גם כחוסם קונבנציונלי וגם כ"דבק מולקולרי", התרכובת CSN5i-3 מצביעה על אסטרטגיה חדשה לעיצוב תרופות בטוחות ובעלות בחירה גבוהה יותר.
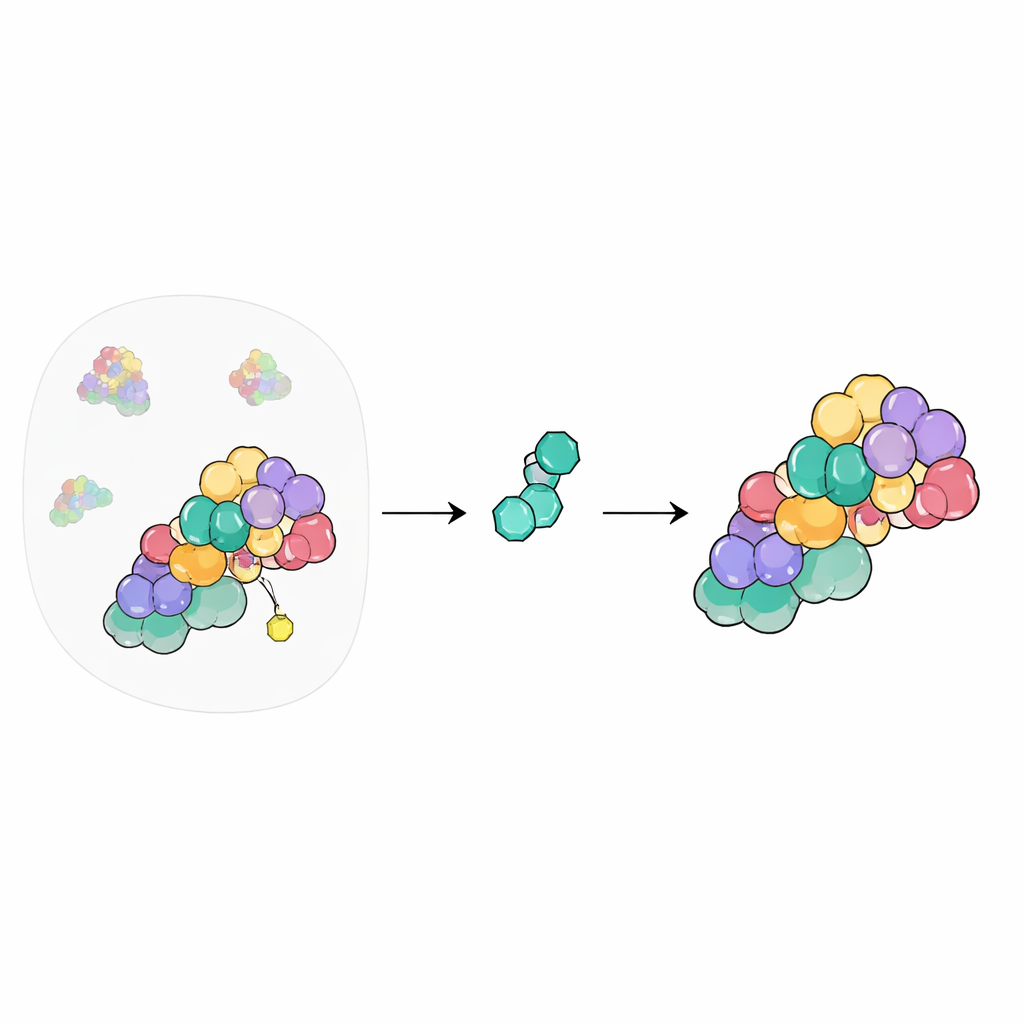
לוח המיתוג של המיחזור בתא
בתאים שלנו פועלת רשת עצומה של מכונות המסמנות חלבונים לא רצויים או פגומים כדי שיושמדו. במרכז המערכת עומדים cullin–RING ligases, שלדיים שמקבצים את הכלים הדרושים לסימון החלבונים. פעילותם נדלקת וכביתת על ידי חיבור והסרה של חלבון קטן הנקרא NEDD8. ה-COP9 signalosome (CSN) משמש כמפסיק — חותך את NEDD8 מה-cullins כדי לאפשר איפוס המערכת. מאחר שלוח המיתוג הזה נוגע במאות תהליכים תאיים, כימאים רצו זמן רב לשלוט ב-CSN בעזרת תרופות, אך לעשות זאת בבטחה הוא אתגרי.
מולקולה קטנה עם פיתול גדול
התרכובת CSN5i-3 עוצבה כדי להצרף לאתר הפעולה של תת-היחידה החותכת של ה-CSN, CSN5, כמו הפקק בבקבוק. בבדיקות פשוטות היא נקשרת לאתר זה ברמה מתונה בלבד, בסקאלת מיקרומולר, מה שלא היה בדרך כלל הופך אותה לתרופה חזקה. ובכל זאת, בתגובות תאיות CSN5i-3 מכבה את ה-CSN בריכוזים בננומולר — בערך אלף פעם חזק יותר ממה שאמינות ההיקשרות שלה הייתה מרמזת. עבודות קודמות רמזו גם שהיא מתנהגת כמעכב "לא תחרותי" — מעדיפה להיקשר לאנזים רק כשהסובסטרט כבר במקום — דפוס שנדיר לראות במעכבים הפועלים ישירות באתר הפעיל. הסטיות הללו הראו שמשהו עדין יותר מתרחש.
לראות את החיבוק המולקולרי
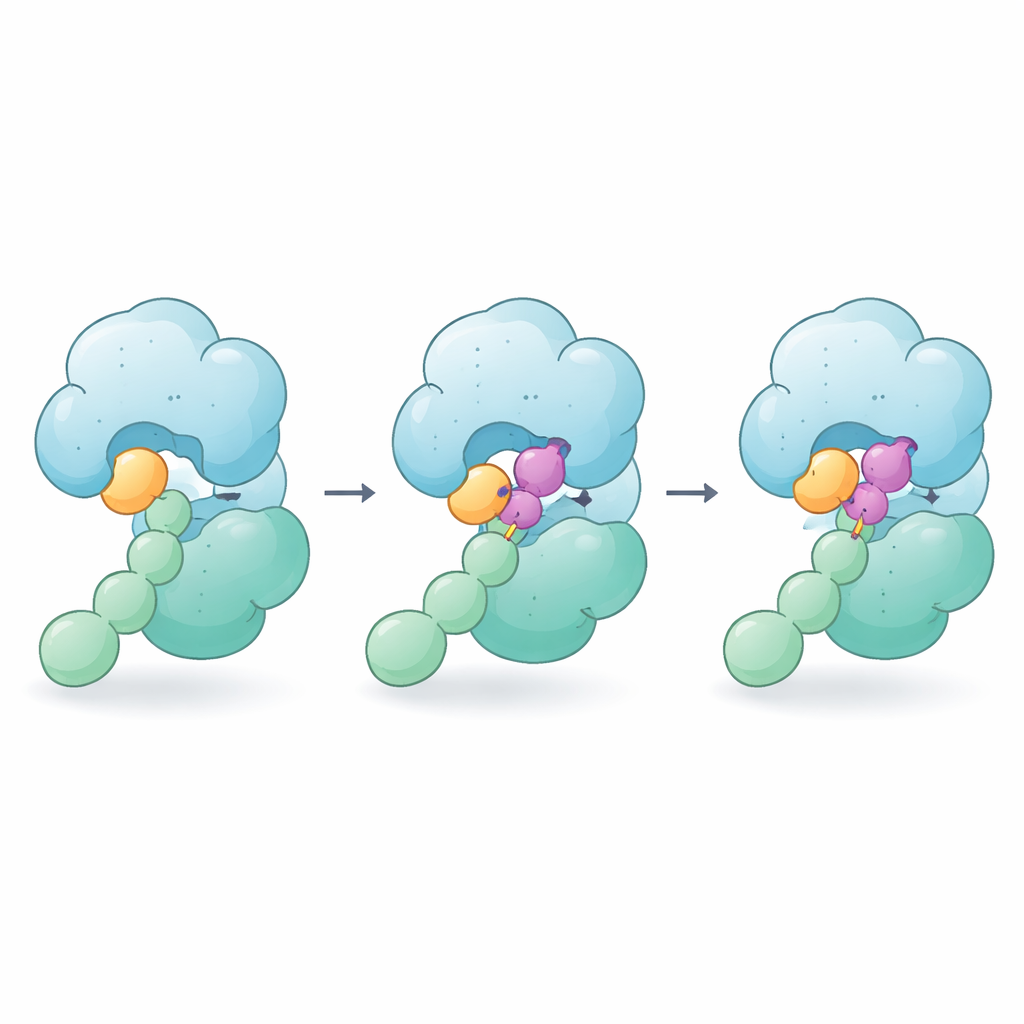
כדי להבין זאת, החוקרים השתמשו במיקרוסקופיה אלקטרונית קריוגנית ברזולוציה גבוהה כדי לדמיין את ה-CSN בכמה מצבים: לבדו, עם שותפיו ה-cullin המותאמים ב-NEDD8, וכש-CSN5i-3 נוכח או נעדר. הם תפסו תחילה מצב "לפני החיתוך" שבו זנב ה-NEDD8 ונקודת החיבור ל-cullin ממוקמים בנוחות בשקע של CSN5, מוחזקים במקום על ידי שרשרת של מגעי חלבון–חלבון שמתארכת מ-NEDD8 דרך ה-cullin וחלבון מסייע בשם RBX אל שאר ה-CSN. המבנה הזה מסביר כיצד ה-CSN מזהה את מטרותיו על פני מגוון cullins תוך שמירה על גיאומטריה מתאימה לשבירת הקשר בין NEDD8 ל-cullin.
איך הדבק מחזיק בלי לחתוך
כאשר מוסיפים CSN5i-3, הוא נכנס לשקע שבו היה אמור לשבת הקשר בין NEDD8 ל-cullin, ולכן הוא עדיין פועל כחוסם קלאסי. אך התמונות חושפות כי המולקולה עושה יותר: קצה אחד נצמד לזנב ה-NEDD8 בעוד הקצה האחר לוחץ על האזור הסמוך של ה-cullin. למעשה, CSN5i-3 הופך לגשר שמחזק את המגעים החלשים בין NEDD8 ל-CSN5. מדידות פיזיקו–כימיות מראות כי בנוכחות התרכובת, NEDD8 החופשי פתאום נקשר בחוזקה ל-CSN, וכל קומפלקס האנזים–סובסטרט נעשה יציב בהרבה. החוקרים קוראים להתנהגות זו "דבק מולקולרי אורטוסטרי" כי התרופה יושבת באתר הפעיל הרגיל (אורטוסטרי) ובו בזמן מדביקה יחדיו אנזים וסובסטרט.
אפקטים מתגלגלים ברחבי התא
על ידי נעילת ה-CSN על שותפיו המצופים ב-NEDD8, CSN5i-3 משנה כמה זמן קומפלקסים אלה נשארים בתאים. בעזרת חציית-קשרים ומסה ספקטרומטריה, הצוות מיפו אילו חלבונים נשארים משויכים ל-CSN לפני ואחרי הטיפול. הם מצאו ש-cullins ורבים מהמתאמים שלהם נמצאים בתדירות גבוהה יותר קשורים ל-CSN בנוכחות התרכובת, בהתאם ל"פקקי תנועה" בריאקציות שגורם אפקט הדבק. באופן מרשים, כמה קולטי סובסטרט נעשים פחות יציבים ומפורקים, בעוד אחרים נלכדים יחד עם ה-CSN. מגוון התוצאות הזה מציע שהבדלים עדינים באופן שבו קולטים בודדים נוגעים ב-CSN יכולים לקבוע האם הם מוגנים או מוסרים כאשר מוחל דבק מולקולרי אורטוסטרי.
מה משמעות הדבר לתרופות עתידיות
המסר המרכזי לקהל שאינו מומחה הוא ש-CSN5i-3 מראה כיצד תרופה יכולה להיות גם פקק וגם דבק בו-זמנית. במקום שתהיה חייבת להיקשר למטרה בחוזקה מוחלטת מעצמה, המולקולה שואבת כוח מהסובסטרט עצמו שהיא מסייעת ללכוד, ומשיגה עוצמה פרקטית גבוהה מתוך אפיניות בסיסית צנועה. כי ניתן לכוון את מגעי הדבק כדי לזהות סובסטרטים מסוימים, גישה זו יכולה, בעקרון, לשמש לעיצוב תרופות שחוסמות פעולות אנזימטיות מזיקות תוך שמירה על אחרות וכתוצאה להפחתת תופעות לוואי. המחברים מציעים את המונח "מעכבי דבק מולקולרי אורטוסטריים" כקטגוריה חדשה של תרכובות שיכולות להיות מיושמות על אנזימים רבים המעורבים בחיתוך או בשינוי חלבונים, ולפתוח נתיב לשליטה סלקטיבית יותר במכונות העמוסות ביותר של התא.
ציטוט: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
מילות מפתח: דבק מולקולרי, COP9 signalosome, פירוק חלבונים, מעכבי אנזימים, גילוי תרופות