Clear Sky Science · ar
CSN5i-3 هو مُثبِط لاصق جزيئي ارتوستيري لمجمع إشارة COP9
لماذا يهم نوع جديد من الأدوية
تعمل العديد من الأدوية الحديثة عن طريق إيقاف الإنزيمات المفرطة النشاط، لكنّها غالبًا ما تصيب أهدافًا كثيرة وتسبب آثارًا جانبية. تكشف هذه الدراسة عن طريقة مفاجئة لجزيء صغير لإيقاف آلة تنظيم خلوية رئيسية، مجمع إشارة COP9، بدقة أكبر بكثير. من خلال العمل كمثبط تقليدي ومثل "لاصق جزيئي" في الوقت نفسه، يشير المركب CSN5i-3 إلى استراتيجية جديدة لتصميم أدوية أكثر أمانًا وانتقائية.
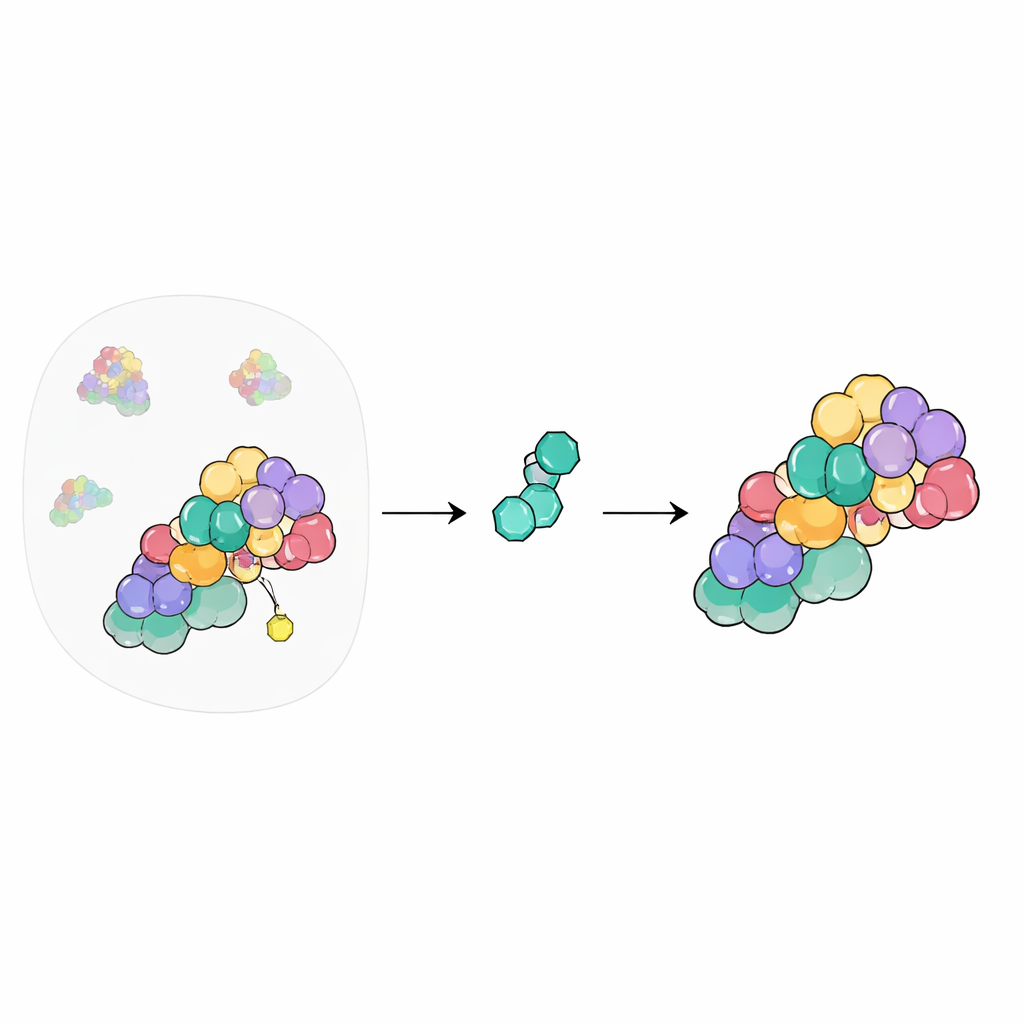
لوحة تحويل إعادة التدوير الخلوية
داخل خلايانا يوجد شبكة ضخمة من الآلات التي تُيَشِّر البروتينات غير المرغوب فيها أو التالفة حتى يمكن تدميرها. في مركز هذا النظام تقع لِيجازات cullin–RING، وهي هياكل تجميع تُقرِّب الأدوات اللازمة لوضع علامة على البروتينات للتخلص منها. يتم تشغيل نشاطها وإيقافه عن طريق إرفاق وإزالة بروتين صغير يُسمى NEDD8. يعمل مجمع إشارة COP9 (CSN) كمفتاح الإيقاف، حيث يزيل NEDD8 عن الـ cullins حتى يعود النظام لحالته الأولية. وبما أن هذه اللوحة تؤثر على مئات العمليات الخلوية، رغب الكيميائيون منذ زمن طويل في التحكم بـ CSN عبر أدوية، لكن تحقيق ذلك بأمان يمثل تحديًا.
جزيء صغير بحيلة كبيرة
صُمِّم المركب CSN5i-3 ليسد موقع العمل في الوحدة القاطعة لمجمع CSN، المكوّنة CSN5، مثل سدادة في زجاجة. في اختبارات بسيطة، يرتبط هذا المركب بالموقع فقط بطريقة متوسطة، في نطاق الميكرو مولار، وهو ما عادةً لا يجعل منه دواءً فعالًا. ومع ذلك، في التفاعلات الخلوية يوقف CSN5i-3 نشاط CSN عند مستويات نانومولارية — أي أقوى بحوالي ألف مرة مما توحي به قوة الارتباط وحدها. أشارت أعمال سابقة أيضًا إلى أنه يتصرف كمثبط "غير تنافسي"، مفضلاً الارتباط بالإنزيم فقط عندما يكون الركيزة موجودة بالفعل، وهو نمط نادر الظهور مع السدادات المباشرة لموقع الفاعلية. اقترحت هذه الشذوذات أن هناك آلية أكثر دقة تحدث.
رؤية العناق الجزيئي
لفهم ذلك، استخدم الباحثون المجهر الإلكتروني المبرد عالي الدقة لتصور CSN في حالات متعددة: وحده، مع شركائه من cullin المعدلين بـ NEDD8، ومع وجود CSN5i-3 أو غيابه. أولًا سجّلوا حالة "ما قبل القص" حيث ذيل NEDD8 ونقطة ارتباطه بالـ cullin موضوعة بإحكام في شقّ CSN5، محمولة في مكانها بسلسلة من تلامسات بروتين-لبروتين تمتد من NEDD8 عبر الـ cullin وبروتين مساعد يُدعى RBX إلى بقية CSN. يفسر هذا البناء كيف يتعرف CSN على أهدافه عبر العديد من الـ cullins مع الحفاظ على الترتيب الهندسي الصحيح لفصل رابط NEDD8–cullin.
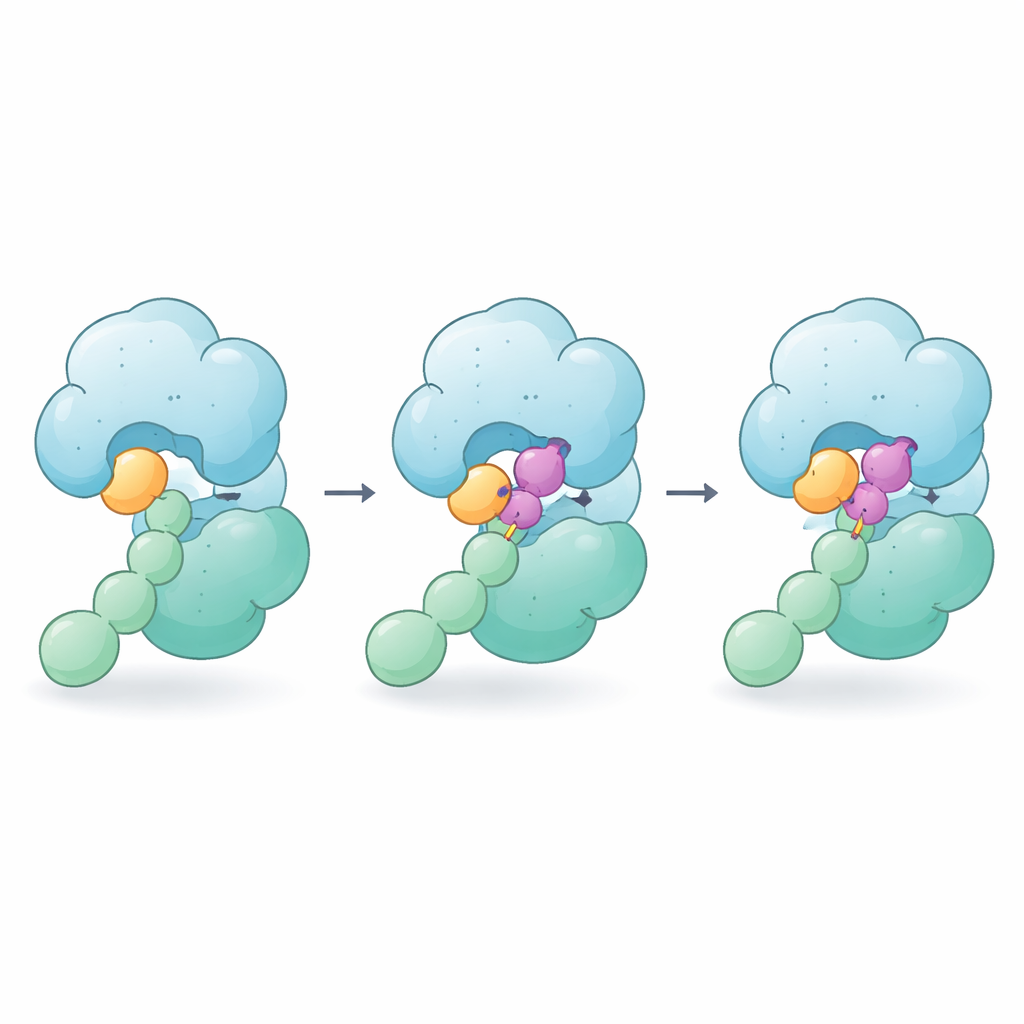
كيف يمسك اللاصق دون أن يقطع
عند إضافة CSN5i-3، يستقرّ في نفس الشق حيث تجلس رابطة NEDD8–cullin، لذا لا يزال يعمل كسدادة كلاسيكية. لكن الصور تكشف أن الجزيء يفعل أكثر من ذلك: طرف منه يستقر بجانب ذيل NEDD8 بينما يضغط الطرف الآخر على منطقة مجاورة في الـ cullin. فعليًا، يصبح CSN5i-3 جسرًا يقوّي التلامسات الضعيفة بين NEDD8 وCSN5. تُظهر القياسات البيوفيزيائية أنه، بوجود المركب، يرتبط NEDD8 الحر فجأة بقوة بـ CSN، ويصبح مركب الإنزيم–الركيزة كله أكثر استقرارًا بكثير. يسمي المؤلفون هذا السلوك "لاصقًا جزيئيًا ارتوستيريًا" لأن الدواء يجلس في موقع النشاط الطبيعي (ارتوستيري) وفي الوقت نفسه يلصق الإنزيم والركيزة معًا.
تأثيرات متسلسلة عبر الخلية
عن طريق تثبيت CSN على شركائه المزخرفين بـ NEDD8، يغيّر CSN5i-3 مدة بقاء هذه المجمّعات في الخلايا. باستخدام الربط المتقاطع والتحليل الطيفي الكتلي، رسم الفريق خريطة البروتينات التي تبقى مرتبطة بـ CSN قبل العلاج وبعده. وجدوا أن الـ cullins والعديد من موائماتها تُعوَّض أكثر ارتباطًا بـ CSN بوجود المركب، متسقًا مع ظاهرة "ازدحام المرور" التفاعلي الناجم عن أثر اللاصق. بشكل لافت، تصبح بعض مستقبلات الركائز أقل استقرارًا وتتحلل، بينما تُحبس أخرى مع CSN. تشير هذه التنوعات في النتائج إلى أن اختلافات دقيقة في كيفية تلامس المستقبلات الفردية مع CSN قد تحدد ما إذا كانت تُحمى أو تُقضى عندما يُطبَّق لاصق جزيئي ارتوستيري.
ما معنى ذلك للأدوية المستقبلية
الرسالة الأساسية لغير المتخصصين هي أن CSN5i-3 يبيّن كيف يمكن للدواء أن يكون سدادة ولاصقًا في الوقت نفسه. بدلًا من الحاجة إلى أن يرتبط الهدف بقوة كبيرة بمفرده، يستعير الجزيء القوة من الركيزة نفسها التي يساعد على احتجازها، محققًا فعالية عملية عالية انطلاقًا من ألفة أساسية متواضعة. وبما أن تلامسات اللاصق يمكن ضبطها للتعرّف على ركائز معينة، فقد يُستخدم هذا الأسلوب، من حيث المبدأ، لتصميم أدوية تحجب أعمال إنزيمية ضارة مع الحفاظ على الأخرى، مما يقلل الآثار الجانبية. يقترح المؤلفون فئة جديدة من المركبات اسمها "مثبطات لاصق جزيئي ارتوستيري" يمكن تطبيقها على العديد من الإنزيمات المشاركة في قطع أو تعديل البروتينات، فاتحةً طريقًا نحو تحكم أكثر انتقائية في أنشطتِها داخل الخلايا.
الاستشهاد: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
الكلمات المفتاحية: لاصق جزيئي, مجمع إشارة COP9, تحلل البروتين, مثبطات الإنزيم, اكتشاف الأدوية