Clear Sky Science · pl
CSN5i-3 jest ortosterycznym inhibitorem‑klejem molekularnym kompleksu COP9 signalosome
Dlaczego nowy rodzaj leku ma znaczenie
Wiele współczesnych leków działa przez wyłączanie nadaktywności enzymów, lecz często oddziałują zbyt szeroko i wywołują skutki uboczne. To badanie odsłania zaskakujący sposób, w jaki mała cząsteczka potrafi precyzyjnie wyłączyć kluczową komórkową maszynerię kontrolną — kompleks COP9 signalosome. Działając zarówno jak konwencjonalny bloker, jak i „klej molekularny”, związek CSN5i-3 wskazuje na nową strategię projektowania bezpieczniejszych, bardziej selektywnych leków.
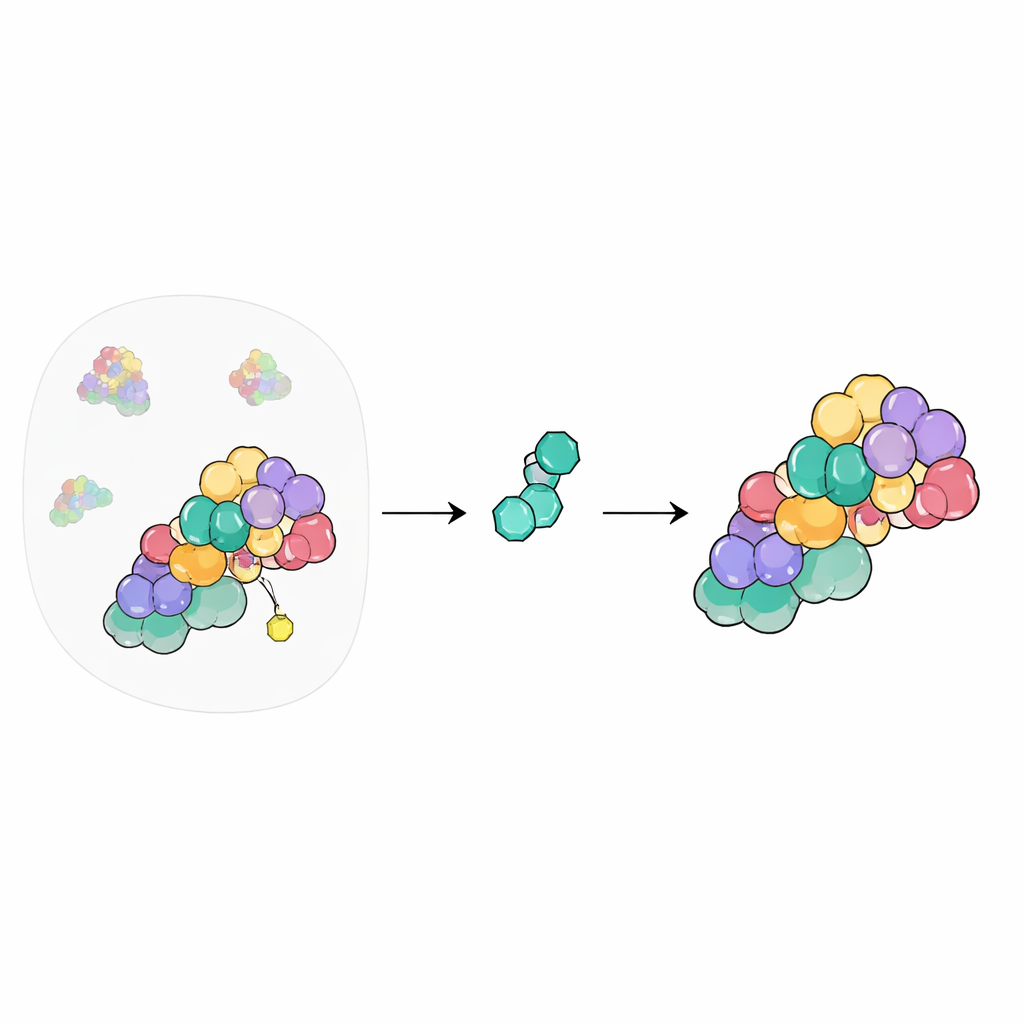
Centralna przełącznica recyklingu komórkowego
W naszych komórkach rozległa sieć maszyn oznacza niechciane lub uszkodzone białka, by mogły zostać zniszczone. W centrum tego systemu znajdują się ligazy typu cullin–RING — rusztowania łączące narzędzia służące do znakowania białek do usunięcia. Ich aktywność włączana i wyłączana jest przez przyłączanie i usuwanie małego białka nazwanego NEDD8. Kompleks COP9 signalosome (CSN) działa jako wyłącznik, odcinając NEDD8 od cullinów, by system mógł się zresetować. Ponieważ ta przełącznica wpływa na setki procesów komórkowych, chemicy od dawna chcą kontrolować CSN za pomocą leków, jednak zrobienie tego bezpiecznie jest wyzwaniem.
Mała cząsteczka z dużym zwrotem akcji
Związek CSN5i-3 zaprojektowano tak, by zatkać miejsce pracy tnącej podjednostki CSN, CSN5, niczym korek w butelce. W prostych testach wiąże się z tym miejscem umiarkowanie, w zakresie mikromolowym, co zwykle nie czyniłoby go silnym lekiem. Jednak w reakcjach komórkowych CSN5i-3 wyłącza CSN w stężeniach nanomolowych — około tysiąc razy silniej niż sugerowałaby jego siła wiązania. Wcześniejsze prace sugerowały też, że zachowuje się jak inhibitor „niekonkurencyjny”, preferując wiązanie z enzymem dopiero gdy substrat jest już obecny — schemat rzadko spotykany dla bezpośrednich blokerów aktywnego miejsca. Te dziwności wskazywały, że dzieje się coś subtelniejszego.
Oglądając molekularne objęcie
Aby to zrozumieć, autorzy użyli wysokorozdzielczej krioelektronowej mikroskopii, by zobrazować CSN w kilku stanach: samodzielnie, z jego cullinami zmodyfikowanymi NEDD8 i z obecnym lub nieobecnym CSN5i-3. Najpierw uchwycili stan „przed przecięciem”, w którym ogonek NEDD8 i punkt przyłączenia cullina są ciasno umieszczone w rowku CSN5, utrzymywane przez łańcuch kontaktów białko–białko rozciągający się od NEDD8 przez cullin i białko pomocnicze RBX do reszty CSN. Ta struktura wyjaśnia, jak CSN rozpoznaje swoje cele w różnych cullinach, zachowując odpowiednią geometrię do przerwania wiązania NEDD8–cullin.
Jak klej trzyma bez cięcia
Gdy dodano CSN5i-3, klinował się on w tym samym rowku, gdzie normalnie siedziałoby wiązanie NEDD8–cullin, więc nadal działa jako klasyczny bloker. Jednak obrazy ujawniają, że cząsteczka robi więcej: jeden koniec układa się przy ogonku NEDD8, podczas gdy drugi naciska na pobliski fragment cullina. W efekcie CSN5i-3 staje się mostem wzmacniającym słabe kontakty między NEDD8 a CSN5. Pomiary biofizyczne pokazują, że w obecności związku wolne NEDD8 nagle wiąże się ściśle z CSN, a cały kompleks enzym–substrat staje się znacznie stabilniejszy. Autorzy nazywają to zachowanie „ortosterycznym klejem molekularnym”, ponieważ lek zajmuje normalne miejsce aktywne (ortosteryczne), a jednocześnie sklejaj razem enzym i substrat.
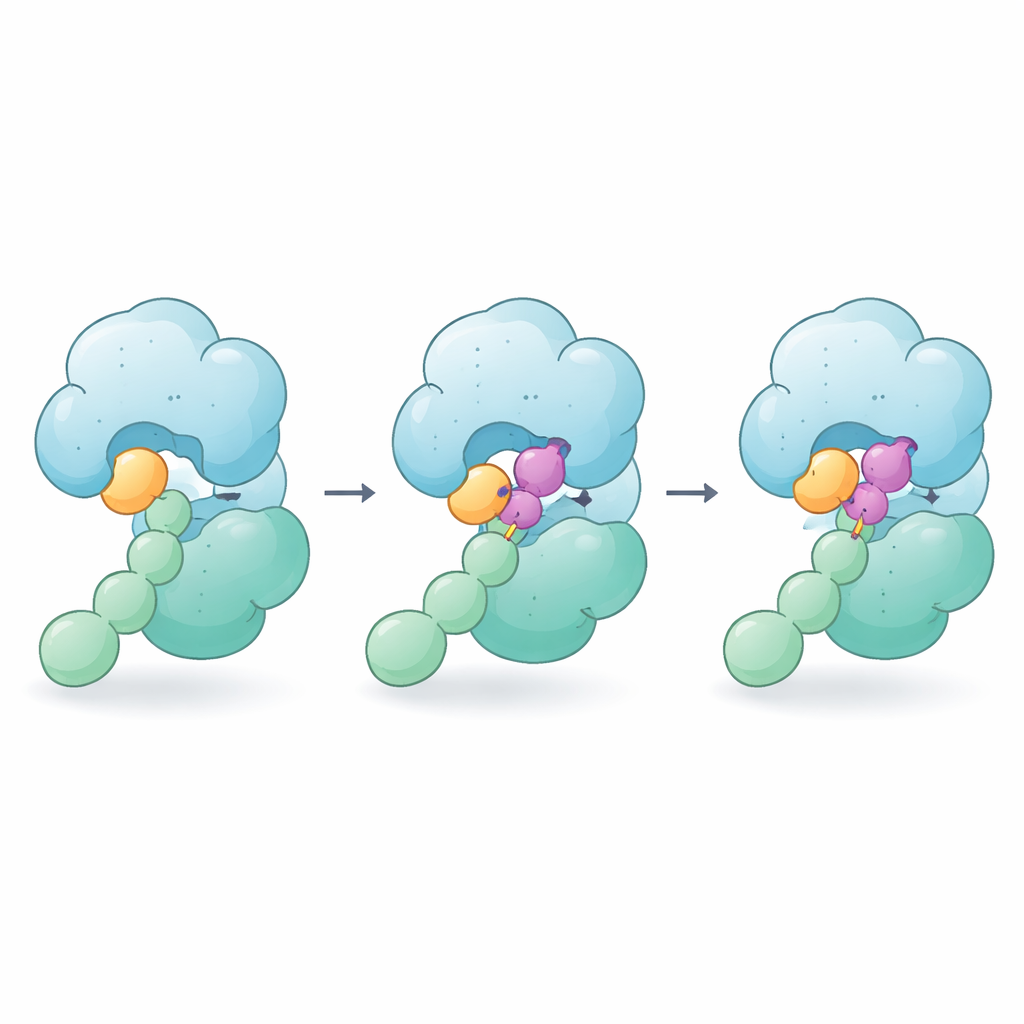
Fale efektów w całej komórce
Blokując CSN na jego partnerach ozdobionych NEDD8, CSN5i-3 zmienia czas, przez jaki te kompleksy utrzymują się w komórkach. Używając krzyżowania i spektrometrii mas, zespół odwzorował, które białka pozostają związane z CSN przed i po leczeniu. Stwierdzili, że culliny i wiele ich adaptorów częściej występuje związanych z CSN, gdy związek jest obecny, co odpowiada „korekty” w reakcji spowodowanej efektem kleju. Co znamienne, niektóre receptory substratów stają się mniej stabilne i są degradowane, podczas gdy inne zostają uwięzione razem z CSN. Ta różnorodność wyników sugeruje, że subtelne różnice w tym, jak poszczególne receptory stykają się z CSN, mogą decydować, czy są chronione, czy eliminowane po zastosowaniu ortosterycznego kleju molekularnego.
Co to oznacza dla przyszłych leków
Główne przesłanie dla osób niebędących specjalistami jest takie, że CSN5i-3 pokazuje, jak lek może być jednocześnie zatką i klejem. Zamiast wiązać swój cel ekstremalnie silnie samodzielnie, cząsteczka pożycza siłę od samego substratu, który pomaga uwięzić, osiągając wysoką praktyczną moc przy skromnym podstawowym powinowactwie. Ponieważ kontakty klejące można dostroić do rozpoznawania określonych substratów, podejście to mogłoby w zasadzie posłużyć do projektowania leków blokujących szkodliwe działania enzymów przy oszczędzaniu innych, zmniejszając skutki uboczne. Autorzy proponują „ortosteryczne inhibitory‑kleje molekularne” jako nową klasę związków, którą można zastosować wobec wielu enzymów uczestniczących w cięciu lub modyfikowaniu białek, otwierając drogę do bardziej selektywnej kontroli najważniejszych maszyn komórkowych.
Cytowanie: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Słowa kluczowe: klej molekularny, kompleks COP9 signalosome, degradacja białek, inhibitory enzymów, odkrywanie leków