Clear Sky Science · it
CSN5i-3 è un inibitore «collante molecolare» ortosterico del segnalosoma COP9
Perché conta un nuovo tipo di farmaco
Molti medicinali moderni agiscono spegnendo enzimi iperattivi, ma spesso colpiscono troppi bersagli e causano effetti collaterali. Questo studio rivela un modo sorprendente in cui una piccola molecola può disattivare con maggiore precisione una macchina di controllo cellulare chiave, il segnalosoma COP9. Agendo sia come un blocco convenzionale sia come un «collante molecolare», il composto CSN5i-3 indica una nuova strategia per progettare farmaci più sicuri e più selettivi.
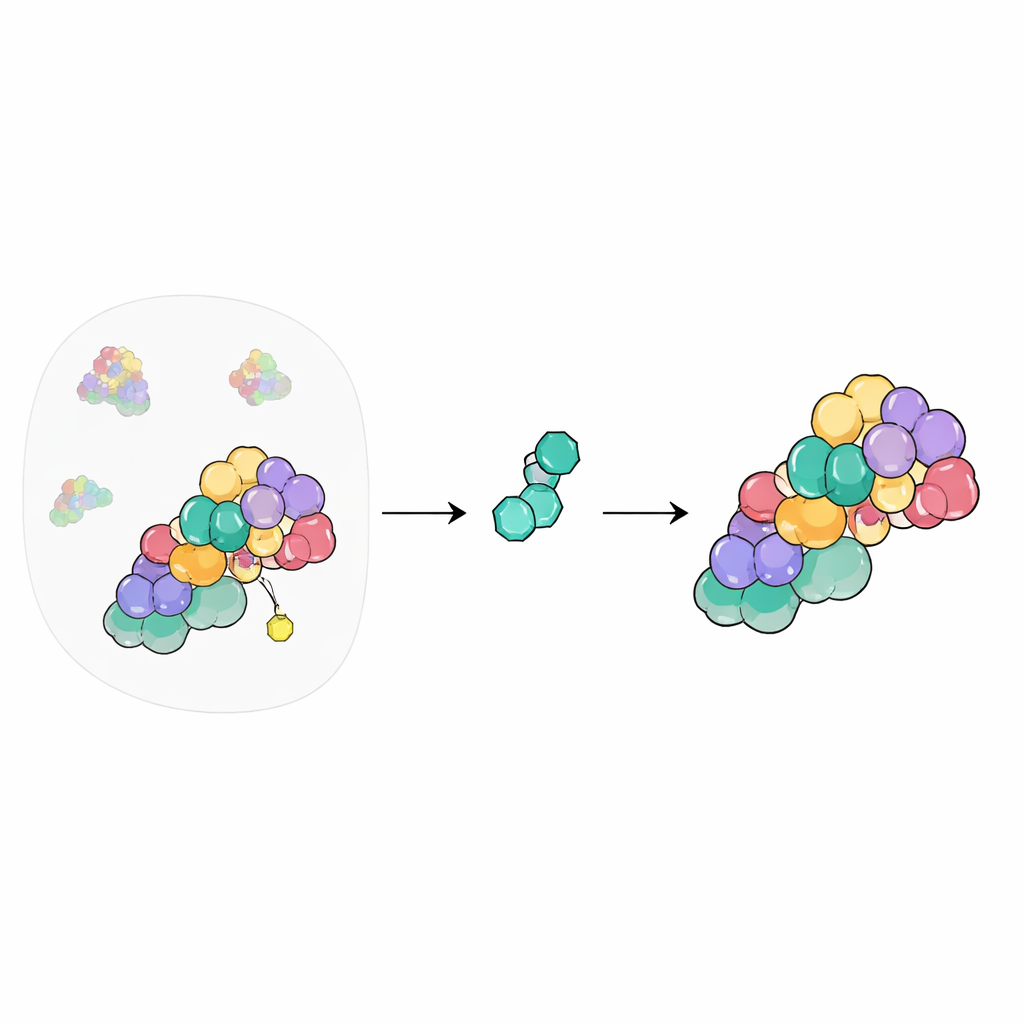
Il centralino del riciclo cellulare
All'interno delle nostre cellule, una vasta rete di macchine contrassegna le proteine indesiderate o danneggiate affinché vengano distrutte. Al centro di questo sistema ci sono le ligasi cullin–RING, impalcature che riuniscono gli strumenti necessari a marcare le proteine per lo smaltimento. La loro attività viene accesa e spenta tramite l'attacco e la rimozione di una piccola proteina chiamata NEDD8. Il segnalosoma COP9 (CSN) funge da interruttore di spegnimento, tagliando via NEDD8 dai cullin affinché il sistema possa resettarsi. Poiché questo centralino interessa centinaia di processi cellulari, i chimici hanno a lungo voluto controllare il CSN con farmaci, ma farlo in modo sicuro è una sfida.
Una piccola molecola con una grande sorpresa
Il composto CSN5i-3 è stato progettato per tappare il sito attivo della subunità tagliente del CSN, CSN5, come un tappo in una bottiglia. In test semplici si lega a questo sito solo in modo moderato, nell'intervallo micromolare, il che normalmente non lo renderebbe un farmaco potente. Eppure nelle reazioni cellulari CSN5i-3 spegne il CSN a livelli nanomolari—circa mille volte più forte di quanto suggerirebbe la sua forza di legame. Lavori precedenti avevano inoltre suggerito che si comporta come un inibitore «non competitivo» che preferisce legarsi all'enzima solo quando il substrato è già presente, uno schema raramente osservato per inibitori diretti del sito attivo. Queste stranezze indicavano che stava succedendo qualcosa di più sottile.
Osservare l’abbraccio molecolare
Per capire, gli autori hanno usato microscopia crioelettronica ad alta risoluzione per visualizzare il CSN in vari stati: da solo, con i suoi partner cullin modificati da NEDD8, e con CSN5i-3 presente o assente. Hanno prima catturato uno stato «pre‑taglio» in cui la coda di NEDD8 e il punto di attacco sul cullin sono posizionati saldamente nella scanalatura di CSN5, tenuti in posizione da una catena di contatti proteina–proteina che si estende da NEDD8 attraverso il cullin e una proteina ausiliaria chiamata RBX fino al resto del CSN. Questa struttura spiega come il CSN riconosce i suoi bersagli attraverso molti diversi cullin pur mantenendo la geometria giusta per rompere il legame NEDD8–cullin.
Come il collante tiene senza tagliare
Quando si aggiunge CSN5i-3, esso si incastra nella stessa scanalatura dove si porrebbe il legame NEDD8–cullin, funzionando quindi anche come un blocco classico. Ma le immagini rivelano che la molecola fa di più: un'estremità si adagia contro la coda di NEDD8 mentre l'altra preme sulla regione vicina del cullin. In pratica, CSN5i-3 diventa un ponte che rafforza i deboli contatti tra NEDD8 e CSN5. Misurazioni biofisiche mostrano che, in presenza del composto, NEDD8 libero si lega improvvisamente in modo stretto al CSN e l'intero complesso enzima–substrato diventa molto più stabile. Gli autori chiamano questo comportamento «collante molecolare ortosterico» perché il farmaco occupa il sito attivo normale (ortosterico) pur incollando insieme enzima e substrato.
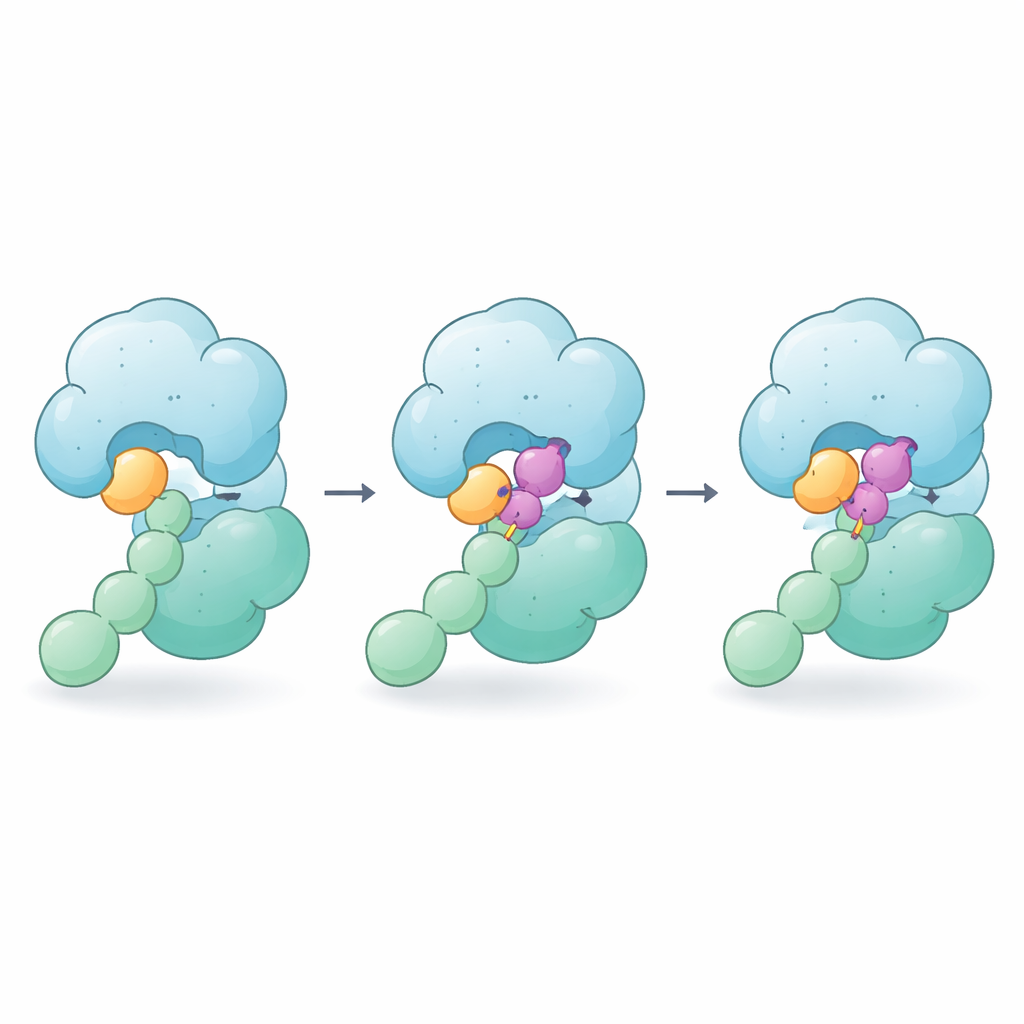
Effetti a catena nella cellula
Bloccando il CSN sui suoi partner decorati da NEDD8, CSN5i-3 modifica la durata di permanenza di questi complessi nelle cellule. Usando cross-linking e spettrometria di massa, il gruppo ha mappato quali proteine restano associate al CSN prima e dopo il trattamento. Hanno riscontrato che i cullin e molti dei loro adattatori si trovano più spesso legati al CSN in presenza del composto, coerente con un «ingorgo» delle reazioni causato dall'effetto collante. In modo impressionante, alcuni recettori di substrato diventano meno stabili e vengono degradati, mentre altri rimangono intrappolati insieme al CSN. Questa diversità di esiti suggerisce che sottili differenze nel modo in cui singoli recettori toccano il CSN possono determinare se vengono protetti o eliminati quando si applica un collante molecolare ortosterico.
Cosa significa per i medicinali futuri
Il messaggio principale per i non specialisti è che CSN5i-3 mostra come un farmaco possa essere allo stesso tempo un tappo e un collante. Invece di dover legare il bersaglio in modo estremamente forte da solo, la molecola prende in prestito forza dal substrato che aiuta a intrappolare, raggiungendo un'elevata potenza reale a partire da un'affinità di base modesta. Poiché i contatti del collante possono essere modulati per riconoscere substrati particolari, questo approccio potrebbe, in principio, essere impiegato per progettare farmaci che bloccano azioni enzimatiche dannose risparmiando altre, riducendo gli effetti collaterali. Gli autori propongono gli «inibitori collanti molecolari ortosterici» come una nuova classe di composti applicabile a molti enzimi coinvolti nel taglio o nella modifica delle proteine, aprendo la strada a un controllo più selettivo delle macchine cellulari più impegnate.
Citazione: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Parole chiave: collante molecolare, segnalosoma COP9, degradazione delle proteine, inibitori enzimatici, scoperta di farmaci