Clear Sky Science · fr
CSN5i-3 est un inhibiteur « glue » moléculaire orthostérique du signalosome COP9
Pourquoi un nouveau type de médicament importe
De nombreux médicaments modernes agissent en désactivant des enzymes hyperactives, mais ils ciblent souvent trop de protéines et provoquent des effets secondaires. Cette étude révèle une manière surprenante pour une petite molécule d’ouvrir la voie à l’arrêt d’une machine cellulaire de contrôle essentielle, le signalosome COP9, avec beaucoup plus de précision. En faisant à la fois office de bloqueur conventionnel et de « glue moléculaire », le composé CSN5i-3 indique une nouvelle stratégie pour concevoir des médicaments plus sûrs et plus sélectifs.
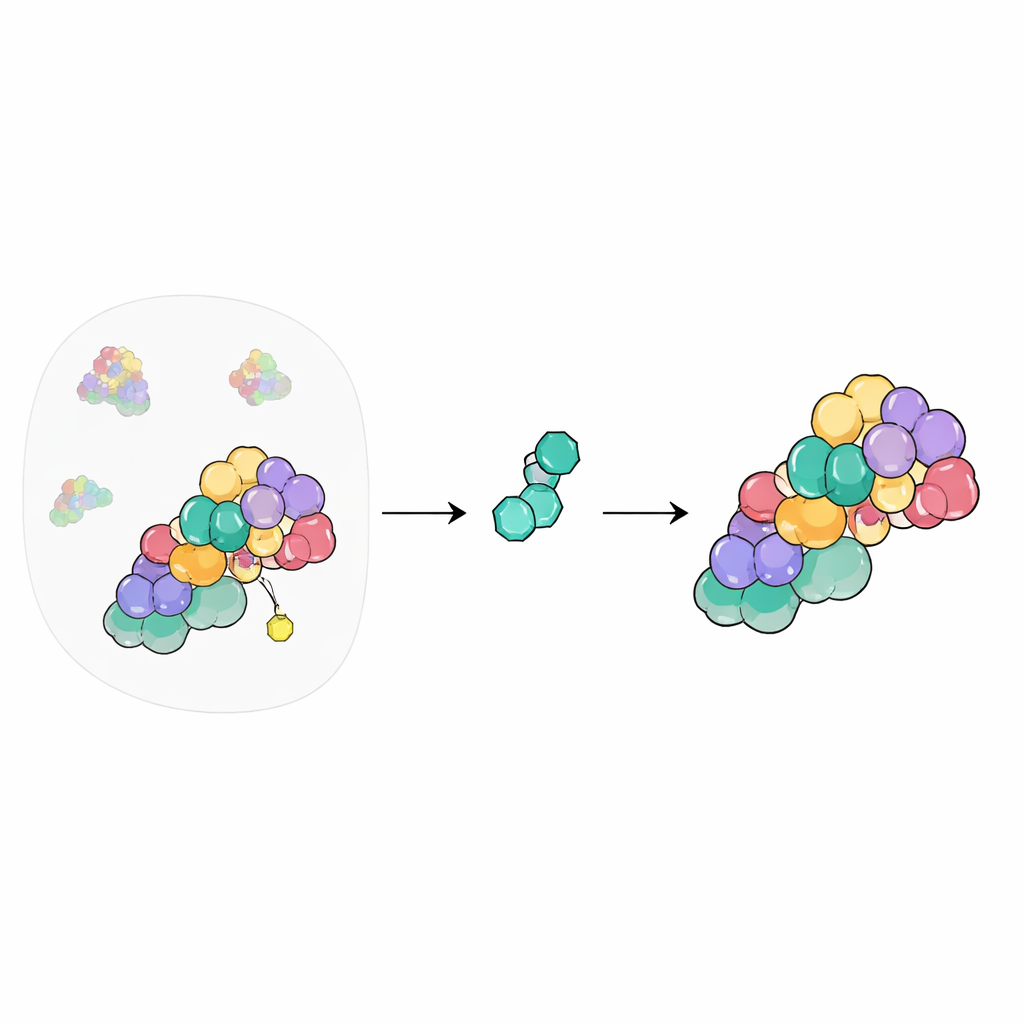
Le central téléphonique du recyclage cellulaire
À l’intérieur de nos cellules, un vaste réseau de machines étiquette les protéines indésirables ou endommagées afin qu’elles puissent être détruites. Au centre de ce système se trouvent les ligases cullin–RING, des échafaudages qui rassemblent les outils nécessaires pour marquer les protéines destinées à l’élimination. Leur activité est activée et désactivée par l’attachement et le retrait d’une petite protéine appelée NEDD8. Le signalosome COP9 (CSN) agit comme l’interrupteur d’arrêt, en coupant NEDD8 des cullines pour permettre au système de se réinitialiser. Parce que cet interrupteur affecte des centaines de processus cellulaires, les chimistes cherchent depuis longtemps à contrôler le CSN par des médicaments, mais y parvenir en toute sécurité reste difficile.
Une petite molécule avec un grand tour
Le composé CSN5i-3 a été conçu pour boucher le site actif de la sous-unité coupante du CSN, CSN5, comme un bouchon dans une bouteille. Dans des tests simples, il se lie à ce site avec une affinité seulement modérée, dans la gamme micromolaire, ce qui ne rendrait normalement pas un médicament très puissant. Pourtant, dans des réactions cellulaires CSN5i-3 éteint le CSN à des niveaux nanomolaires — environ mille fois plus fort que n’en suggérerait sa force de liaison. Des travaux antérieurs laissaient aussi entendre qu’il se comporte comme un inhibiteur « non compétitif », préférant se lier à l’enzyme seulement quand le substrat est déjà en place, un schéma rarement observé pour des bloqueurs directs du site actif. Ces étrangetés suggéraient qu’un mécanisme plus subtil était en jeu.
Voir l’étreinte moléculaire
Pour comprendre cela, les auteurs ont utilisé la cryo‑microscopie électronique à haute résolution pour visualiser le CSN dans plusieurs états : seul, avec ses partenaires cullines modifiés par NEDD8, et avec ou sans CSN5i-3. Ils ont d’abord capturé un état « pré‑coupe » dans lequel la queue de NEDD8 et le point d’attache sur la culline sont fermement positionnés dans la rainure de CSN5, maintenus en place par une chaîne de contacts protéine–protéine qui s’étend de NEDD8 à travers la culline et une protéine auxiliaire nommée RBX jusqu’au reste du CSN. Cette structure explique comment le CSN reconnaît ses cibles parmi de nombreuses cullines tout en gardant la géométrie correcte pour rompre la liaison NEDD8–culline.
Comment la glue maintient sans couper
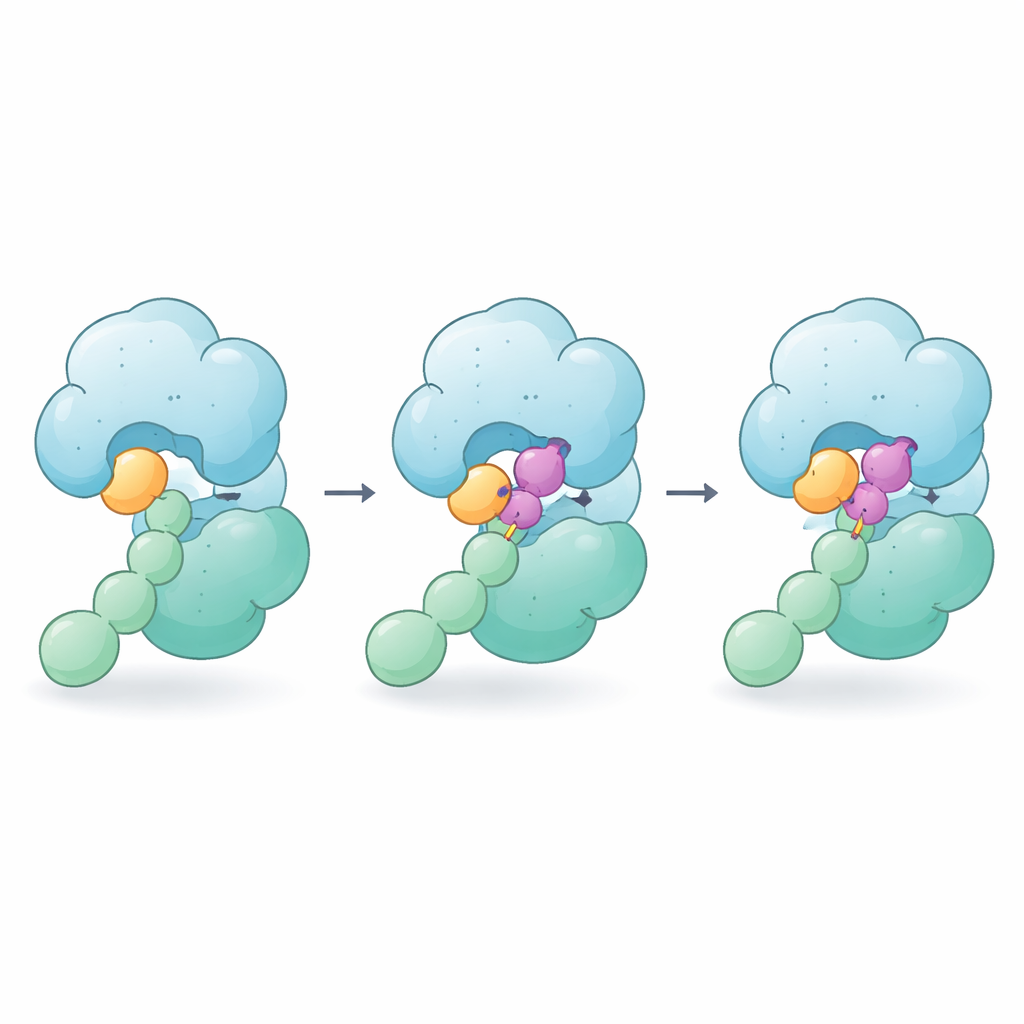
Lorsque CSN5i-3 est ajouté, il se cale dans la même rainure où se placerait la liaison NEDD8–culline, agissant donc comme un bloqueur classique. Mais les images révèlent que la molécule fait davantage : une extrémité se loge contre la queue de NEDD8 tandis que l’autre appuie sur la région voisine de la culline. En pratique, CSN5i-3 devient un pont qui renforce les contacts faibles entre NEDD8 et CSN5. Des mesures biophysiques montrent qu’en présence du composé, NEDD8 libre se lie soudainement fortement au CSN, et l’ensemble enzyme–substrat devient beaucoup plus stable. Les auteurs qualifient ce comportement de « glue moléculaire orthostérique » parce que le médicament se place dans le site actif normal (orthostérique) tout en collant enzyme et substrat.
Effets en cascade dans la cellule
En verrouillant le CSN sur ses partenaires décorés par NEDD8, CSN5i-3 modifie la durée de vie de ces complexes dans les cellules. À l’aide de réactifs de réticulation et de spectrométrie de masse, l’équipe a cartographié quelles protéines restent associées au CSN avant et après traitement. Ils ont constaté que les cullines et beaucoup de leurs adaptateurs sont plus souvent trouvés liés au CSN en présence du composé, cohérent avec des « embouteillages » réactionnels causés par l’effet glue. De façon frappante, certains récepteurs de substrat deviennent moins stables et sont dégradés, tandis que d’autres se retrouvent piégés avec le CSN. Cette diversité de résultats suggère que de subtiles différences dans la manière dont des récepteurs individuels contactent le CSN peuvent déterminer s’ils sont protégés ou éliminés lorsqu’une glue moléculaire orthostérique est appliquée.
Ce que cela signifie pour les médicaments futurs
Le message clé pour les non‑spécialistes est que CSN5i-3 montre comment un médicament peut être à la fois un bouchon et une glue en même temps. Au lieu de devoir se lier extrêmement fortement à sa cible par lui‑même, la molécule emprunte de la force au substrat même qu’elle aide à piéger, atteignant une grande puissance en conditions réelles à partir d’une affinité de base modeste. Parce que les contacts de glue peuvent être ajustés pour reconnaître des substrats particuliers, cette approche pourrait, en principe, être utilisée pour concevoir des médicaments qui bloquent les actions nuisibles d’enzymes tout en épargnant d’autres, réduisant ainsi les effets secondaires. Les auteurs proposent les « inhibiteurs glue moléculaires orthostériques » comme une nouvelle classe de composés applicable à de nombreuses enzymes impliquées dans la coupure ou la modification des protéines, ouvrant une voie vers un contrôle plus sélectif des machines cellulaires les plus actives.
Citation: Shi, H., Wang, X., Yu, C. et al. CSN5i-3 is an orthosteric molecular glue inhibitor of COP9 signalosome. Nature 652, 1375–1383 (2026). https://doi.org/10.1038/s41586-026-10129-y
Mots-clés: glue moléculaire, signalosome COP9, dégradation des protéines, inhibiteurs d’enzymes, découverte de médicaments