Clear Sky Science · tr
Amino asit bileşimi, peptid sentezi sırasında agregasyonu belirler
Neden küçük zincirler büyük ilaçlar için önem taşır
Günümüzün birçok modern ilacı, peptit adı verilen kısa amino asit zincirleridir. Kimyagerler bu zincirleri küçük boncuklar üzerinde, birer yapı taşı ekleyerek inşa edebilirler; ancak süreç genellikle büyüyen zincirler birbirine yapışıp kümelendiğinde aksar. Bu çalışma, bu kümelenmeyi esas olarak kontrol edenin yapı taşlarının kesin sırası değil, her türden kaç tane bulunduğunun toplamda nasıl dağıldığı olduğunu gösteriyor. Makine öğrenimi ve hedefe yönelik deneyler kullanarak, yazarlar hangi amino asitlerin kümelenmeyi kuvvetle teşvik ettiğini veya engellediğini ortaya koyuyor ve zorlu sentezlenebilir peptitleri çok daha verimli yapmak için bu bilgiyi nasıl kullanacağınızı gösteriyor.
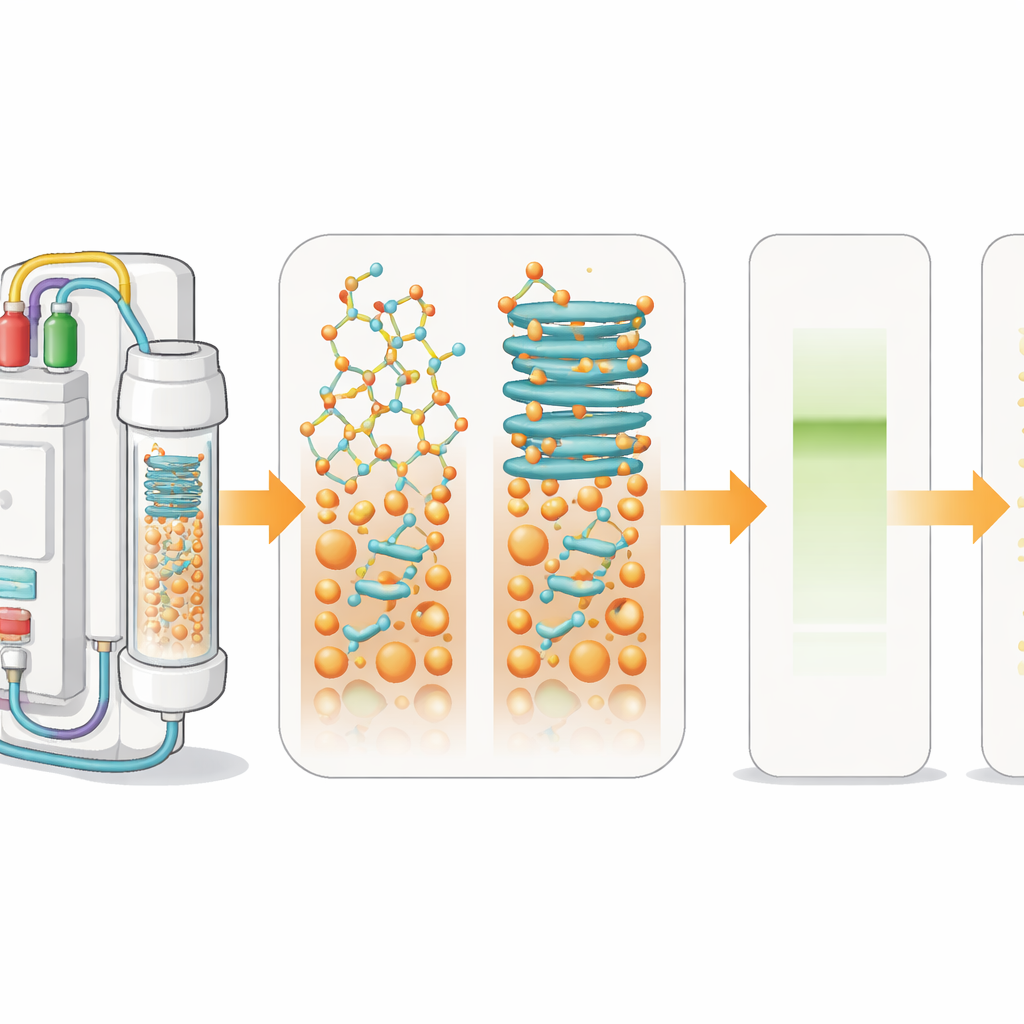
Peptit ilaçları nasıl birleştirilir
Laboratuvarda peptit yapmak için kimyagerler katı faz peptit sentezi adı verilen bir yöntem kullanır. İlk amino asit çözünmeyen bir boncuğa bağlanır ve ardından ek amino asitler, bir bileziğe boncuk takar gibi döngüler halinde eklenir. Her adımda koruyucu bir grup çıkarılır ve yeni bir birim bağlanır. Yerleşik bir ışık detektörü, koruyucu gruplar çıkarıldığında üretilen sinyallerin büyüklüğünü ve şeklini ölçerek bu adımları gerçek zamanlı izler. Boncuklardaki büyüyen zincirler birbirine yapışıp yaprak benzeri yapılar oluşturduğunda, sinyaller genişler. Bu “agregasyon” reaksiyonları yavaşlatır ve tek bir temiz peptit yerine hatalı ürün karışımlarına yol açar.
Binlerce sentezi verinin konuşmasına bırakmak
Araştırmacılar, otomatik akış tabanlı peptit sentezlerinin iki büyük veri kümesini birleştirerek toplamda 500’den fazla benzersiz diziyi ele aldılar. Her sentezdeki her adım için eklenen amino asit ve ışık tabanlı sinyallerden çıkarılan nicel bir agregasyon ölçüsü vardı. Ardından, amino asit dizilerini metin gibi okuyan modern dil benzeri modellerden klasik istatistiksel modellere ve bir sentezi bir olay dizisi olarak ele alan zaman serisi yöntemlerine kadar geniş bir makine öğrenimi yelpazesi uygulayarak basit bir evet–hayır sorusunu yanıtladılar: verilen peptit test edilen koşullar altında agregasyon gösterir mi?
Sıradanlıktan bileşime şaşırtıcı kayma
Tüm bu yöntemlerde, amino asit sırasının ne kadar zekice kodlandığına bakılmaksızın, tahmin doğruluğu benzer mütevazı seviyelerde dolaştı. Bu, kritik bir testi gündeme getirdi. Takım, her peptidin amino asit sırasını rastgele karıştırdı ancak her türün toplam sayısını aynı tuttu. Eğer kesin sıra kritik olsaydı, performans çökmeliydi. Çökmedi: modeller karıştırılmış dizilerde de aynı performansı gösterdi. Her peptidi, yalnızca her amino asidin fraksiyonunu kaydeden 20 sayılık bir “bileşim vektörüne” indirgediklerinde bile doğruluk benzer kaldı. Bunu deneysel olarak doğrulamak için yazarlar, dörtü agregasyon gösteren ve dördü göstermeyen olmak üzere sekiz bilinen peptidi alıp her birinin beş karıştırılmış versiyonunu sentezlediler. Çoğu karıştırılmış varyant orijinalleri gibi davrandı: agregasyon gösteren diziler hâlâ kümelendi ve kümelenmeyenler büyük ölçüde çözünür kaldı; ayrıca zincir boyunca benzer konumlarda kümelenmeye başlama eğilimindeydiler.
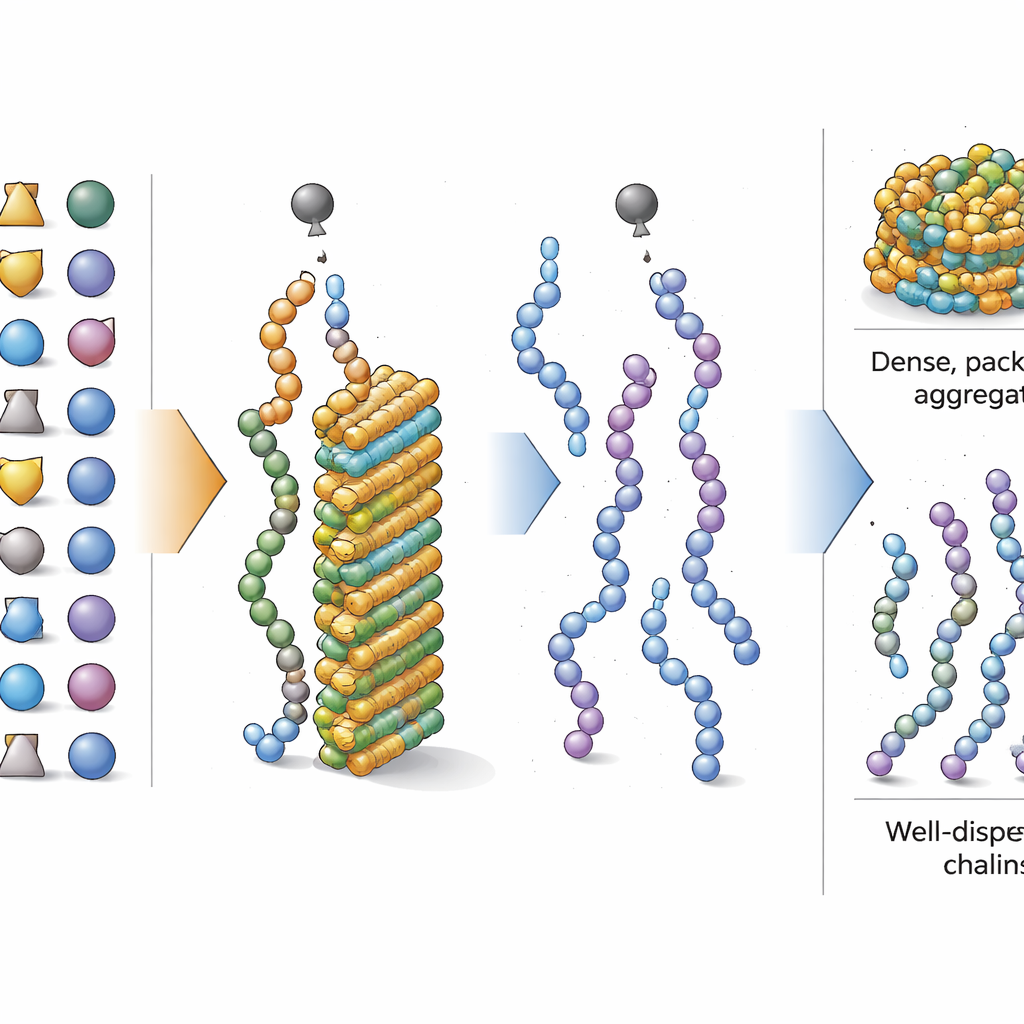
Amino asitler arasında iyi ve kötü aktörler
Bütün dikkat bileşime kaydığında, araştırmacılar sentez sırasında bir peptidi kümelenmeye veya kümelenmekten uzaklaştırmaya en çok hangi amino asitlerin ittiğini sordular. Yorumlanabilir bir makine öğrenimi aracı kullanarak, her amino asitin fraksiyonunun artmasının modelin tahminini ne kadar değiştirdiğini puanladılar. İzole yan zincirlere sahip basit, yağlı yapı taşlarının—örneğin izolösin ve valin ile yaygın kullanılan korumalı formları olan serin ve treonin—yüksek miktarlarda bulunduğunda agregasyonu kuvvetle teşvik ettiğini buldular. Buna karşılık, daha hacimli veya daha karmaşık yan gruplara sahip amino asitler, örneğin korumalı formlarıyla fenilalanin, tirozin, aspartik asit ve arjinin, agregasyonu azaltma eğilimindeydi. Glisin–serin ve lösin–lösin gibi bazı kısa iki amino asitli desenler de ek kümelenme eğilimleri gösterdi, ancak genel amino asit türlerinin dengesi baskın faktör olarak kaldı.
İçgörüleri daha iyi sentez tariflerine dönüştürmek
Bu “kümeleyen” ve “küme çözendir” amino asit haritasıyla ekip, bir sentez çalıştırılmadan önce pratik düzeltmeler önerebilen bir model topluluğu (ensemble) oluşturdu. Önerilen bir peptit için program, agregasyon olasılığını tahmin eder ve zincirin sabitlenmiş uca yakın bölgelerinde sorunlu amino asitlerin en çok katkıda bulunduğu pozisyonları belirler. Ardından, bu pozisyonları geçici olarak agregasyonu bozan ancak son deproteksiyon adımından sonra istenen amino asitlere geri dönen psödoproline gibi özel versiyonlarla değiştirmeyi önerir. Bu stratejiyi iki özellikle sorunlu peptit fragmanında test eden araştırmacılar, model tarafından seçilen pozisyonlara birkaç böyle ikame uyguladılar. Sonuç, kaba saflıkta dramatik bir artış oldu—ürün karışımının yaklaşık beşte birinden üçte üçüne çıkma—modelin hangi pozisyonların daha çok yardımcı olacağını sıralamasıyla uyumlu şekilde.
Bu, gelecekteki peptit ilaçları için ne anlama geliyor
Uzman olmayan biri için temel mesaj şudur: bu sentez koşulları altında peptit kümelenmesi hassas bir kilit-anahtar deseninden ziyade bir toplu tarif sorunu gibi davranır: “yağlı” ve “hacimli” bileşenlerin oranları, bunların kesin sıralarından daha önemlidir. Bunu tanıyarak ve nicelendirerek yazarlar hem uzun süredir süregelen sentez başarısızlıklarını açıklayabildi hem de bunlardan kaçınmak için basit, veri odaklı bir yol sundu. Çalışmaları, makine öğreniminin kimyasal süreçlerde gizli kuralları nasıl ortaya çıkarabileceğini ve bunları doğrudan tasarım araçlarına dönüştürebileceğini göstererek, peptit fikirlerinden güvenilir, ölçeklenebilir ilaçlara giden yolu hızlandırır.
Atıf: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Anahtar kelimeler: peptid sentezi, amino asit bileşimi, agregasyon, makine öğrenimi, katı faz kimyası