Clear Sky Science · ru
Состав аминокислот определяет агрегацию при синтезе пептидов
Почему крошечные цепочки важны для крупных лекарств
Многие современные лекарства представляют собой короткие цепочки аминокислот — пептиды. Химики собирают эти цепочки по одному звену на крошечных шариках, но процесс часто задерживается, потому что растущие цепочки слипаются друг с другом. В этом исследовании показано, что основным фактором слипания является не точный порядок звеньев, а общее количество каждого типа аминокислот. С помощью методов машинного обучения и целевых экспериментов авторы выявили, какие аминокислоты сильнее всего вызывают или предотвращают слипание, и показали, как использовать эти знания для более эффективного синтеза труднодоступных пептидов.
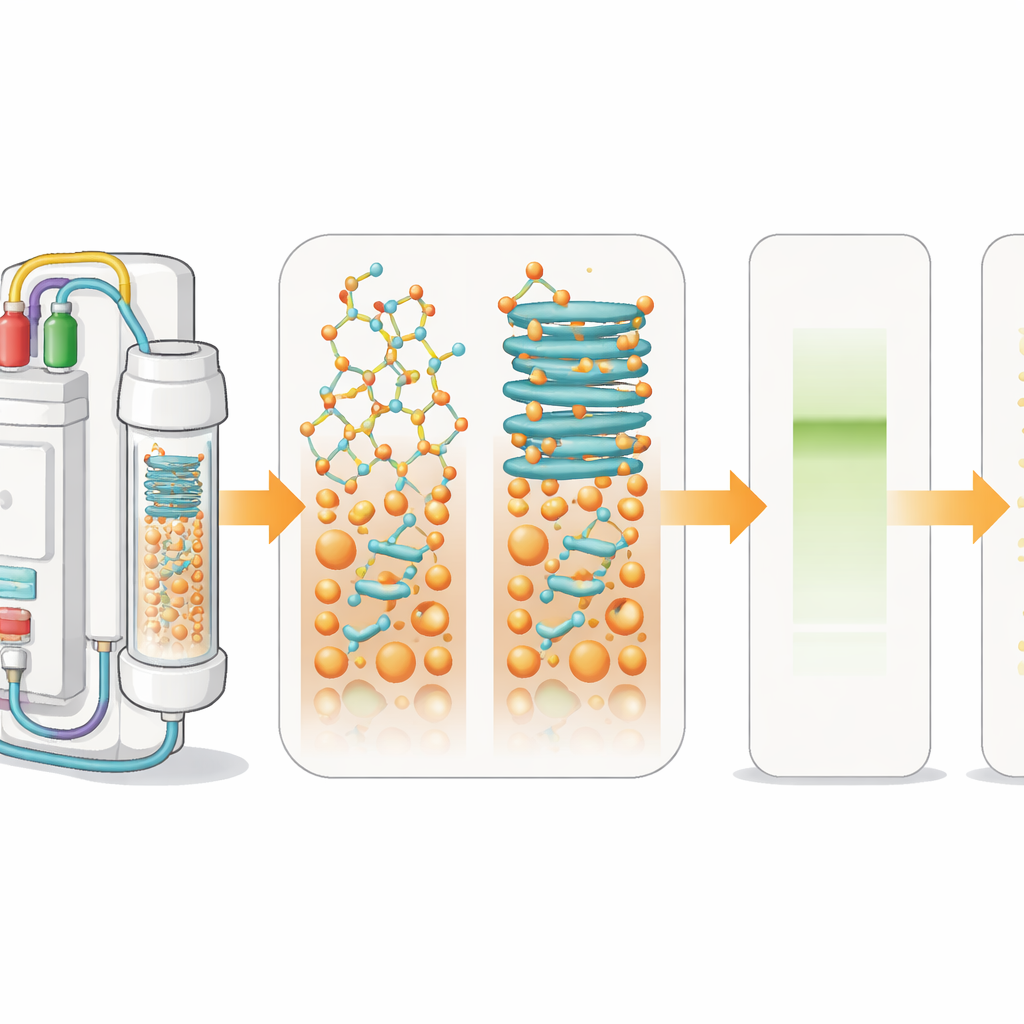
Как сшивают пептидные лекарства
В лаборатории пептиды синтезируют методом синтеза пептидов в твердой фазе. Первая аминокислота прикрепляется к нерастворимому шарику, затем другие аминокислоты добавляются по циклам, как если бы нанизывали бусины на браслет. На каждом шаге снимается защитная группа и присоединяется новый фрагмент. Встроенный световой датчик отслеживает эти шаги в реальном времени, измеряя форму и величину сигналов, возникающих при удалении защитных групп. Когда растущие цепочки на шариках начинают слипаться и складываться в листоподобные структуры, сигналы расширяются. Такая «агрегация» замедляет реакции и приводит к смеси бракованных продуктов вместо одного чистого пептида.
Дать данным высказать мнение о тысячах синтезов
Исследователи объединили два больших набора данных автоматизированных потоковых синтезов пептидов, в сумме более 500 уникальных последовательностей. Для каждого шага в каждом синтезе у них был и добавляемый аминокислотный фрагмент, и количественная мера степени агрегации, извлечённая из световых сигналов. Затем они применили широкий набор методов машинного обучения — от современных моделей в стиле обработки языка, читающих строки аминокислот как текст, до классических статистических моделей и методов временных рядов, рассматривающих синтез как последовательность событий — чтобы ответить на простой вопрос да/нет: аггрегирует ли данный пептид при протестированных условиях?
Неожиданный сдвиг от порядка к ингредиентам
Во всех этих методах точность прогнозов была примерно на одном умеренном уровне, независимо от того, насколько изящно кодировался порядок аминокислот. Это подтолкнуло к ключевому тесту. Команда случайным образом перемешала порядок аминокислот в каждой последовательности, сохранив при этом общие количества каждого типа. Если бы точный порядок был критичен, производительность моделей должна была бы сильно упасть. Этого не произошло: модели работали так же хорошо на перемешанных последовательностях. Даже когда каждую последовательность свели к 20-числовому «вектору состава», фиксирующему долю каждой аминокислоты, точность оставалась аналогичной. Чтобы подтвердить это экспериментально, авторы взяли восемь известных пептидов — четыре аггрегирующих и четыре неаггрегирующих — и синтезировали по пять перемешанных версий каждого. Большинство перемешанных вариантов вели себя как оригиналы: аггрегирующие последовательности по-прежнему агрегировали, неаггрегирующие оставались в основном растворимыми, причём агрегация обычно начиналась в похожих позициях вдоль цепочки.
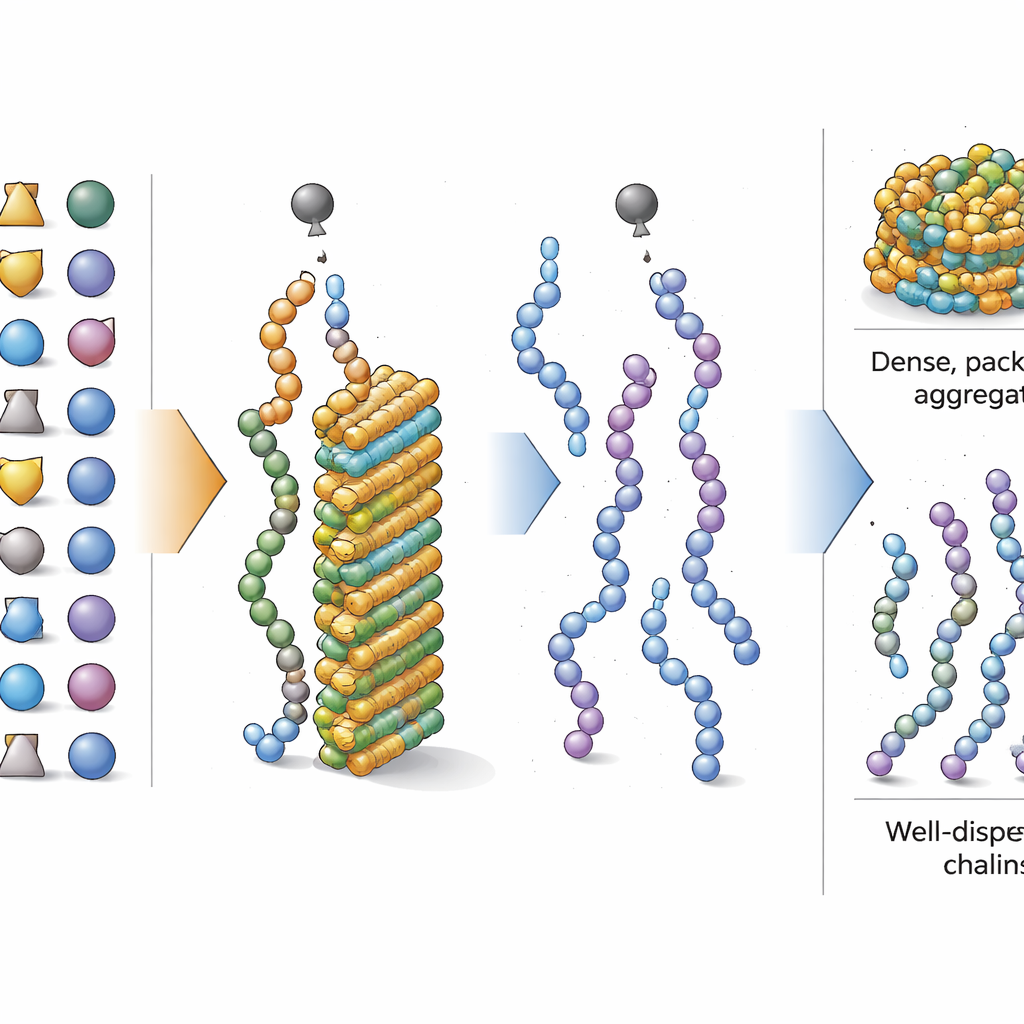
Хорошие и плохие «игроки» среди аминокислот
Сфокусировавшись на общем составе, исследователи выяснили, какие аминокислоты сильнее всего склоняют пептид к агрегации или от неё во время синтеза. С помощью интерпретируемого инструмента машинного обучения они оценили, как увеличение доли каждой аминокислоты влияет на прогноз модели. Оказалось, что строительные блоки с простыми «маслянистыми» боковыми цепями — такие как изолейцин и валин, а также обычно используемые защищённые формы серина и треонина — при высокой концентрации сильно способствуют агрегации. Напротив, аминокислоты с более объёмными или сложными боковыми группами, включая защищённые формы фенилаланина, тирозина, аспарагиновой кислоты и аргинина, склоняли к уменьшению агрегации. Некоторые короткие двухаминокислотные мотивы, например глицин–серин и лейцин–лейцин, также проявляли дополнительную склонность к слипанию, но доминирующим фактором оставался общий баланс типов аминокислот.
Превращение выводов в лучшие рецепты синтеза
Вооружившись картой «склеивающих» и «разъединяющих» аминокислот, команда создала ансамбль моделей, который может предложить практические исправления до запуска синтеза. Для предлагаемого пептида программа предсказывает вероятность агрегации и указывает позиции ближе к закреплённому концу цепочки, где проблемные аминокислоты вносят наибольший вклад. Затем она рекомендует заменять их специальными вариантами, например псевдопролиновыми строительными блоками, которые временно нарушают агрегацию, но возвращаются к желаемым аминокислотам после финального шага снятия защитных групп. Испытания этой стратегии на двух известных проблемных фрагментах показали: введение небольшого числа таких замен в выбранных моделью позициях резко повысило грубую чистоту — примерно с одной пятой до около трёх четвертей продуктовой смеси — в соответствии с ранжированием модели по наиболее полезным позициям.
Что это значит для будущих пептидных лекарств
Для неспециалиста основной вывод таков: при этих условиях синтетическая агрегация пептидов ведёт себя скорее как задача с рецептами объёма, а не как тонкий замок и ключ — важнее пропорции «маслянистых» и «объёмных» ингредиентов, чем их точный порядок. Осознав и количественно охарактеризовав это, авторы смогли объяснить давние неудачи синтеза и предложить простой, основанный на данных способ их избежать. Их работа демонстрирует, как машинное обучение может выявлять скрытые правила в химических процессах и превращать их в понятные инструменты проектирования, что в конечном счёте ускоряет путь от идеи пептида до надёжных, масштабируемых лекарств.
Цитирование: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Ключевые слова: синтез пептидов, состав аминокислот, агрегация, машинное обучение, химия твердой фазы