Clear Sky Science · pl
Skład aminokwasowy napędza agregację podczas syntezy peptydów
Dlaczego krótkie łańcuchy mają znaczenie dla wielkich leków
Wiele nowoczesnych leków to krótkie łańcuchy aminokwasów zwane peptydami. Chemicy budują te łańcuchy, doklejając kolejne ogniwa na małych kulkach, lecz proces często zatrzymuje się, ponieważ rosnące łańcuchy zaczynają się ze sobą sklejać. Badanie to pokazuje, że głównym czynnikiem kontrolującym to sklejanie nie jest dokładna kolejność ogniw, lecz ogólna liczba każdego typu aminokwasu. Dzięki uczeniu maszynowemu i ukierunkowanym eksperymentom autorzy ujawniają, które aminokwasy najsilniej sprzyjają lub przeciwdziałają sklejaniu oraz jak wykorzystać tę wiedzę, by dużo efektywniej wytwarzać peptydy trudne do syntezy.
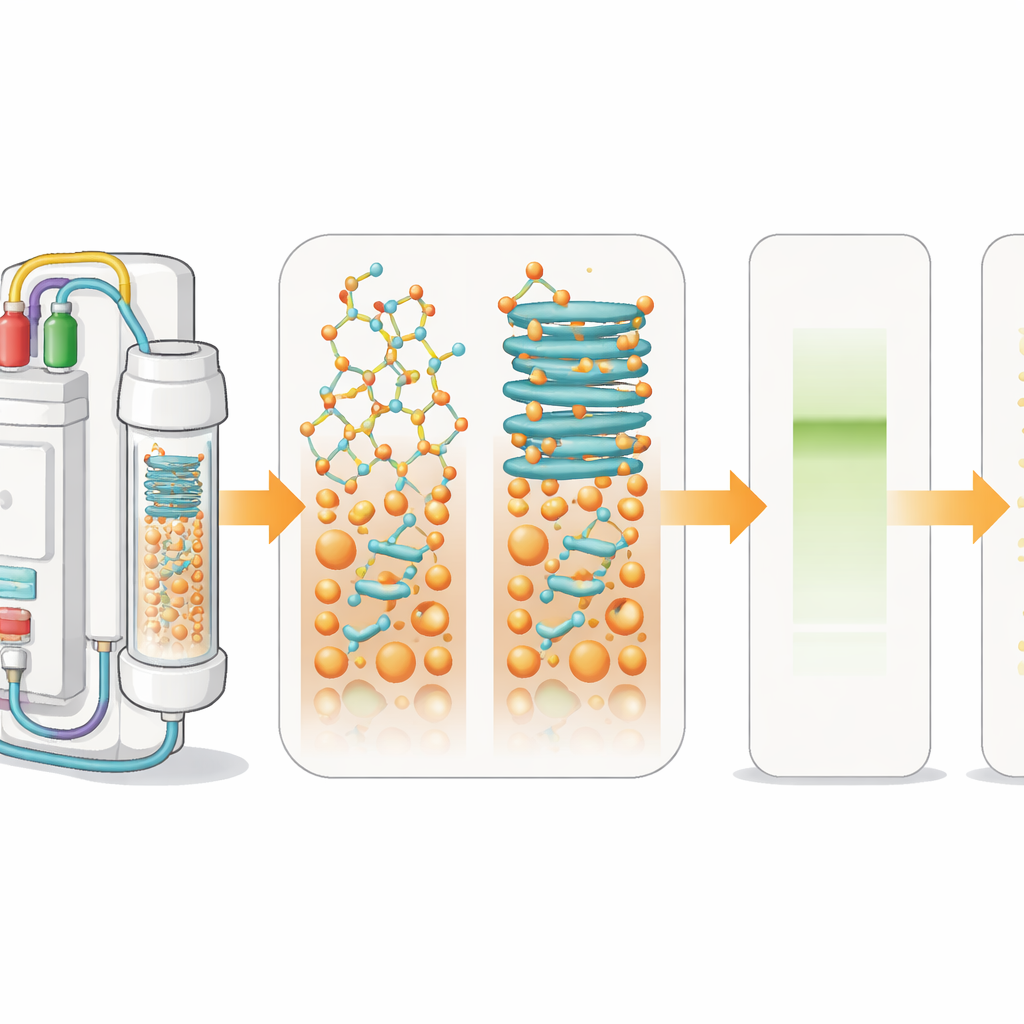
Jak składa się leki peptydowe
Aby w laboratorium wytwarzać peptydy, chemicy stosują metodę zwaną syntezą peptydów w fazie stałej. Pierwszy aminokwas jest przyłączany do nierozpuszczalnej kulki, po czym kolejne aminokwasy dodawane są w cyklach, jak nawlekanie koralików na bransoletkę. W każdym kroku usuwa się grupę ochronną i przyłącza nową jednostkę. Wbudowany czujnik świetlny śledzi te etapy w czasie rzeczywistym, mierząc wielkość i kształt sygnałów powstających przy usuwaniu grup ochronnych. Gdy rosnące łańcuchy na kulkach zaczynają przylegać do siebie i składać się w struktury przypominające arkusze, sygnały się poszerzają. Taka „agregacja” spowalnia reakcje i prowadzi do mieszanin wadliwych produktów zamiast jednego czystego peptydu.
Pozwolić danym przemówić za tysiące syntez
Naukowcy połączyli dwie duże bazy danych automatycznych syntez peptydów w przepływie, obejmujące łącznie ponad 500 unikatowych sekwencji. Dla każdego kroku w każdej syntezie mieli zarówno informację o dodawanym aminokwasie, jak i ilościowy wskaźnik stopnia agregacji wyekstrahowany z sygnałów świetlnych. Zastosowali następnie szerokie spektrum metod uczenia maszynowego — od nowoczesnych modeli w stylu językowym, które czytają ciągi aminokwasów jak tekst, po klasyczne modele statystyczne i metody szeregów czasowych traktujące syntezę jako sekwencję zdarzeń — by odpowiedzieć na proste pytanie tak–nie: czy dany peptyd agreguje w testowanych warunkach?
Niespodziewane przesunięcie od kolejności ku składnikom
We wszystkich tych metodach dokładność predykcji utrzymywała się na podobnym, umiarkowanym poziomie, niezależnie od tego, jak sprytnie zapisywano kolejność aminokwasów. To skłoniło zespół do kluczowego testu. Losowo przetasowali kolejność aminokwasów w każdej sekwencji, zachowując jednak ogólne liczby każdego typu. Gdyby precyzyjna kolejność była decydująca, wydajność modeli powinna była się zawalić. Nie stało się tak: modele radziły sobie równie dobrze na przetasowanych sekwencjach. Nawet gdy każdy peptyd sprowadzono do 20-wymiarowego „wektora składu”, który po prostu zapisywał ułamek każdego aminokwasu, dokładność pozostała zbliżona. Aby potwierdzić to eksperymentalnie, autorzy wzięli osiem znanych peptydów — cztery, które agregują, i cztery, które tego nie robią — i zsyntetyzowali pięć przetasowanych wersji każdego. Większość wariantów zachowywała się podobnie do oryginałów: sekwencje agregujące nadal agregowały, a nieagregujące przeważnie pozostawały rozpuszczalne, przy czym zaczynały agregować w podobnych miejscach wzdłuż łańcucha.
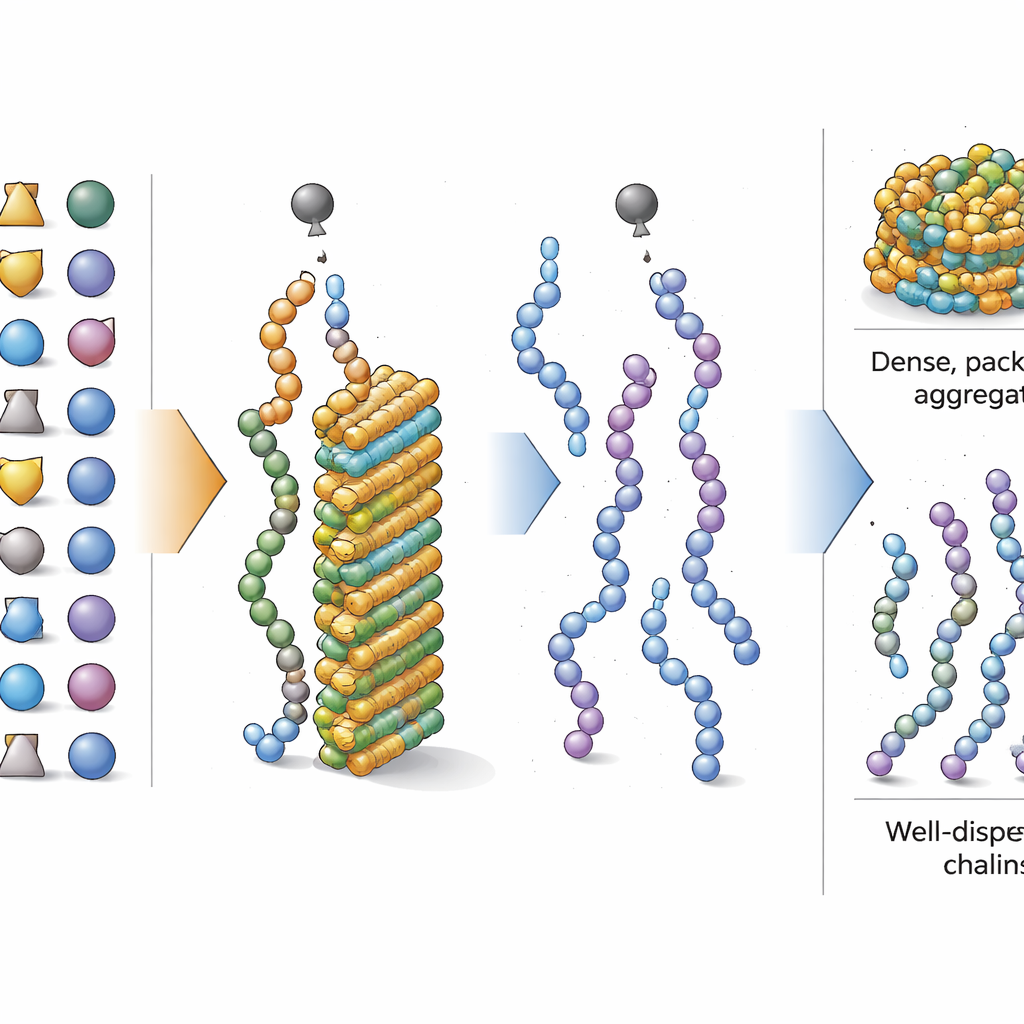
Dobry i zły wpływ aminokwasów
Skoro uwaga przesunęła się na ogólny skład, badacze zapytali następnie, które aminokwasy najsilniej przesuwają peptyd w kierunku lub od agregacji podczas syntezy. Korzystając z interpretowalnego narzędzia uczenia maszynowego, ocenili, jak zwiększenie ułamka danego aminokwasu zmienia predykcję modelu. Stwierdzili, że jednostki z prostymi, „oleistymi” łańcuchami bocznymi — takie jak izoleucyna i walina, a także powszechnie używane chronione formy seryny i treoniny — silnie sprzyjają agregacji, gdy występują w dużych ilościach. Natomiast aminokwasy z bardziej masywnymi lub złożonymi grupami bocznymi, w tym chronione formy fenyloalaniny, tyrozyny, kwasu asparaginowego i argininy, zwykle zmniejszały agregację. Pewne krótkie wzory dwu-aminokwasowe, jak gly–ser i leu–leu, również wykazywały dodatkową skłonność do sklejania, ale dominującym czynnikiem pozostawała ogólna równowaga typów aminokwasów.
Przekuć wnioski w lepsze przepisy syntezy
Posiadając mapę aminokwasów „sklejających” i „odsklejających”, zespół zbudował zestaw modeli, które potrafią zasugerować praktyczne poprawki jeszcze przed przeprowadzeniem syntezy. Dla proponowanego peptydu program przewiduje, czy agregacja jest prawdopodobna, i wskazuje pozycje bliskie zakotwiczonymu końcowi łańcucha, gdzie problematyczne aminokwasy przyczyniają się najbardziej. Następnie rekomenduje zastąpienie ich specjalnymi wersjami, takimi jak bloki budulcowe pseudoprolinowe, które tymczasowo zakłócają agregację, a po końcowym odblokowaniu wracają do pożądanych aminokwasów. Testując tę strategię na dwóch notorycznie problematycznych fragmentach peptydów, badacze wprowadzili niewielką liczbę takich podstawień na pozycjach wybranych przez model. Efektem był dramatyczny wzrost czystości surowego produktu — z około jednej piątej do około trzech czwartych mieszaniny produktu — zgodny z rankingiem modelu wskazującym, które pozycje pomogą najbardziej.
Co to znaczy dla przyszłych leków peptydowych
Dla laika główne przesłanie brzmi: w tych warunkach syntezy sklejanie peptydów zachowuje się mniej jak delikatny mechanizm z zamkiem i kluczem, a bardziej jak problem przepisu masowego: proporcje „oleistych” i „masywnych” składników mają większe znaczenie niż ich dokładna kolejność. Dzięki rozpoznaniu i ilościowemu opisaniu tego zjawiska autorzy mogli zarówno wyjaśnić długo trwające niepowodzenia syntez, jak i zaproponować prosty, oparty na danych sposób ich unikania. Ich praca pokazuje, jak uczenie maszynowe może wydobywać ukryte zasady w procesach chemicznych i przekładać je na proste narzędzia projektowe, co ostatecznie przyspiesza drogę od pomysłów na peptydy do wiarygodnych, skalowalnych leków.
Cytowanie: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Słowa kluczowe: synteza peptydów, skład aminokwasowy, agregacja, uczenie maszynowe, chemia fazy stałej