Clear Sky Science · it
La composizione in amminoacidi guida l’aggregazione durante la sintesi peptidica
Perché le catene piccole contano per i grandi farmaci
Molti farmaci moderni sono catene corte di amminoacidi chiamate peptidi. I chimici possono costruire queste catene un mattone alla volta su piccole perle, ma il processo spesso si blocca perché le catene in crescita si aggregano. Questo studio mostra che non è l’ordine preciso dei mattoni a controllare principalmente questa aggregazione, ma il numero complessivo di ciascun tipo presente. Usando apprendimento automatico ed esperimenti mirati, gli autori rivelano quali amminoacidi favoriscono o impediscono maggiormente l’aggregazione e mostrano come usare queste conoscenze per sintetizzare in modo molto più efficiente peptidi difficili da ottenere.
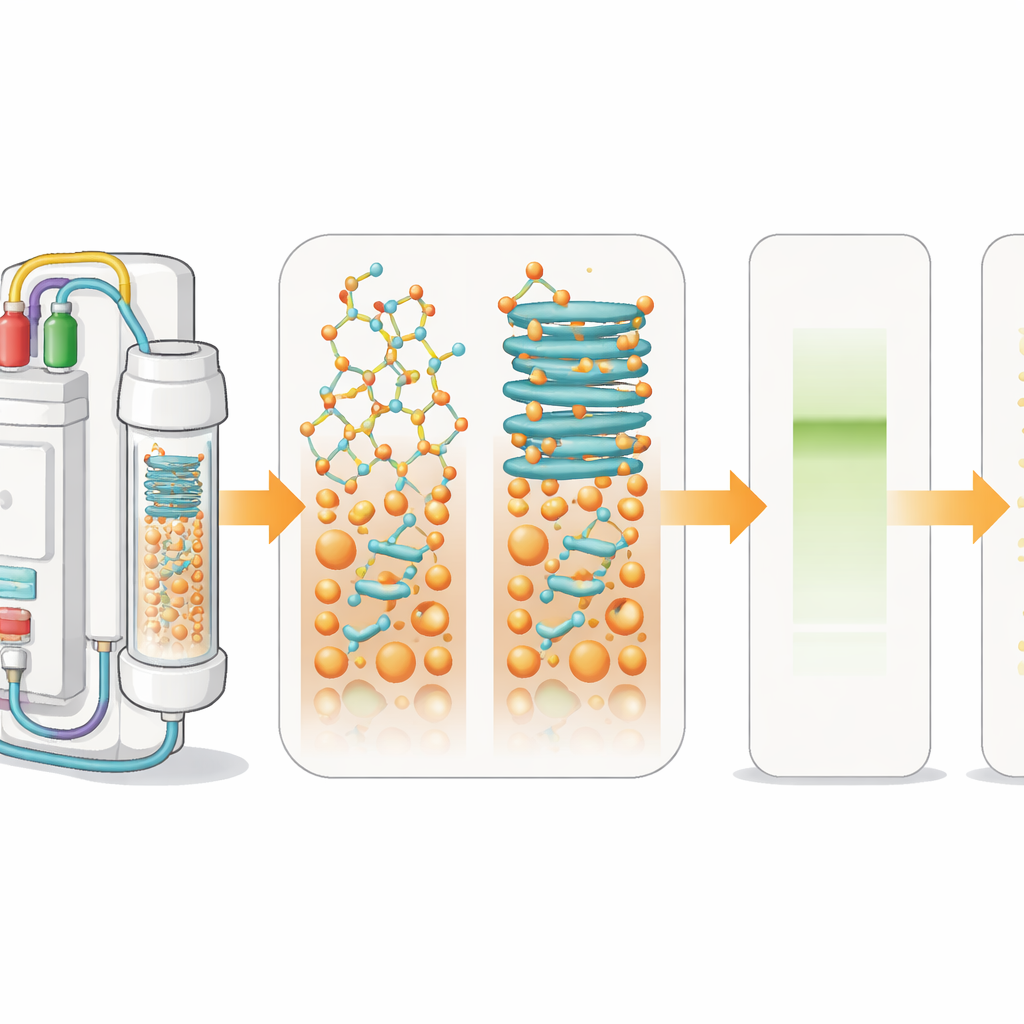
Come si cuciono insieme i farmaci peptidici
Per produrre peptidi in laboratorio, i chimici usano un metodo chiamato sintesi peptidica in fase solida. Il primo amminoacido viene fissato a una perla insolubile, quindi si aggiungono ulteriori amminoacidi in cicli, come infilare perle su un braccialetto. Ad ogni passaggio viene rimosso un gruppo protettivo e si lega una nuova unità. Un rivelatore di luce integrato monitora questi passaggi in tempo reale misurando l’intensità e la forma dei segnali prodotti quando i gruppi protettivi vengono rimossi. Quando le catene in crescita sulle perle cominciano ad attaccarsi tra loro e piegarsi in strutture a foglio, i segnali si allargano. Questa «aggregazione» rallenta le reazioni e porta a miscele di prodotti difettosi invece di un singolo peptide pulito.
Lasciar parlare i dati di migliaia di sintesi
I ricercatori hanno combinato due grandi insiemi di dati di sintesi peptidica automatizzata in flusso, per un totale di oltre 500 sequenze uniche. Per ogni passaggio di ogni sintesi disponevano sia dell’amminoacido aggiunto sia di una misura quantitativa di quanto stesse avvenendo l’aggregazione, estratta dai segnali ottici. Hanno quindi applicato una vasta gamma di approcci di apprendimento automatico — dai modelli moderni in stile linguaggio che leggono le stringhe di amminoacidi come testo, ai modelli statistici classici e ai metodi per serie temporali che trattano una sintesi come una sequenza di eventi — per rispondere a una semplice domanda sì–no: un dato peptide si aggrega nelle condizioni testate?
Un sorprendente spostamento dall’ordine agli ingredienti
Attraverso tutti questi metodi, l’accuratezza predittiva si attestava su un livello modesto simile, indipendentemente da quanto fosse sofisticata la codifica dell’ordine degli amminoacidi. Questo ha portato a un test cruciale. Il team ha mescolato casualmente l’ordine degli amminoacidi in ciascun peptide ma ha mantenuto inalterati i conteggi complessivi di ciascun tipo. Se l’ordine preciso fosse stato determinante, le prestazioni sarebbero dovute crollare. Non è avvenuto: i modelli hanno fatto altrettanto bene sulle sequenze mescolate. Anche quando ogni peptide è stato ridotto a un «vettore di composizione» di 20 numeri che registra semplicemente la frazione di ciascun amminoacido presente, l’accuratezza è rimasta simile. Per confermarlo sperimentalmente, gli autori hanno preso otto peptidi noti — quattro che aggregano e quattro che non lo fanno — e hanno sintetizzato cinque varianti mescolate di ciascuno. La maggior parte delle varianti mescolate si è comportata come gli originali: le sequenze aggreganti hanno continuato ad aggregare, quelle non aggreganti sono rimaste in gran parte solubili, e tendevano ad iniziare l’aggregazione in posizioni simili lungo la catena.
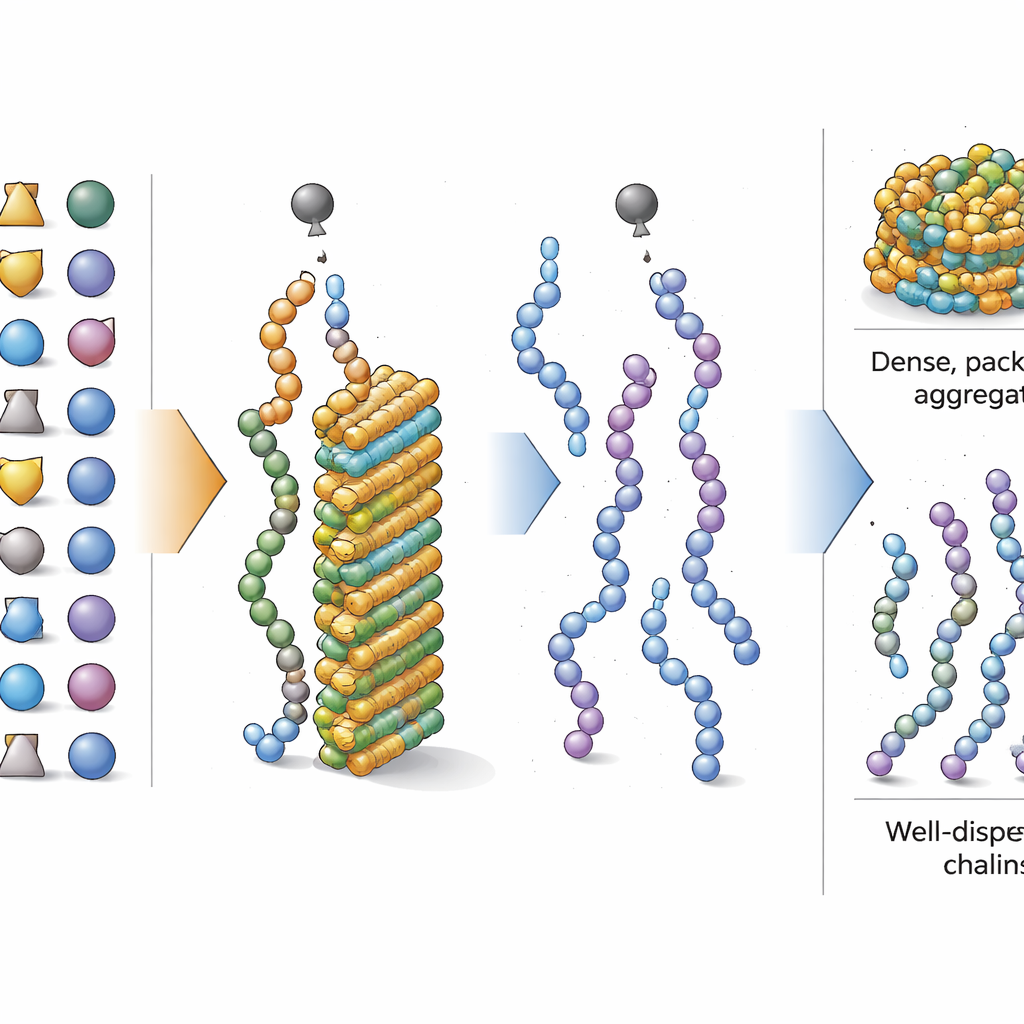
Attori positivi e negativi tra gli amminoacidi
Con lo sguardo spostato sulla composizione complessiva, i ricercatori hanno quindi chiesto quali amminoacidi spingono più fortemente un peptide verso o contro l’aggregazione durante la sintesi. Usando uno strumento interpretabile di machine learning, hanno valutato quanto l’aumento della frazione di ciascun amminoacido modificasse la previsione del modello. Hanno scoperto che i mattoni con catene laterali semplici e oleose — come isoleucina e valina, oltre a forme protette comunemente usate di serina e treonina — favoriscono fortemente l’aggregazione quando sono presenti in elevate quantità. Al contrario, amminoacidi con gruppi laterali più voluminosi o complessi, comprese forme protette di fenilalanina, tirosina, acido aspartico e arginina, tendevano a ridurre l’aggregazione. Alcuni brevi motivi di due amminoacidi, come glicina–serina e leucina–leucina, mostravano anche una tendenza aggiuntiva a causare incollamento, ma il bilancio complessivo dei tipi di amminoacidi rimaneva il fattore dominante.
Trasformare le intuizioni in ricette di sintesi migliori
Muniti di questa mappa degli amminoacidi «aggreganti» e «anti-aggreganti», il team ha costruito un insieme di modelli in grado di suggerire rimedi pratici prima di eseguire una sintesi. Per un peptide proposto, il programma predice se l’aggregazione è probabile e individua posizioni vicine all’estremità ancorata della catena dove amminoacidi problematici contribuiscono maggiormente. Raccomanda quindi di sostituirli con versioni speciali, come i blocchi di costruzione pseudoprolinici, che interrompono temporaneamente l’aggregazione ma ritornano agli amminoacidi desiderati dopo il passo finale di deprotezione. Testando questa strategia su due frammenti peptidici notoriamente problematici, i ricercatori hanno introdotto un piccolo numero di tali sostituzioni nelle posizioni selezionate dal modello. Il risultato è stato un aumento drammatico della purezza grezza — da circa un quinto a circa tre quarti della miscela di prodotti — in linea con la graduatoria del modello su quali posizioni avrebbero aiutato di più.
Cosa significa per i futuri farmaci peptidici
Per un non specialista, il messaggio centrale è che, per queste condizioni di sintesi, l’incollamento dei peptidi si comporta meno come un meccanismo delicato a serratura e chiave e più come un problema di ricetta all’ingrosso: le proporzioni degli ingredienti «oleosi» e «voluminosi» contano più del loro ordine esatto. Riconoscendo e quantificando questo, gli autori hanno potuto sia spiegare fallimenti di sintesi di lunga data sia offrire un modo semplice e guidato dai dati per evitarli. Il loro lavoro mostra come l’apprendimento automatico possa scoprire regole nascoste nei processi chimici e convertirle in strumenti di progettazione diretti, accelerando infine il percorso dalle idee peptidiche a farmaci affidabili e scalabili.
Citazione: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Parole chiave: sintesi peptidica, composizione in amminoacidi, aggregazione, apprendimento automatico, chimica in fase solida