Clear Sky Science · pt
A composição de aminoácidos determina a agregação durante a síntese de peptídeos
Por que cadeias minúsculas importam para grandes medicamentos
Muitos medicamentos modernos são cadeias curtas de aminoácidos chamadas peptídeos. Químicos podem construir essas cadeias bloco a bloco em pequenas esferas, mas o processo frequentemente emperra porque as cadeias em crescimento se aglutinam. Este estudo mostra que não é principalmente a ordem exata dos blocos que controla essa aglomeração, e sim quantas unidades de cada tipo estão presentes no conjunto. Usando aprendizado de máquina e experimentos direcionados, os autores revelam quais aminoácidos impulsionam ou evitam fortemente a aglomeração e mostram como usar esse conhecimento para sintetizar peptídeos difíceis de forma muito mais eficiente.
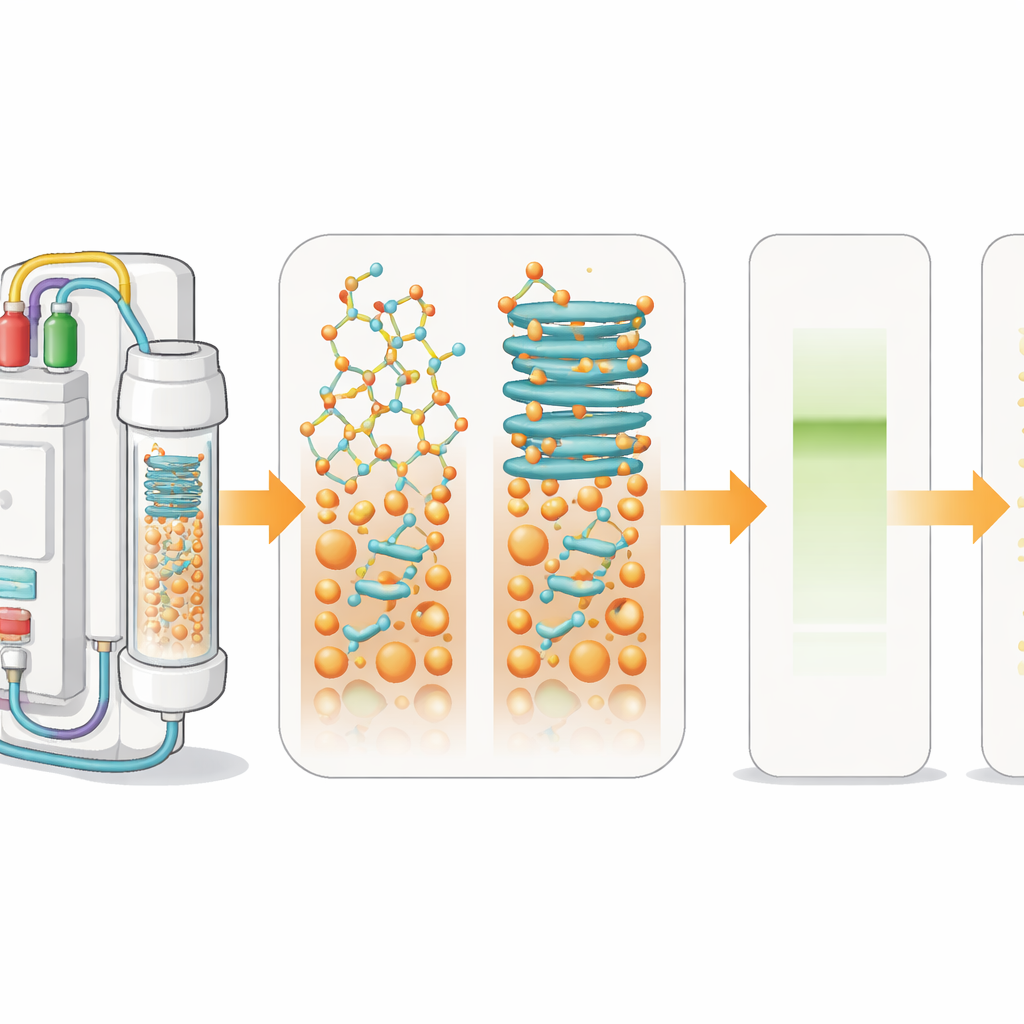
Como os fármacos peptídicos são montados
Para fabricar peptídeos em laboratório, os químicos usam um método chamado síntese de peptídeos em fase sólida. O primeiro aminoácido é ligado a uma esfera insolúvel e, em seguida, aminoácidos adicionais são adicionados em ciclos, como colocar contas em uma pulseira. Em cada etapa, um grupo protetor é removido e uma nova unidade é acoplada. Um detector de luz embutido acompanha essas etapas em tempo real medindo o tamanho e a forma dos sinais produzidos quando grupos protetores são retirados. Quando as cadeias em crescimento nas esferas começam a colar-se e formar estruturas em folha, os sinais se alargam. Essa “agregação” desacelera as reações e leva a misturas de produtos defeituosos em vez de um único peptídeo limpo.
Deixar os dados falarem por milhares de sínteses
Os pesquisadores combinaram dois grandes conjuntos de dados de sínteses automatizadas de peptídeos em fluxo, totalizando mais de 500 sequências únicas. Para cada etapa de cada síntese, eles dispuseram tanto do aminoácido adicionado quanto de uma medida quantitativa de quanta agregação estava ocorrendo, extraída dos sinais baseados em luz. Em seguida aplicaram uma ampla gama de abordagens de aprendizado de máquina — desde modelos modernos estilo linguagem que leem sequências de aminoácidos como texto, até modelos estatísticos clássicos e métodos de séries temporais que tratam uma síntese como uma sequência de eventos — para responder a uma pergunta simples de sim/não: um dado peptídeo agrega nas condições testadas?
Uma mudança surpreendente da ordem para os ingredientes
Em todos esses métodos, a precisão de previsão ficou em um nível modesto e semelhante, independentemente de quão engenhosamente a ordem dos aminoácidos fosse codificada. Isso motivou um teste decisivo. A equipe embaralhou aleatoriamente a ordem dos aminoácidos em cada peptídeo, mas manteve as contagens totais de cada tipo iguais. Se a ordem precisa fosse crucial, o desempenho deveria despencar. Não foi o caso: os modelos se saíram tão bem com as sequências embaralhadas. Mesmo quando cada peptídeo foi reduzido a um “vetor de composição” de 20 números que registra simplesmente a fração de cada aminoácido presente, a precisão permaneceu similar. Para confirmar isso experimentalmente, os autores tomaram oito peptídeos conhecidos — quatro que agregam e quatro que não — e sintetizaram cinco versões embaralhadas de cada um. A maioria das variantes embaralhadas comportou-se como os originais: sequências que agregavam continuaram a agregar, e as não agregantes permaneceram em grande parte solúveis, tendendo a iniciar a agregação em posições semelhantes ao longo da cadeia.
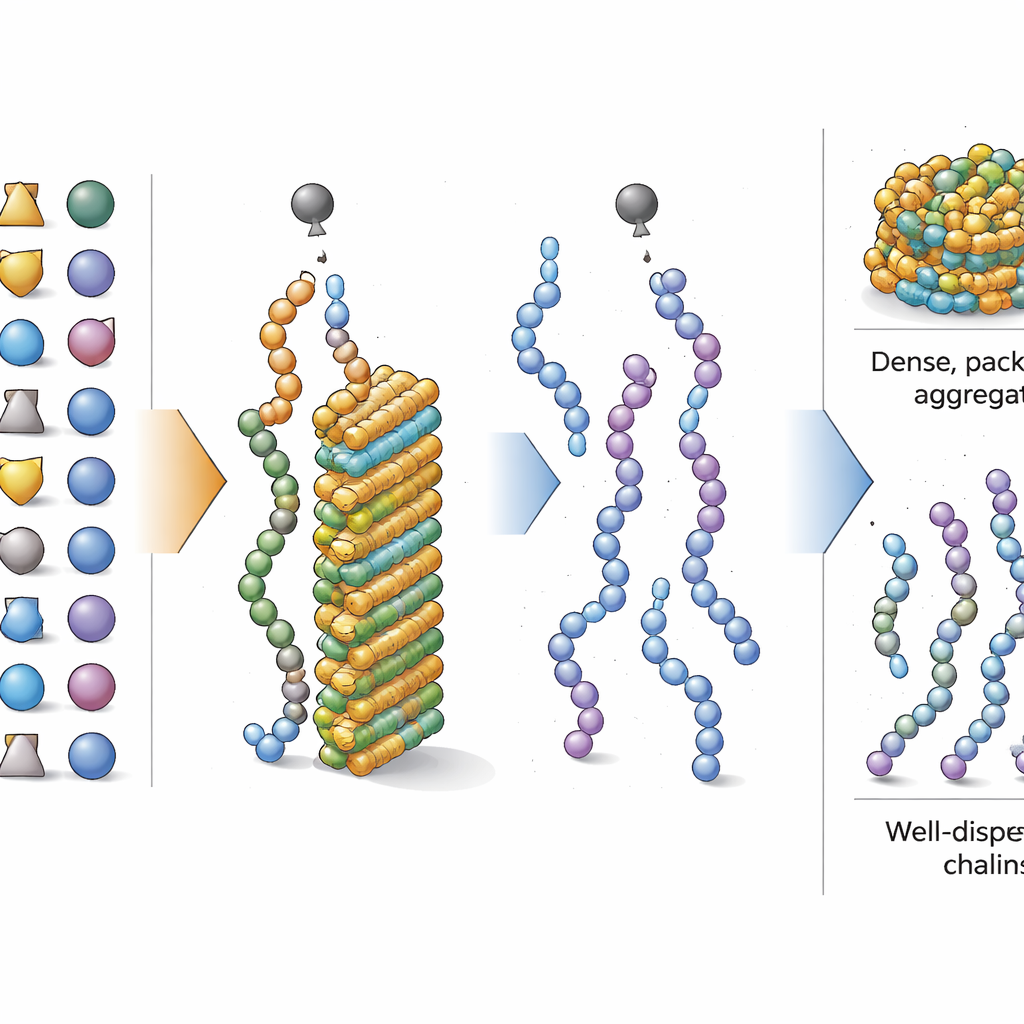
Heróis e vilões entre os aminoácidos
Com o foco deslocado para a composição total, os pesquisadores perguntaram em seguida quais aminoácidos inclinavam mais fortemente um peptídeo para agregar ou para permanecer solúvel durante a síntese. Usando uma ferramenta de aprendizado de máquina interpretável, eles pontuaram quanto aumentar a fração de cada aminoácido alterava a previsão do modelo. Encontraram que blocos de construção com cadeias laterais simples e oleosas — como isoleucina e valina, bem como formas protegidas comumente usadas de serina e treonina — promovem fortemente a agregação quando presentes em altas quantidades. Em contraste, aminoácidos com grupos laterais mais volumosos ou complexos, incluindo formas protegidas de fenilalanina, tirosina, ácido aspártico e arginina, tenderam a reduzir a agregação. Certos padrões curtos de dois aminoácidos, como glicina–serina e leucina–leucina, também mostraram tendência adicional a causar aglutinação, mas o balanço geral dos tipos de aminoácidos permaneceu o fator dominante.
Transformando insights em receitas de síntese melhores
Munida desse mapa de aminoácidos “agregantes” e “desagregantes”, a equipe construiu um conjunto de modelos que pode sugerir correções práticas antes de rodar uma síntese. Para um peptídeo proposto, o programa prevê se a agregação é provável e identifica posições próximas à extremidade ancorada da cadeia onde aminoácidos problemáticos mais contribuem. Em seguida recomenda trocar esses por versões especiais, como blocos de construção pseudoprolina, que interrompem temporariamente a agregação mas reverte m para os aminoácidos desejados após a etapa final de desproteção. Testando essa estratégia em dois fragmentos peptídicos notoriamente problemáticos, os pesquisadores introduziram um pequeno número dessas substituições em posições selecionadas pelo modelo. O resultado foi um salto dramático na pureza bruta — de aproximadamente um quinto para cerca de três quartos da mistura do produto — em concordância com o ranking do modelo sobre quais posições ajudariam mais.
O que isso significa para futuros medicamentos peptídicos
Para um não especialista, a mensagem central é que, nas condições sintéticas estudadas, a aglomeração de peptídeos comporta-se menos como um padrão delicado de fechadura e chave e mais como um problema de receita em escala: as proporções dos ingredientes “oleosos” e “volumosos” importam mais do que sua ordem exata. Ao reconhecer e quantificar isso, os autores puderam tanto explicar falhas de síntese de longa data quanto oferecer uma maneira simples e orientada por dados de evitá-las. O trabalho demonstra como o aprendizado de máquina pode descobrir regras ocultas em processos químicos e convertê-las em ferramentas de projeto diretas, acelerando afinal o caminho de ideias peptídicas a medicamentos confiáveis e escaláveis.
Citação: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Palavras-chave: síntese de peptídeos, composição de aminoácidos, agregação, aprendizado de máquina, química em fase sólida