Clear Sky Science · sv
Aminosyrasammansättning styr aggregering under peptidsyntes
Varför små kedjor har betydelse för stora läkemedel
Många moderna läkemedel är korta kedjor av aminosyror kallade peptider. Kemister bygger dessa kedjor en byggsten åt gången på små pärlor, men processen stannar ofta upp eftersom växande kedjor klumpar ihop sig. Denna studie visar att det inte är den exakta ordningen av byggstenar som främst styr denna klumpning, utan hur många av varje typ som finns totalt. Genom att kombinera maskininlärning och riktade experiment visar författarna vilka aminosyror som starkt driver eller förhindrar klumpning och hur man kan använda denna kunskap för att tillverka svårsyntetiserade peptider mycket effektivare.
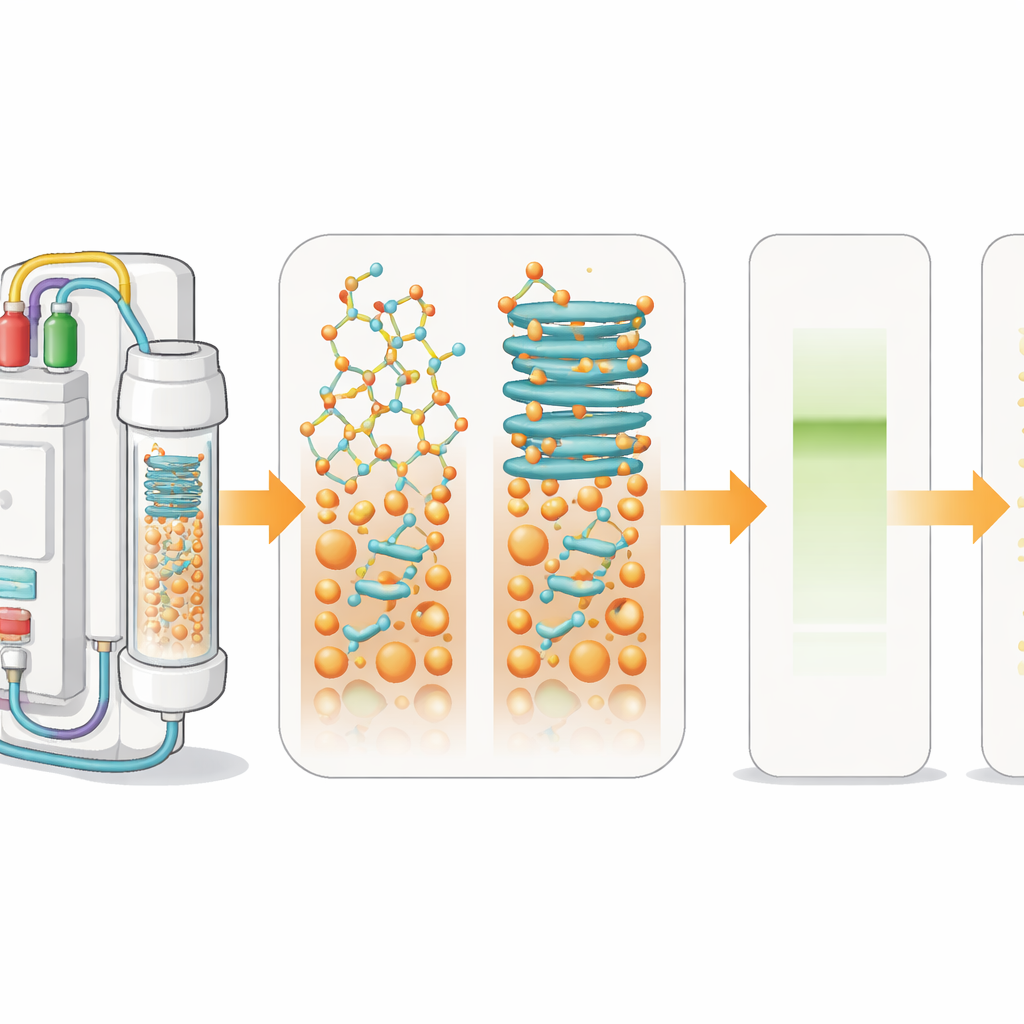
Hur peptidläkemedel sys ihop
För att tillverka peptider i labbet använder kemister en metod kallad fastfas-peptidsyntes. Den första aminosyran fästs på en olöslig pärla, och sedan tillsätts ytterligare aminosyror i cykler, ungefär som att trä pärlor på ett armband. Vid varje steg avlägsnas en skyddsgrupp och en ny enhet kopplas på. En inbyggd ljusdetektor följer dessa steg i realtid genom att mäta storlek och form på signaler som uppstår när skyddsgrupper tas bort. När de växande kedjorna på pärlorna börjar fastna ihop och vika sig till ark-liknande strukturer breddas signalerna. Denna ”aggregering” saktar ned reaktionerna och leder till blandningar av felaktiga produkter i stället för en enda ren peptid.
Låta data tala för tusentals synteser
Forskarlaget slog ihop två stora dataset från automatiserade flowbaserade peptidsynteser, totalt mer än 500 unika sekvenser. För varje steg i varje syntes hade de både den aminosyra som tillsattes och ett kvantitativt mått på hur mycket aggregering som pågick, extraherat från ljussignalerna. De tillämpade sedan en rad olika maskininlärningsmetoder — från moderna språkstilade modeller som läser aminosyrasekvenser som text, till klassiska statistiska modeller och tidsseriemetoder som behandlar en syntes som en sekvens av händelser — för att besvara en enkel ja–nej-fråga: aggregerar en given peptid under testade förhållanden?
En överraskande förskjutning från ordning till ingredienser
I alla dessa metoder låg prediktionsnoggrannheten på ungefär samma måttliga nivå, oavsett hur smart aminosyraordningen kodades. Det ledde till ett avgörande test. Teamet slumpade ordningen på aminosyrorna i varje peptid men behöll den totala förekomsten av varje typ. Om exakt ordning varit avgörande borde prestandan kollapsa. Det gjorde den inte: modellerna klarade sig lika bra på permuterade sekvenser. Även när varje peptid reducerades till en 20-talig ”sammansättningsvektor” som helt enkelt anger andelen av varje aminosyra, förblev noggrannheten likartad. För att bekräfta detta experimentellt tog författarna åtta kända peptider — fyra som aggregerar och fyra som inte gör det — och syntetiserade fem slumpade varianter av varje. De flesta permuterade varianterna uppträdde likt originalen: aggregerande sekvenser fortsatte att aggregera och icke-aggregerande förblev till stor del lösliga, och de tenderade att börja aggregera vid liknande positioner längs kedjan.
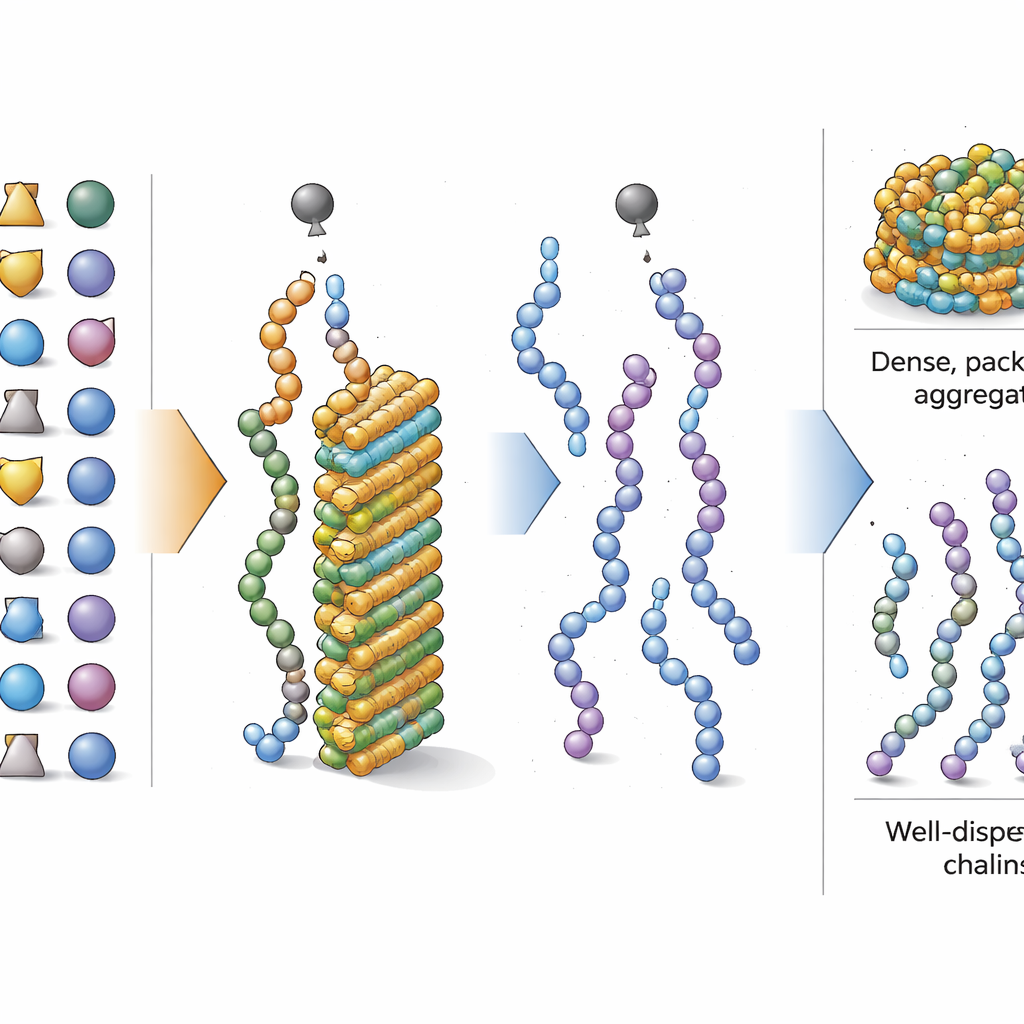
Goda och dåliga aktörer bland aminosyror
Med fokus förskjuten till total sammansättning frågade forskarna därefter vilka aminosyror som starkast tippar en peptid mot eller bort från aggregering under syntesen. Med ett tolkbart maskininlärningsverktyg skattade de hur mycket en ökning i andelen av varje aminosyra förändrade modellens prediktion. De fann att byggstenar med enkla, oljiga sidokedjor — såsom isoleucin och valin, liksom vanligen använda skyddade former av serin och treonin — starkt främjar aggregering när de förekommer i höga mängder. Däremot tenderade aminosyror med större eller mer komplexa sidogrupper, inklusive skyddade former av fenylalanin, tyrosin, asparaginsyra och arginin, att minska aggregering. Vissa korta två-aminosyramönster, som glycin–serin och leucin–leucin, visade också en ökad tendens att orsaka klumpning, men den övergripande balansen av aminosyratyper förblev den dominerande faktorn.
Göra insikter till bättre syntesrecept
Med denna karta över ”klumpande” och ”avklumpande” aminosyror byggde teamet ett ensemble av modeller som kan föreslå praktiska åtgärder innan en syntes körs. För en föreslagen peptid förutspår programmet om aggregering är sannolik och pekar ut positioner nära den förankrade änden av kedjan där problematiska aminosyror bidrar mest. Det rekommenderar sedan att byta ut dessa mot speciella varianter, såsom pseudoprolin-byggstenar, som temporärt stör aggregering men återgår till önskade aminosyror efter den slutliga avskyddssteget. När de testade denna strategi på två beryktade problematiska peptidfragment infördes ett litet antal sådana substitutioner på modellvalda positioner. Resultatet var ett dramatiskt hopp i rårenhet — från ungefär en femtedel till cirka tre fjärdedelar av produktblandningen — i linje med modellens prioritering av vilka positioner som skulle hjälpa mest.
Vad detta betyder för framtida peptidläkemedel
För en icke-specialist är huvudbudskapet att, för dessa syntesförhållanden, beter sig peptidklumpning mindre som ett känsligt lås-och-nyckel-mönster och mer som ett problem med receptets proportioner: andelarna av de ”oljiga” respektive ”skrymmande” ingredienserna spelar större roll än deras exakta ordning. Genom att känna igen och kvantifiera detta kunde författarna både förklara långvariga syntesproblem och erbjuda ett enkelt, datadrivet sätt att undvika dem. Deras arbete visar hur maskininlärning kan upptäcka dolda regler i kemiska processer och omvandla dem till lättanvända designverktyg, vilket i slutändan snabbar på vägen från peptididéer till tillförlitliga, skalbara läkemedel.
Citering: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
Nyckelord: peptidsyntes, aminosyrasammansättning, aggregering, maskininlärning, fastfas-kemi