Clear Sky Science · ja
アミノ酸組成がペプチド合成中の凝集を左右する
小さな鎖が大きな医薬品にとって重要な理由
現代の医薬品の多くはペプチドと呼ばれる短いアミノ酸の鎖です。化学者はこれらの鎖を小さなビーズ上で一つずつ組み立てられますが、成長する鎖が互いにかたまってしまい工程が停滞することがよくあります。本研究は、この「かたまり」は個々の構成要素の正確な配列よりも、各種類のアミノ酸が全体にどれだけ含まれているかという全体的な量に主に支配されることを示しています。機械学習と標的を絞った実験を用いて、どのアミノ酸が凝集を強く促進または抑制するかを明らかにし、合成が難しいペプチドをはるかに効率的に作る方法を提示します。
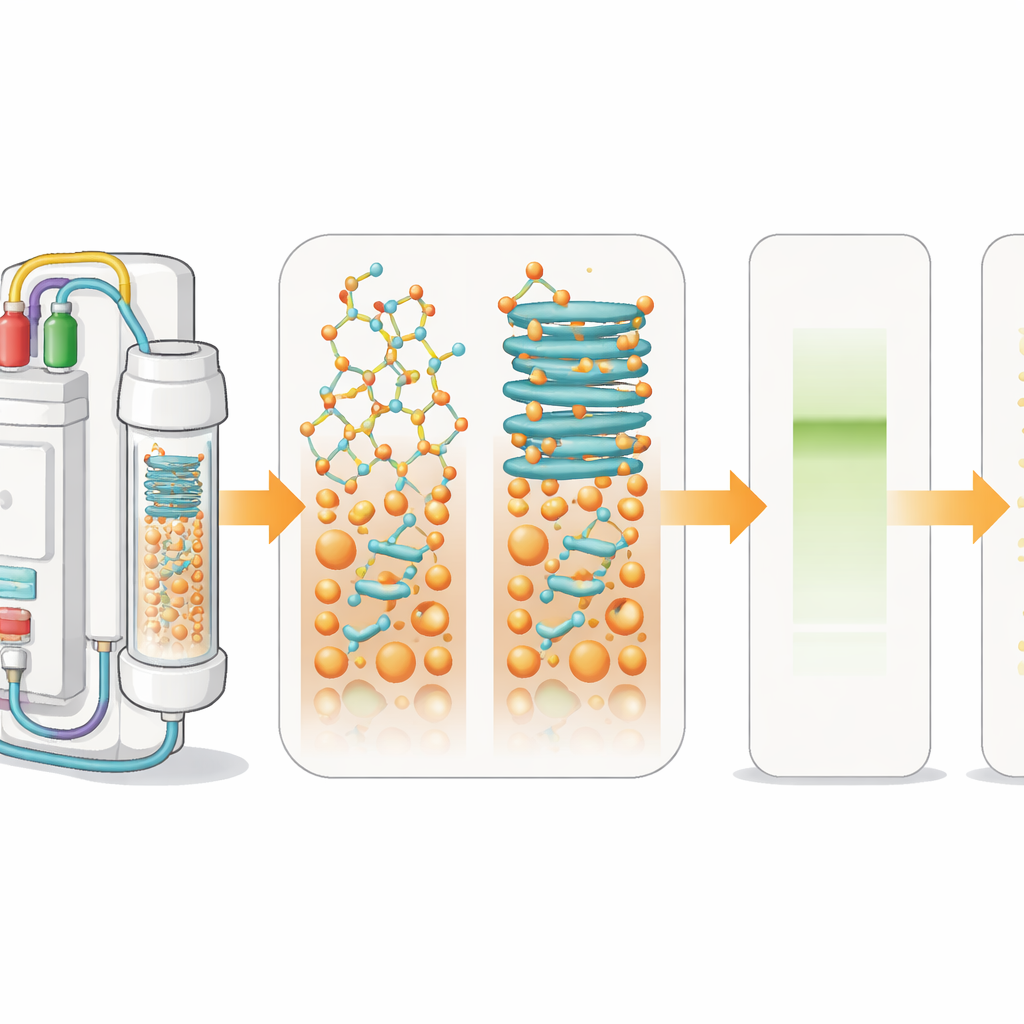
ペプチド医薬はどうやって綴じられるか
実験室でペプチドを作るには、固相ペプチド合成と呼ばれる方法が使われます。最初のアミノ酸を不溶性のビーズに結び付け、その後追加のアミノ酸をサイクルごとに、ブレスレットにビーズをはめるように順次結合させます。各ステップでは保護基が除去され、新しい単位が結合されます。保護基が外れるときに生じる信号の大きさや形を測る内蔵の光検出器がこれらの工程をリアルタイムで追跡します。ビーズ上の伸長中の鎖が互いにまとまりシート状に折りたたまれ始めると、信号が広がります。この「凝集」は反応を遅らせ、単一のきれいなペプチドではなく欠陥を含む混合物を生み出します。
何千もの合成からデータに語らせる
研究者たちは、自動流動型ペプチド合成の大規模データセットを2件結合し、合わせて500を超えるユニークな配列を扱いました。各合成の各ステップについて、追加されるアミノ酸の種類と、光信号から抽出した定量的な凝集の程度が記録されていました。研究チームは、アミノ酸配列をテキストのように読む現代的な言語モデルから、古典的な統計モデルや時系列手法まで幅広い機械学習アプローチを適用し、単純な二者択一の問いに答えようとしました:与えられた条件下でそのペプチドは凝集するか、しないか?
配列から成分へという意外な転換
これらすべての方法で、アミノ酸の順序をどれだけ巧妙に符号化しても、予測精度は概ね同じ控えめな水準にとどまりました。そこで重要な検証が行われます。各ペプチドのアミノ酸の順序をランダムにシャッフルしつつ、各種類の総数はそのままにしました。もし正確な順序が重要であれば予測性能は崩れるはずです。しかしそうはなりませんでした:モデルはシャッフルされた配列でも同程度にうまく機能しました。各ペプチドを20次元の“組成ベクトル”――各アミノ酸の存在比率を単純に記録した数値列――に縮約しても、精度はほとんど変わりませんでした。実験的に確認するため、著者らは既知の8つのペプチド(凝集するもの4つ、しないもの4つ)を取り、それぞれ5つのシャッフル版を合成しました。ほとんどのシャッフル変異体は元の挙動を保ちました:凝集する配列は依然凝集し、非凝集性の配列は大部分が可溶性を保ち、凝集を始める位置も鎖に沿って類似していました。
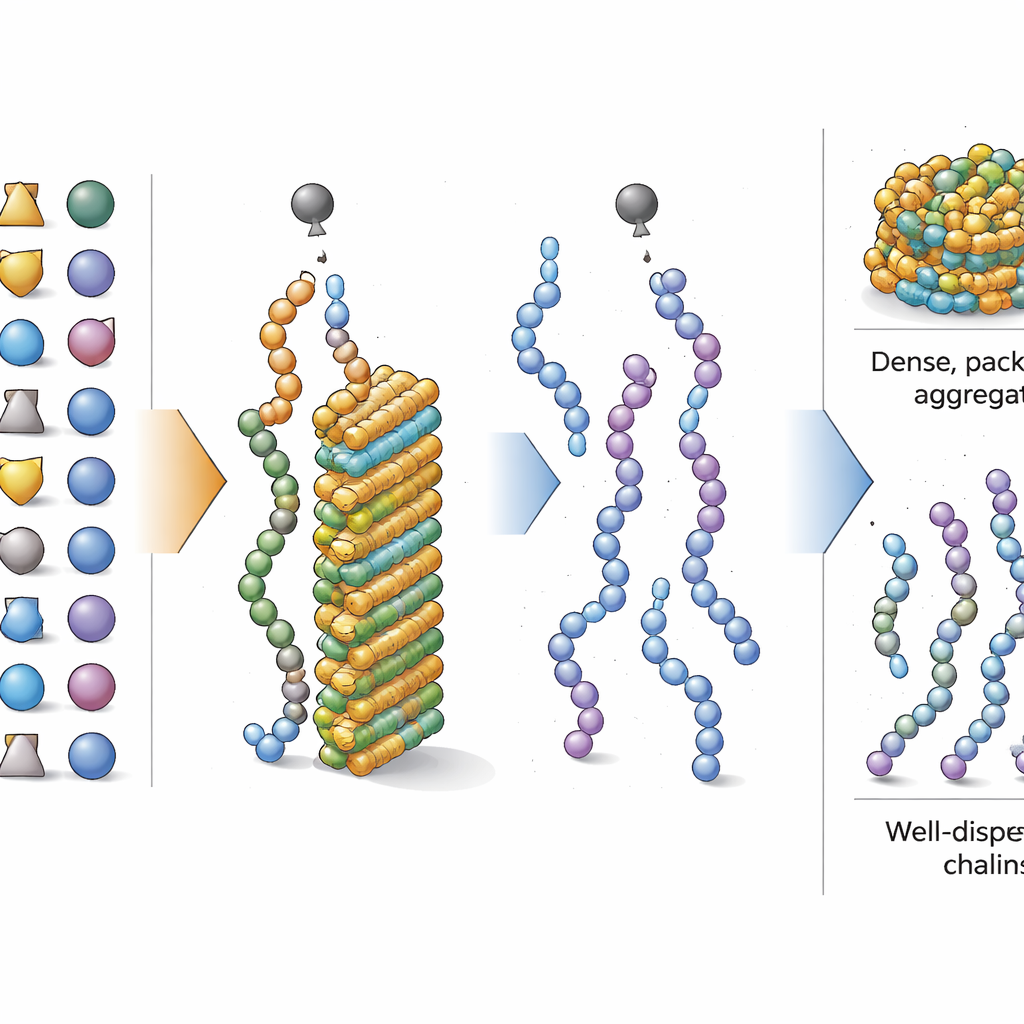
アミノ酸の間での良し悪し
全体の組成に焦点が移ったところで、研究者らは次に、合成中の凝集を促進または抑制するアミノ酸がどれかを問い直しました。解釈可能な機械学習ツールを用い、各アミノ酸の比率を増やすことがモデルの予測にどれだけ影響するかを評価しました。その結果、イソロイシンやバリンのような単純で疎水性の側鎖を持つ構成要素――および保護された形のセリンやスレオニンなど――が高割合で存在すると強く凝集を促進することがわかりました。一方で、保護されたフェニルアラニンやチロシン、アスパラギン酸、アルギニンなど、よりかさ高いか複雑な側鎖を持つアミノ酸は凝集を減らす傾向がありました。グリシン–セリンやロイシン–ロイシンのような短い二残基のパターンが追加で凝集を起こしやすい傾向を見せることもありましたが、全体としてはアミノ酸型のバランスが支配的な要因でした。
知見をより良い合成処方へ変える
「凝集を促す」アミノ酸と「凝集を抑える」アミノ酸の地図を得て、研究チームは合成を実行する前に実用的な修正を提案できるモデルアンサンブルを構築しました。提案されたペプチドについて、プログラムは凝集が起きそうかを予測し、鎖の固定端近くで問題となるアミノ酸が最も寄与している位置を特定します。続いて疑似プロリンのように一時的に凝集を乱すが最終的な脱保護後には元のアミノ酸に戻る特殊なビルディングブロックへの置換を推奨します。この戦略を特に扱いにくい2つのペプチド断片に適用して、モデルが選んだ位置に少数の置換を導入したところ、粗生成物の純度が劇的に向上しました――おおむね5分の1程度から約4分の3へと上昇し、どの位置の変更が効果的かというモデルのランク付けと一致しました。
将来のペプチド医薬にとっての意義
専門外の人にとっての中心的なメッセージは、これらの合成条件下ではペプチドの凝集は繊細な鍵と鍵穴のような配列依存の振る舞いというよりも、どの「油っぽい」成分と「かさ高い」成分がどの割合で混ざっているかという大枠のレシピ問題に近い、ということです。これを認識し定量化することで、著者らは長年続いた合成失敗の説明がつき、それを回避するためのシンプルでデータ駆動型の手法を提供できました。本研究は、機械学習が化学プロセスの隠れた規則を明らかにし、それを単純な設計ツールに変換して、アイデアから信頼性のあるスケーラブルな医薬品への道筋を加速できることを示しています。
引用: Tamás, B., Alberts, M., Laino, T. et al. Amino acid composition drives aggregation during peptide synthesis. Nat. Chem. 18, 677–685 (2026). https://doi.org/10.1038/s41557-026-02090-0
キーワード: ペプチド合成, アミノ酸組成, 凝集, 機械学習, 固相化学