Clear Sky Science · tr
SAGA ÇEKİRDEĞİNİN bozulması KAT2A'nın yan yıkımını tetikler
Hücre Mekaniği Parçalandığında
Her hücre içinde, genleri açıp kapamak gibi hayati görevler birçok farklı protein parçasından oluşan büyük moleküler makinelerce yerine getirilir. Bu çalışma, genleri açmaya yardımcı olan ve kanserlerde sıkça sömürülen SAGA adlı makinayı inceliyor. Araştırmacılar, SAGA’nın temel yapısal parçalarına zarar verirseniz yalnızca makineyi zayıflatmakla kalmayıp, ana işleyici bileşenlerinden biri olan KAT2A adlı proteinin seçici olarak yok edilmesini tetiklediğini keşfettiler; bu da ilaçların potansiyel olarak hedefleyebileceği gizli bir zayıflığı açığa çıkarıyor.
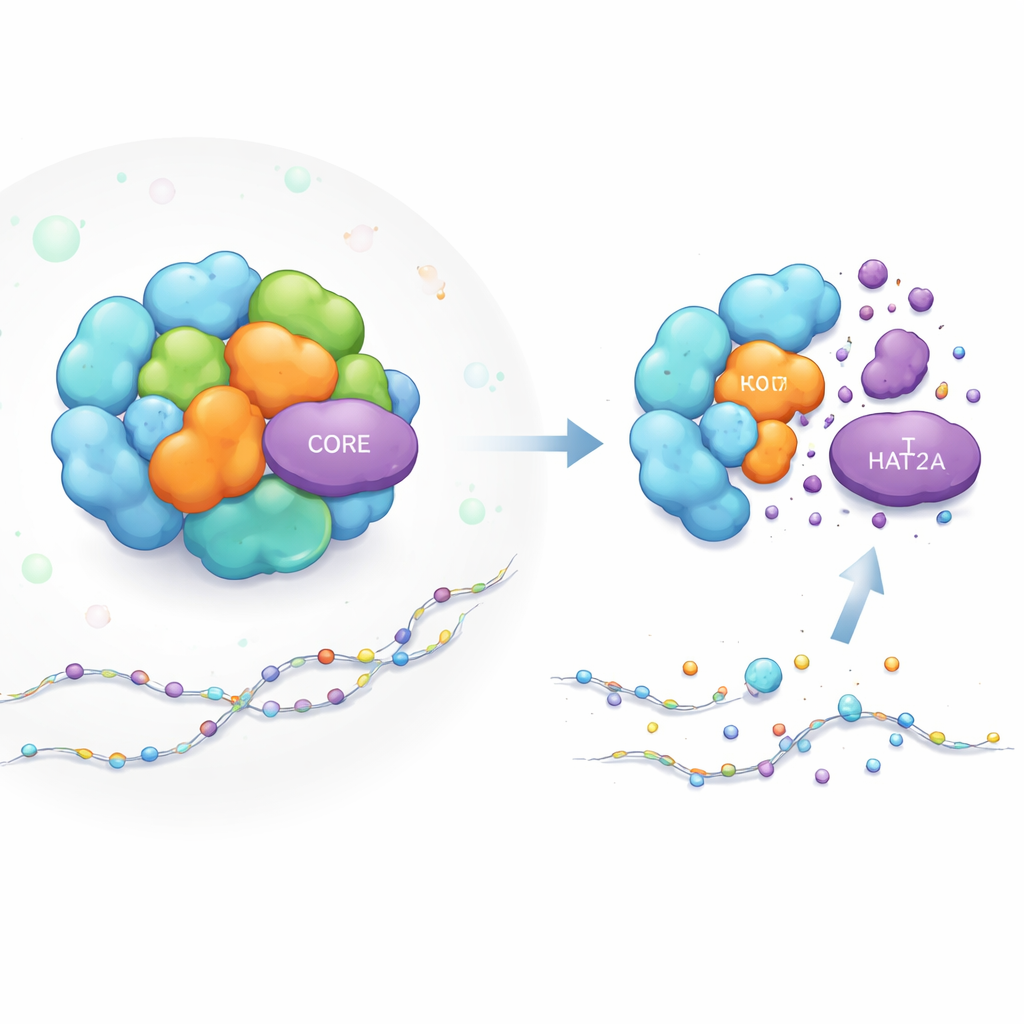
Bir Gen Anahtarlama Makinesi Nasıl Kurulur
SAGA kompleksi, gen etkinleştirme için modüler bir atölye gibidir. Bazı parçalar, histon proteinlerine (DNA’yı paketleyen makaralar) asetil “etiketleri” eklemek gibi kimyasal görevleri yapar; bu, yakınlardaki genlerin daha kolay açılmasını sağlar. KAT2A, SAGA’nın ana modüllerinden birinde asetil ekleyen işçidir. Diğer SAGA bileşenleri ise iskele gibi davranarak yapıya şekil verir ve modülleri DNA’ya yakın doğru konumda tutar. Bilim insanları SAGA’nın ne yaptığını büyük ölçüde biliyordu, ancak KAT2A gibi bireysel parçaların bu kalabalık ve dinamik makine içinde nasıl kararlılığının korunduğu anlaşılamamıştı.
Parçalar Çıkarılınca Ne Olacağını Test Etmek
SAGA’nın iç işleyişini incelemek için yazarlar, hücrelerdeki KAT2A miktarıyla orantılı olarak parlayan bir floresan raporlayıcı geliştirdiler. CRISPR gen düzenleme ile SAGA bileşenlerini teker teker sildiler ve KAT2A seviyelerinin nasıl değiştiğini gözlemlediler. Aynı asetilasyon modülündeki birkaç yakın ortak çıkarıldığında KAT2A bolluğu azaldı, beklendiği gibi. Ancak şaşırtıcı şekilde, TADA1, TAF5L ve TAF6L adlı belirli bir yapısal ÇEKİRDEK üçlüsünün çıkarılması da KAT2A proteininde keskin bir düşüşe neden oldu; oysa bu parçalar doğrudan kimyasal reaksiyonlar gerçekleştirmez. Etki, lösemi hücreleri dahil olmak üzere birden fazla insan hücre tipinde görüldü; bu da bunun hücre hattına özgü bir anomali değil, genel bir özellik olduğunu gösteriyor.
Bozuk Yapıdan Kayıp Gen Aktivitesine
Moleküler sonuçlara daha yakından bakıldığında, ekip bu ÇEKİRDEK proteinlerin kaybının sadece KAT2A düzeylerini kırpmaktan daha fazlasını yaptığını gösterdi. SAGA kompleksi kendisi dağılıyor ve asetilasyon modülü daha büyük yapının dışına ayrılıyor. Hücresel bileşenleri boyuta göre ayırdıklarında, KAT2A, sağlam SAGA’yı temsil eden yüksek moleküler ağırlıklı fraksiyonlardan tek başına proteine uygun daha hafif fraksiyonlara kaydı. Aynı zamanda KAT2A, genom genelinde DNA başlangıç bölgelerinden büyük ölçüde kayboldu ve histon H3 üzerinde oluşturduğu (K9 olarak adlandırılan) asetil işaretleri önemli ölçüde azaldı. Önemli olarak, ÇEKİRDEK’in bozulması, ilişkili bir enzim olan KAT2B’nin telafi edici yanıtını engelledi; bu da asetilasyon kaybını daha derin ve hücrenin onarmasını zorlaştıran bir hâle getirdi.
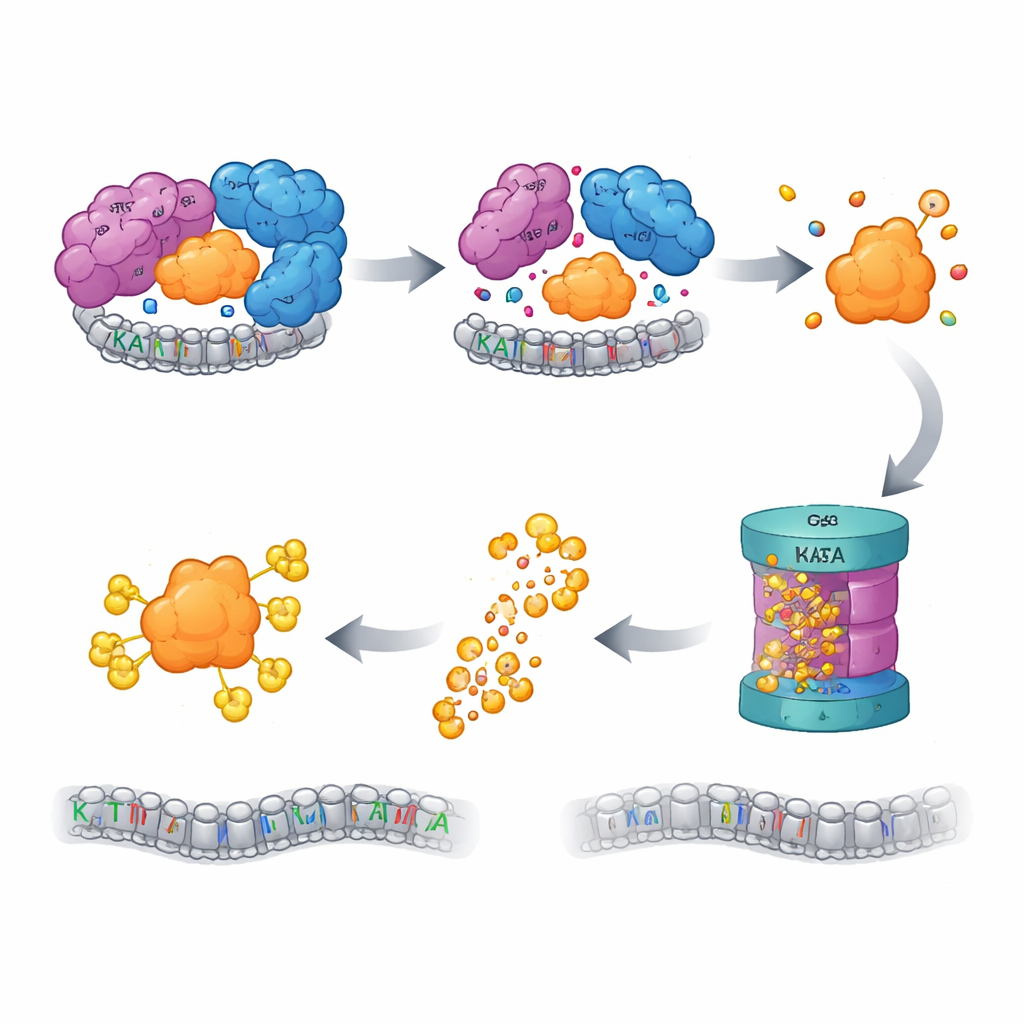
Kalite Kontrol Parçalama Modunu Açıyor
Hücreler, ortaklarını kaybetmiş ve yanlış katlanma veya kümelenme riski taşıyan “yetim” proteinleri izleyen kalite kontrol sistemlerine sahiptir. Yazarlar, SAGA ÇEKİRDEK bozulduğunda serbest KAT2A’nın hücrenin ana protein imha mekanizması olan ubiquitin–proteazom sistemi tarafından yok edilmek üzere işaretlendiğini buldu. Proteazomu veya bu etiketleme kaskadındaki daha önceki adımları engellemek KAT2A seviyelerini geri getirdi. Binin üzerinde ubiquitin ilişkili genin yer aldığı odaklanmış bir CRISPR taraması, UBR5 adında bir E3 ligaz ile onun yardımcı deubiquitinazı OTUD5’i, yetim KAT2A’yı tanıma ve yok etmede kilit oyuncular olarak belirledi. İlginç şekilde, KAT2A’nın yakın akrabası KAT2B aynı koşullar altında stabil kaldı ve KAT2A’nın başına yakın kısa, KAT2A’ya özgü bir diziyi mutasyona uğratmak proteinin yok edilmeye karşı daha dirençli olmasını sağladı; bu, KAT2A’yı imha için işaretleyen minimal, paraloglara özgü bir “degron”u tanımlıyor.
Tedavi Umudu Taşıyan Gizli Bir Zayıflık
Genel olarak çalışma, KAT2A’nın kararlılığı ve aktivitesinin SAGA kompleksinin bütün mimarisiyle sıkı sıkıya bağlı olduğunu gösteriyor. Yapısal ÇEKİRDEK bileşenleri kaybolduğunda SAGA dağılır, KAT2A korunmasız bir yetim olarak serbest kalır ve UBR5–OTUD5 gözetim sistemi hızla onu hücresel parçalama makinesine yönlendirir; bu da genom genelinde genleri açan asetil işaretlerini azaltır. KAT2A birkaç kanserde bilinen bir zayıflık olduğundan, yapı, montaj ve seçici yıkım arasındaki bu yerleşik bağlantı yeni bir strateji öneriyor: ilaçlar KAT2A’nın aktif bölgesini doğrudan hedeflemek yerine, enzimatik olmayan SAGA iskele proteinlerini destabilize ederek hem KAT2A’nın kromatina erişimini engelleyebilir hem de onun yan yıkımını teşvik edebilir.
Atıf: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Anahtar kelimeler: SAGA kompleksi, KAT2A, protein kalite kontrolü, ubiquitin proteazom sistemi, kanser epigenetiği