Clear Sky Science · pl
Zakłócenie rdzenia SAGA wywołuje kolateralną degradację KAT2A
Kiedy maszyneria komórkowa się rozpada
W każdej komórce kluczowe zadania, takie jak włączanie i wyłączanie genów, wykonują wielkie molekularne maszyny zbudowane z wielu różnych białkowych części. W niniejszym badaniu przyjrzano się jednej z takich maszyn — kompleksowi SAGA, który wspiera aktywację genów i bywa wykorzystywany w nowotworach. Badacze odkryli, że uszkodzenie kluczowych elementów strukturalnych SAGA nie tylko osłabia maszynę — wywołuje selektywne zniszczenie jednego z jej głównych wykonawczych składników, białka nazwanego KAT2A, ujawniając ukrytą słabość, którą potencjalnie można wykorzystać terapeutycznie.
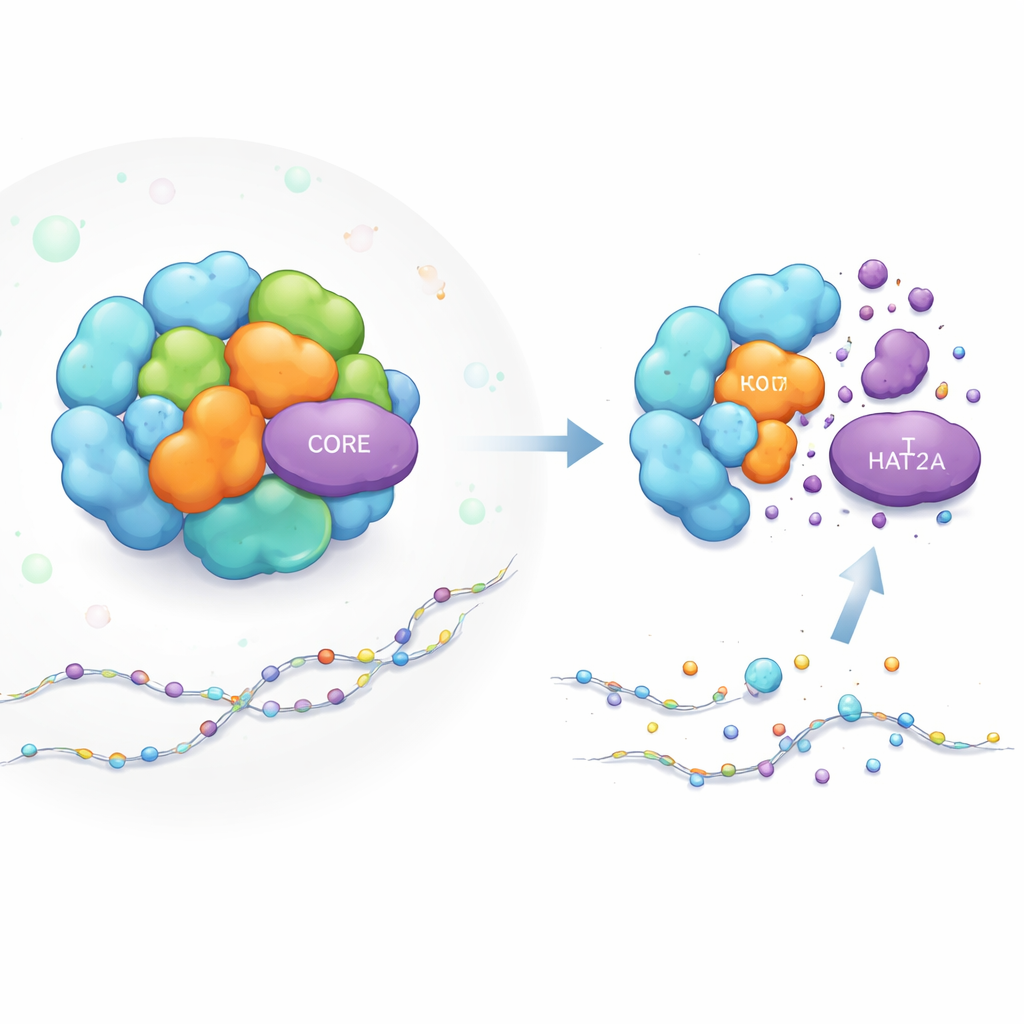
Jak zbudowana jest maszyna przełączająca geny
Kompleks SAGA przypomina modułowy warsztat do aktywacji genów. Niektóre części wykonują zadania chemiczne, na przykład dodają acetylowe „znaczniki” do białek histonowych (bębenków, na które nawinięte jest DNA), co ułatwia włączanie pobliskich genów. KAT2A jest wykonawcą dodającym te acetylacje w jednym z kluczowych modułów SAGA. Inne elementy SAGA pełnią funkcję rusztowania, nadając całej strukturze kształt i utrzymując moduły we właściwej pozycji względem DNA. Choć naukowcy wiedzieli dużo o funkcji SAGA, nie rozumieli, jak stabilność poszczególnych składników, takich jak KAT2A, jest utrzymywana w tym zatłoczonym, dynamicznym kompleksie.
Testy: co się dzieje po usunięciu elementów
Aby zbadać wewnętrzne działanie SAGA, autorzy skonstruowali fluorescencyjny reporter, który świeci proporcjonalnie do ilości KAT2A w żywych komórkach. Przy użyciu edycji genów CRISPR po kolei unieczynniali poszczególne składniki SAGA i obserwowali zmiany poziomu KAT2A. Usunięcie kilku sąsiednich partnerów w tym samym module acetylującym zmniejszało obfitość KAT2A, co było spodziewane. Zaskakująco jednak eliminacja określonego trio strukturalnych białek rdzeniowych — TADA1, TAF5L i TAF6L — również powodowała gwałtowny spadek białka KAT2A, mimo że te części nie przeprowadzają bezpośrednio reakcji chemicznych. Efekt obserwowano w różnych ludzkich typach komórek, w tym w komórkach białaczkowych, co sugeruje, że jest to cecha ogólna, a nie osobliwość konkretnej linii komórkowej.
Od złamanej struktury do utraty aktywności genów
Szczegółowa analiza molecularnych następstw wykazała, że utrata tych białek rdzeniowych robi więcej niż tylko obniża poziom KAT2A. Sam kompleks SAGA rozpada się, a moduł acetylacji odłącza się od większego zespołu. Po rozdzieleniu składników komórkowych według masy, KAT2A przesunął się z frakcji o wysokiej masie cząsteczkowej, reprezentujących nieuszkodzony SAGA, do lżejszych frakcji zgodnych z samotnym białkiem. Równocześnie KAT2A w dużej mierze zniknął z miejsc startu transkrypcji w całym genomie, a zwykłe acetylacje, które umieszcza na histonie H3 (w pozycji K9), zostały znacząco zredukowane. Co istotne, zaburzenie rdzenia zablokowało zwykłą kompensacyjną odpowiedź, w której pokrewne enzymy, jak KAT2B, mogą wyrównać straty, co pogłębia i utrudnia naprawę utraty acetylacji.
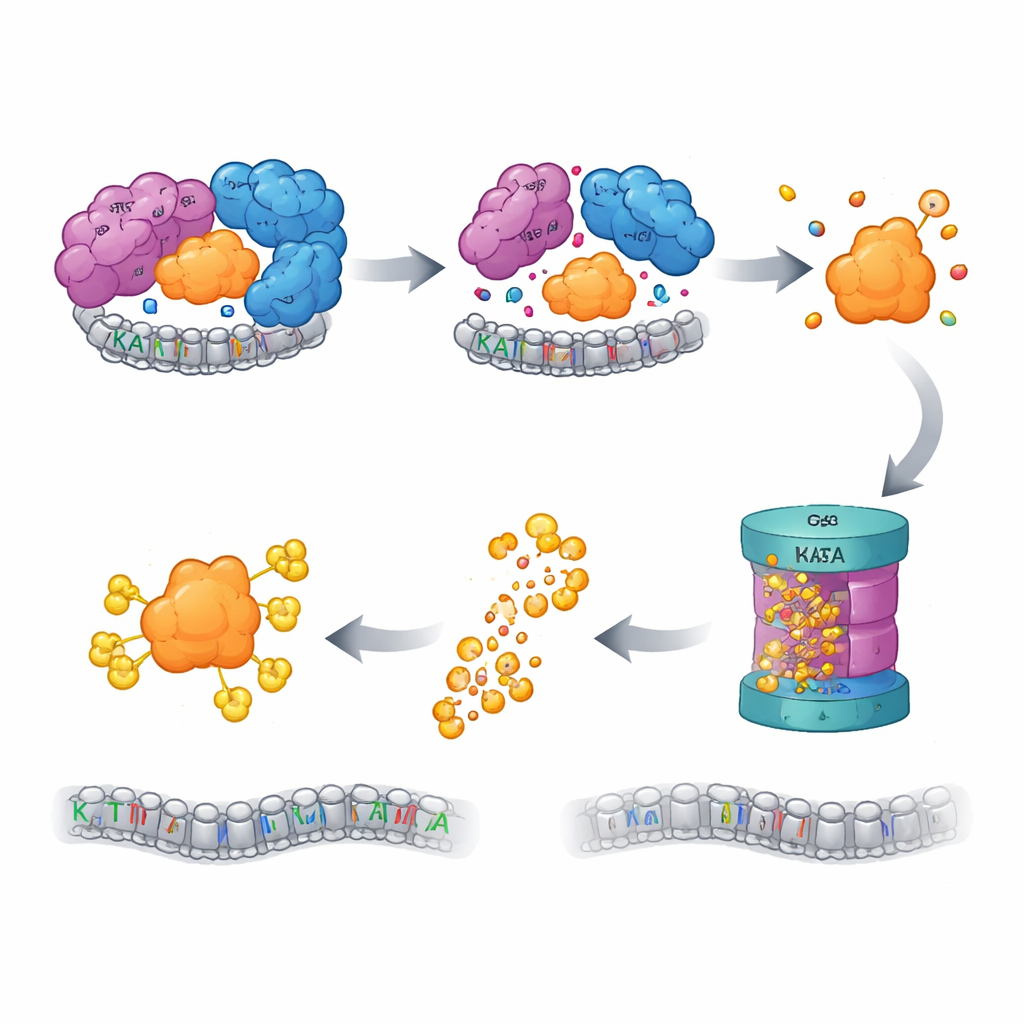
Kontrola jakości uruchamia niszczarkę
Komórki dysponują systemami kontroli jakości, które wykrywają „sierocie” białka — składniki, które straciły partnerów i grożą uszkodzeniem, jeżeli pozostaną niechronione i będą się źle fałdować lub agregować. Autorzy stwierdzili, że gdy rdzeń SAGA jest zaburzony, wolne KAT2A jest znakowane do zniszczenia przez system ubikwityna–proteasom, główną komórkową maszynerię do usuwania białek. Zablokowanie proteasomu lub wcześniejszych etapów tego kaskadowego znakowania przywracało poziomy KAT2A. Skoncentrowany screening CRISPR ponad tysiąca genów związanych z ubikwityną wskazał ligazę E3 o nazwie UBR5 wraz z jej enzymem deubikwitynującym OTUD5 jako kluczowych graczy w rozpoznawaniu i degradacji sierociego KAT2A. Co ciekawe, bliski kuzyn KAT2A — KAT2B — pozostawał stabilny w tych samych warunkach, a zmutowanie krótkiej sekwencji specyficznej dla KAT2A w pobliżu jego początku wystarczało, by uczynić białko bardziej odporne na degradację, identyfikując minimalny, paralogowo specyficzny „degron”, który oznacza KAT2A do usunięcia.
Ukryta słabość z obietnicą terapeutyczną
Podsumowując, praca pokazuje, że stabilność i aktywność KAT2A są ściśle związane z nienaruszoną architekturą kompleksu SAGA. Gdy tracone są strukturalne składniki rdzenia, SAGA się rozpada, KAT2A uwalnia się jako niechronione sierota, a układ nadzoru UBR5–OTUD5 szybko kieruje je do komórkowej niszczarki, zmniejszając ilość acetylowych znaczników aktywujących geny w całym genomie. Ponieważ KAT2A jest znaną słabością w kilku nowotworach, to wbudowane powiązanie między strukturą, montażem i selektywną degradacją sugeruje nową strategię: zamiast bezpośrednio celować w miejsce aktywne KAT2A, leki mogłyby destabilizować nieenzymatyczne białka rusztowania SAGA, jednocześnie blokując dostęp KAT2A do chromatyny i promując jego kolateralne zniszczenie.
Cytowanie: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Słowa kluczowe: Kompleks SAGA, KAT2A, kontrola jakości białek, system ubikwityna-proteasom, epigenetyka nowotworów