Clear Sky Science · he
שיבוש ליבת SAGA מושך אחריו דגרדציה משנית של KAT2A
כאשר מכונת התא מתפרקת
בתוך כל תא, משימות חיוניות כמו הפעלת וכיבוי גנים מבוצעות על ידי מכונות מולקולריות ענקיות הבנויות מרב־חלקים חלבוניים שונים. המחקר הזה בוחן אחת מכלי־העבודה האלה, קומפלקס שנקרא SAGA, שעוזר בהפעלת גנים ולעתים מנוצל בתהליכי סרטן. החוקרים גילו שאם פוגעים בחלקים המבניים המכריעים של SAGA, לא רק שמחלישים את המכונה — אלא גם מזרזים את ההשמדה הסלקטיבית של אחד הרכיבים העובדים המרכזיים שלה, חלבון שנקרא KAT2A, וחושפים חולשה נסתרת שאפשר לנצל תרופתית.
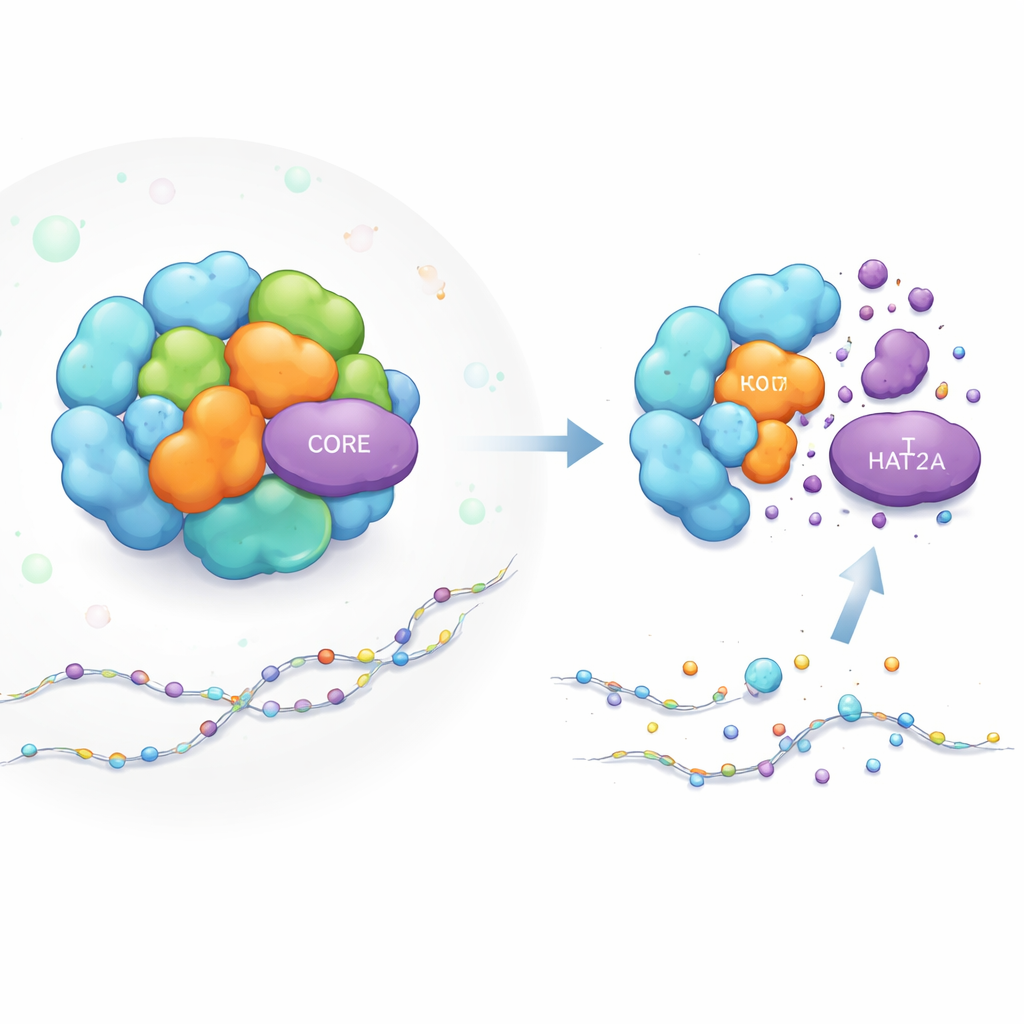
איך בנויה מכונת ההפעלה של גנים
קומפלקס SAGA דומה לסדנה מודולרית להפעלת גנים. חלקים מסוימים מבצעים משימות כימיות, כמו הוספת תגי אצטיל להיסטונים (הספוליות שעושות אריזה ל‑DNA), מה שמקל על הפעלת גנים סמוכים. KAT2A הוא העובד שמוסיף את האצטיל במודול מרכזי של SAGA. חלקים אחרים של SAGA מתפקדים יותר כמו שלד, נותנים לצבר כולו את צורתו ומחזיקים את המודולים במקום הנכון קרוב ל‑DNA. בעוד שמדענים ידעו רבות על תפקידי SAGA, לא היה ברור איך נשמר היציבות של רכיבים בודדים כמו KAT2A בתוך המכונה הצפופה והדינמית הזאת.
בוחנים מה קורה כשרוקנים חלקים
כדי לחקור את פעולת הפנים של SAGA, המחברים בנו דיווחן פלואורסנטי שזוהר ביחס לכמות KAT2A בתאים חיים. בעזרת עריכת גנים CRISPR הם השביתו כל רכיב של SAGA אחד‑אחד וצפו בשינויים ברמות KAT2A. הסרת מספר שותפים סמוכים באותו מודול האצטילציה הקטינה את שפע KAT2A, כפי שציפו. באופן מפתיע, השתקה של טריו מסוים של חלבוני ליבה מבניים — TADA1, TAF5L ו‑TAF6L — גם היא גרמה לירידה חדה בכמות חלבון KAT2A, אף על פי שחלקים אלה אינם מבצעים באופן ישיר תגובות כימיות. התופעה נצפתה בסוגי תאים אנושיים מרובים, כולל תאי לוקמיה, מה שמראה שמדובר בתכונה כללית ולא בקוצר דרך של קו תאים ספציפי.
ממבנה שבור לפעילות גנטית שאבדה
במבט מקרוב על התוצאות המולקולריות, הצוות הראה שאיבוד חלבוני הליבה עושה יותר מאשר רק להקטין את רמות KAT2A. קומפלקס SAGA עצמו מתפרק, ומודול האצטילציה מתנתק מההרכבה הגדולה. כאשר הפרידו רכיבים תאיים לפי גודל, KAT2A נדד ממקטעים כבדי־משקל מולקולרי, המייצגים SAGA שלם, אל מקטעים קלים יותר התואמים לחלבון יחיד. באותו זמן, KAT2A נעלם ברובו מאתרי תחילת ה‑DNA ברחבי הגנום, וסימני האצטיל הרגילים שהוא משים על היסטון H3 (במיקום הנקרא K9) ירדו באופן משמעותי. חשוב לציין, ששיבוש הליבה חסם את תגובת הגיבוי הרגילה שבה אנזים קרוב, KAT2B, יכול לפצות, מה שהעמיק את אובדן האצטילציה והקשה על התא לתקן זאת.
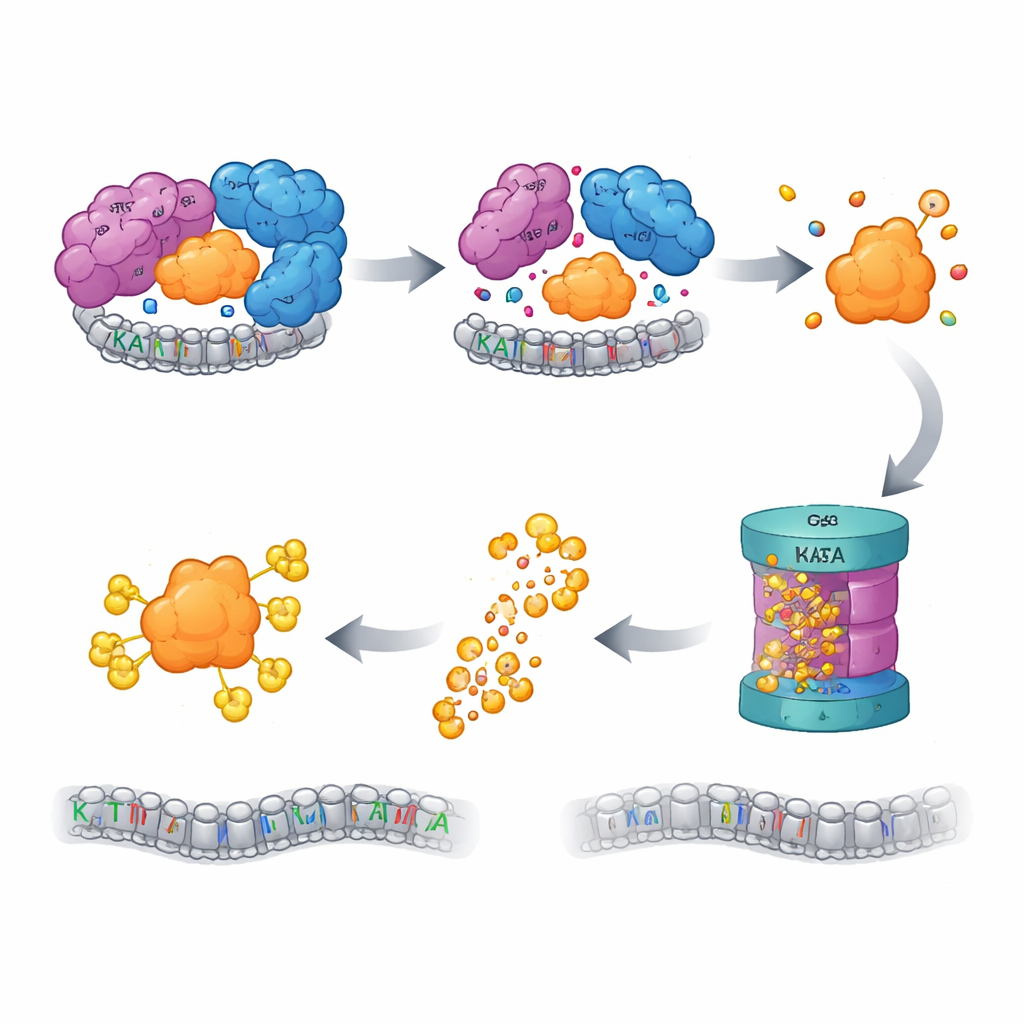
בקרת איכות מפעילה את המגרסה
לתאים יש מערכות בקרת איכות שמנטרות חלבונים "יתומים" — מרכיבים שאיבדו את שותפיהם וסכנתם לטעון נזק אם יתקמטו או יצברו. המחברים גילו שכאשר ליבת SAGA מופרעת, KAT2A החופשי מתוייג להשמדה על‑ידי מערכת היוביקוויטין–פרוטאזום, מכונת ההשמדת החלבונים המרכזית של התא. חסימת הפרוטאזום, או שלבים מוקדמים יותר בשרשרת התייגות זו, החזירה את רמות KAT2A. מסך CRISPR ממוקד על יותר מאלף גנים הקשורים ליוביקוויטין זיהה ליגאז E3 בשם UBR5, יחד עם דה‑יוביקוויטינאז העוזר לו OTUD5, כשחקנים מרכזיים בזיהוי ובהשמדת KAT2A היתום. באופן מעניין, בן דודו הקרוב של KAT2A, KAT2B, נשאר יציב באותן תנאים, ומוטציה ברצף קצר, ספציפי ל‑KAT2A בקרבת ההתחלה שלו, הספיקה להפוך את החלבון לעמיד יותר להשמדה, וזיהתה "דגרון" מינימלי וספציפי לפראלוג שמסמן את KAT2A להשמדה.
חולשה נסתרת עם הבטחה תרופתית
בסך הכל, המחקר ממחיש ששימור יציבותו ופעילותו של KAT2A קשור בחוזקה לאדריכלות השלמה של קומפלקס SAGA. כשחלקים מבניים בליבה נעלמים, SAGA מתפרק, KAT2A משתחרר כיתום חשוף, ומערכת הפיקוח UBR5–OTUD5 מנווטת במהירות להשמדתו בפרוטאזום התאי, מה שמפחית את סימני האצטיל הפעילים על הגנום כולו. מכיוון ש‑KAT2A מהווה נקודת תורפה מוכרת בכמה סוגי סרטן, הקישור המובנה הזה בין מבנה, הרכבה ודגרדציה סלקטיבית מציע אסטרטגיה חדשה: במקום לכוון ישירות לאתר הפעיל של KAT2A, ניתן לפתח תרופות שיפגעו בחלבוני השלד הלא‑אנזימטיים של SAGA, ובמקביל יחסמו את גישת KAT2A לכרומטין ויעודדו את השמדתו המשנית.
ציטוט: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
מילות מפתח: מולטי־קומפלקס SAGA, KAT2A, בקרת איכות חלבונים, מערכת יוביקוויטין־פרוטאזום, אפיגנטיקה סרטנית