Clear Sky Science · de
Störung des SAGA-CORE löst die kollaterale Degradation von KAT2A aus
Wenn die zelluläre Maschinerie auseinanderfällt
In jeder Zelle übernehmen riesige molekulare Maschinen, die aus vielen verschiedenen Proteinteilen bestehen, lebenswichtige Aufgaben wie das Ein- und Ausschalten von Genen. Diese Studie untersucht eine solche Maschine, den SAGA-Komplex, der die Genaktivierung unterstützt und bei Krebs häufig missbraucht wird. Die Forschenden stellten fest, dass das Beschädigen zentraler Strukturbauteile des SAGA nicht nur die Maschine schwächt – es löst auch die selektive Zerstörung eines ihrer wichtigsten Funktionsteile, des Proteins KAT2A, aus und macht damit eine verborgene Verwundbarkeit sichtbar, die pharmakologisch nutzbar sein könnte.
Wie eine Gen-Schaltmaschine aufgebaut ist
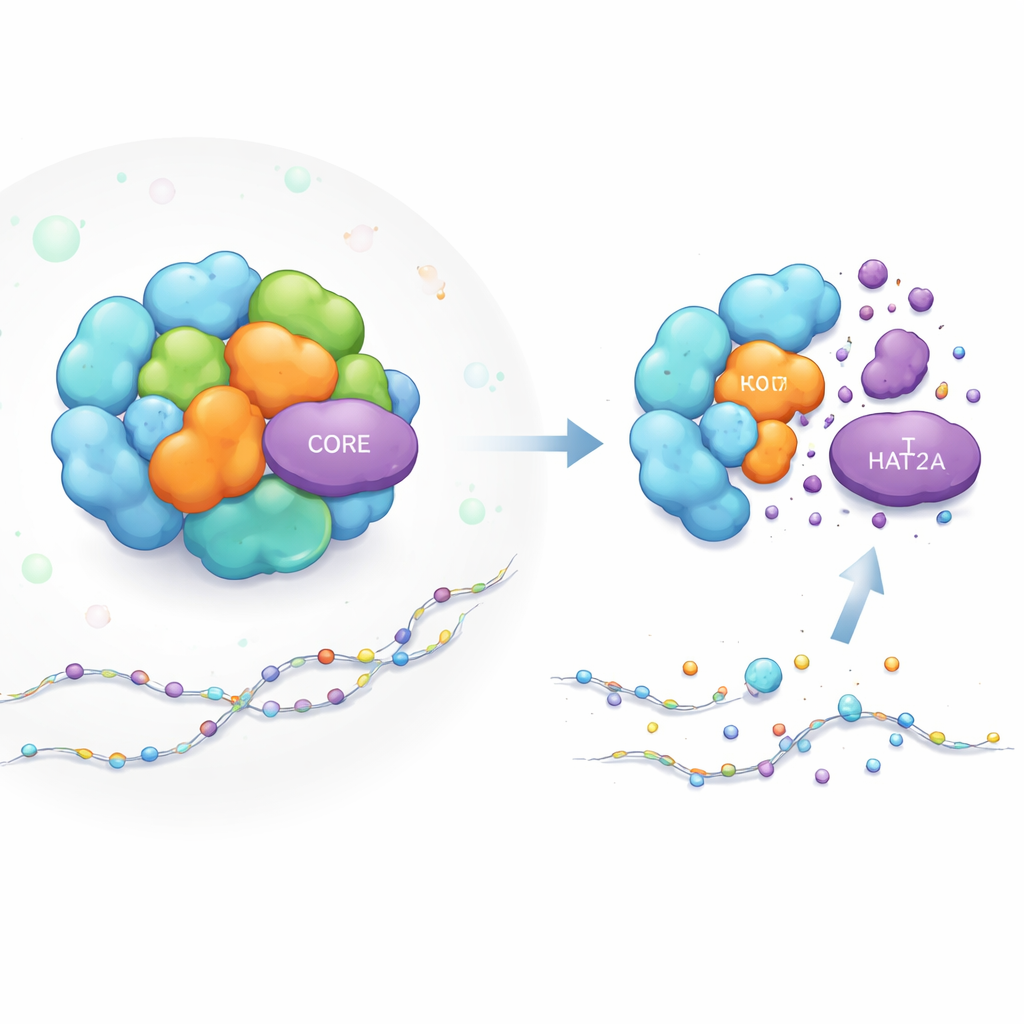
Der SAGA-Komplex ist wie eine modulare Werkstatt zur Genaktivierung. Einige Teile führen chemische Aufgaben aus, etwa das Anbringen von Acetyl‑„Markern“ an Histonproteinen (den Spulen, die die DNA verpacken), was Gene in der Nähe leichter aktivierbar macht. KAT2A ist der Acetyl‑Anfüger in einem der wichtigen SAGA‑Module. Andere SAGA‑Teile wirken eher wie ein Gerüst, sie geben der ganzen Struktur Form und positionieren die Module in der richtigen Nähe zur DNA. Während Forschende bereits viel über die Funktion von SAGA wussten, blieb unklar, wie die Stabilität einzelner Komponenten wie KAT2A innerhalb dieser dicht gepackten, dynamischen Maschine aufrechterhalten wird.
Was passiert, wenn Teile entfernt werden
Um die inneren Abläufe von SAGA zu untersuchen, entwickelten die Autorinnen und Autoren einen fluoreszenten Reporter, der proportional zur Menge an KAT2A in lebenden Zellen aufleuchtet. Mit CRISPR‑Geneditierung schalteten sie nacheinander jede SAGA‑Komponente aus und beobachteten, wie sich die KAT2A‑Spiegel veränderten. Das Entfernen mehrerer benachbarter Partner im selben Acetylierungsmodul verringerte erwartungsgemäß die KAT2A‑Menge. Überraschenderweise führte die Deletion eines spezifischen Trios struktureller CORE‑Proteine — TADA1, TAF5L und TAF6L — ebenfalls zu einem starken Abfall des KAT2A‑Proteins, obwohl diese Teile keine direkten chemischen Reaktionen ausführen. Dieser Effekt zeigte sich in mehreren menschlichen Zelltypen, einschließlich Leukämiezellen, was darauf hinweist, dass es sich um ein allgemeines Merkmal und nicht um eine Besonderheit einer Zelllinie handelt.
Von gebrochener Struktur zu verlorener Genaktivität
Bei näherer Betrachtung der molekularen Folgen zeigte das Team, dass der Verlust dieser CORE‑Proteine mehr bewirkt als nur eine Reduktion der KAT2A‑Menge. Der SAGA‑Komplex zerfällt, und das Acetylierungsmodul löst sich von der größeren Assemblierung. Bei der Fraktionierung zellulärer Komponenten nach Größe wanderte KAT2A von hochmolekularen Fraktionen, die intaktes SAGA repräsentieren, in leichtere Fraktionen, die einem einzelnen Protein entsprechen. Gleichzeitig verschwand KAT2A weitgehend von Genstartstellen im gesamten Genom, und die üblichen Acetylmarken, die es an Histon H3 anbringt (an der Position K9), waren deutlich vermindert. Wichtig ist, dass die Störung des CORE die übliche Backup‑Antwort blockierte, bei der ein verwandtes Enzym, KAT2B, kompensieren kann, sodass der Verlust der Acetylierung ausgeprägter und für die Zelle schwerer zu reparieren war.
Die Qualitätskontrolle schaltet den Schredder ein
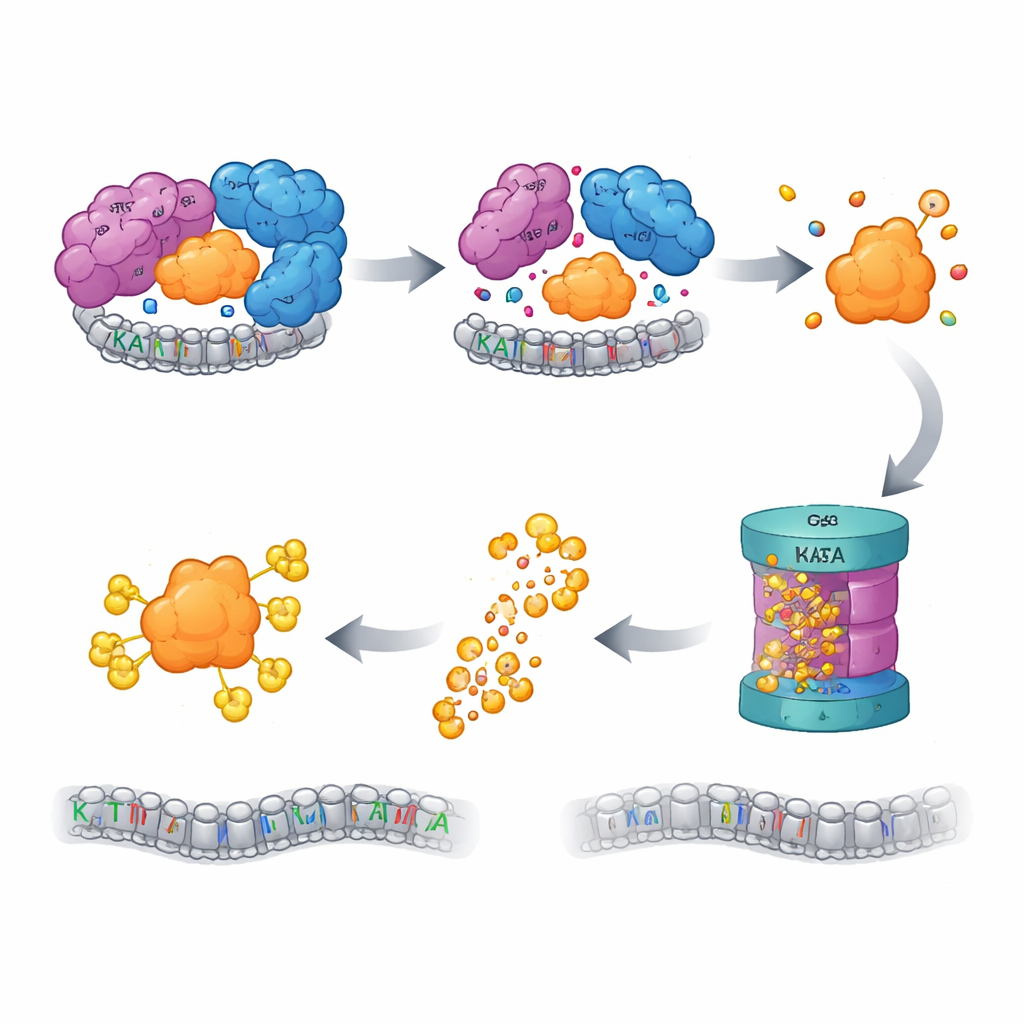
Zellen verfügen über Qualitätskontrollsysteme, die nach „verwaisten“ Proteinen Ausschau halten — Komponenten, die ihre Partner verloren haben und Gefahr laufen, fehlzufalten oder zu verklumpen, wenn man sie unbeaufsichtigt lässt. Die Autorinnen und Autoren fanden heraus, dass bei Störung des SAGA‑CORE freies KAT2A für die Zerstörung durch das Ubiquitin‑Proteasom‑System markiert wird, die zentrale Protein‑Entsorgungsmaschinerie der Zelle. Das Blockieren des Proteasoms oder früherer Schritte in dieser Markierungskaskade stellte die KAT2A‑Spiegel wieder her. Ein gezielter CRISPR‑Screen von mehr als tausend ubiquitinbezogenen Genen identifizierte eine E3‑Ligase namens UBR5 zusammen mit ihrer Helfer‑Deubiquitinase OTUD5 als Schlüsselfaktoren bei der Erkennung und dem Abbau von verwaistem KAT2A. Interessanterweise blieb KAT2A’s naher Verwandter KAT2B unter denselben Bedingungen stabil, und die Mutation einer kurzen, KAT2A‑spezifischen Sequenz nahe dem N‑Termin reichte aus, um das Protein widerstandsfähiger gegen Abbau zu machen — ein minimaler, paralogue‑spezifischer „Degron“, der KAT2A zur Entsorgung markiert.
Eine verborgene Schwäche mit therapeutischem Potenzial
Insgesamt zeigt die Arbeit, dass die Stabilität und Aktivität von KAT2A eng an die intakte Architektur des SAGA‑Komplexes gebunden ist. Gehen strukturelle CORE‑Komponenten verloren, zerfällt SAGA, KAT2A wird als ungeschütztes Waisenkind freigesetzt und das UBR5–OTUD5‑Überwachungssystem leitet es rasch zum zellulären Schredder, wodurch die genaktivierenden Acetylmarken im gesamten Genom reduziert werden. Da KAT2A in mehreren Krebsarten eine bekannte Verwundbarkeit darstellt, deutet diese eingebaute Verbindung zwischen Struktur, Assemblierung und selektiver Degradation auf eine neue Strategie hin: Anstatt direkt die aktive Stelle von KAT2A anzugreifen, könnten Medikamente nicht‑enzymatische SAGA‑Gerüstproteine destabilisieren, KAT2As Zugang zu Chromatin blockieren und gleichzeitig dessen kollateralen Abbau fördern.
Zitation: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Schlüsselwörter: SAGA-Komplex, KAT2A, Protein-Qualitätskontrolle, Ubiquitin-Proteasom-System, Krebs-Epigenetik