Clear Sky Science · pt
Destruição do CORE do SAGA provoca degradação colateral de KAT2A
Quando a Máquina Celular Desmorona
Dentro de cada célula, funções essenciais como ligar e desligar genes são desempenhadas por enormes máquinas moleculares formadas por muitas peças proteicas diferentes. Este estudo examina uma dessas máquinas, chamada complexo SAGA, que ajuda a ativar genes e frequentemente é sequestrada no câncer. Os pesquisadores descobriram que, se você danificar peças estruturais chave do SAGA, não apenas enfraquece a máquina — você desencadeia a destruição seletiva de uma de suas principais unidades de trabalho, uma proteína chamada KAT2A, revelando uma vulnerabilidade oculta que fármacos poderiam potencialmente explorar.
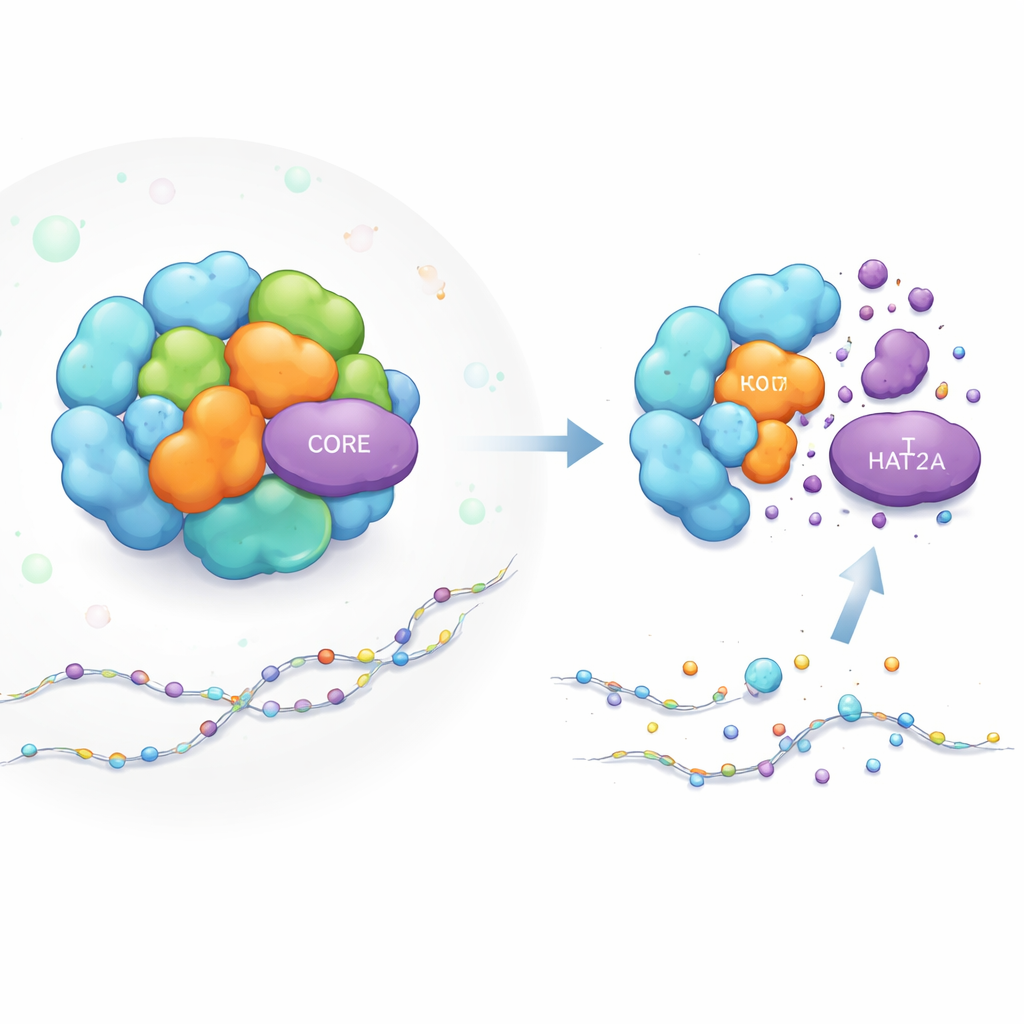
Como uma Máquina de Comutação de Genes é Montada
O complexo SAGA funciona como uma oficina modular para ativação gênica. Algumas partes realizam tarefas químicas, como adicionar “etiquetas” de acetil às histonas (os carretéis que organizam o DNA), o que facilita a ativação de genes próximos. KAT2A é o trabalhador que adiciona essas acetilações em um dos módulos chave do SAGA. Outras partes do SAGA atuam mais como andaimes, conferindo forma à estrutura e mantendo os módulos na posição correta junto ao DNA. Embora os cientistas soubessem muito sobre o que o SAGA faz, não entendiam como a estabilidade de componentes individuais como KAT2A é mantida dentro dessa máquina densa e dinâmica.
Testando o que Acontece Quando Peças São Removidas
Para sondar o funcionamento interno do SAGA, os autores construíram um repórter fluorescente que brilha em proporção à quantidade de KAT2A em células vivas. Usando edição gênica CRISPR, eliminaram cada componente do SAGA um por um e observaram como os níveis de KAT2A mudavam. A remoção de vários parceiros próximos no mesmo módulo de acetilação reduziu a abundância de KAT2A, como esperado. Surpreendentemente, a degradação de um trio específico de proteínas estruturais do CORE — TADA1, TAF5L e TAF6L — também fez com que a proteína KAT2A caísse abruptamente, mesmo que essas partes não realizem reações químicas diretamente. O efeito foi observado em vários tipos de células humanas, incluindo células de leucemia, mostrando que é uma característica geral e não uma peculiaridade de uma linhagem celular.
De Estrutura Quebrada à Perda de Atividade Gênica
Ao examinar mais de perto as consequências moleculares, a equipe mostrou que a perda dessas proteínas do CORE faz mais do que simplesmente reduzir os níveis de KAT2A. O próprio complexo SAGA se desmantela, e o módulo de acetilação se desacopla da montagem maior. Quando separaram componentes celulares por tamanho, KAT2A deslocou-se de frações de alto peso molecular, representando o SAGA intacto, para frações mais leves compatíveis com a proteína solitária. Ao mesmo tempo, KAT2A praticamente desapareceu dos sítios de início de genes em todo o genoma, e as marcas usuais de acetilação que ela coloca na histona H3 (na posição chamada K9) foram substancialmente reduzidas. Importante, a disrupção do CORE bloqueou a resposta de reserva habitual em que uma enzima relacionada, KAT2B, pode compensar, tornando a perda de acetilação mais profunda e mais difícil de reparar pela célula.
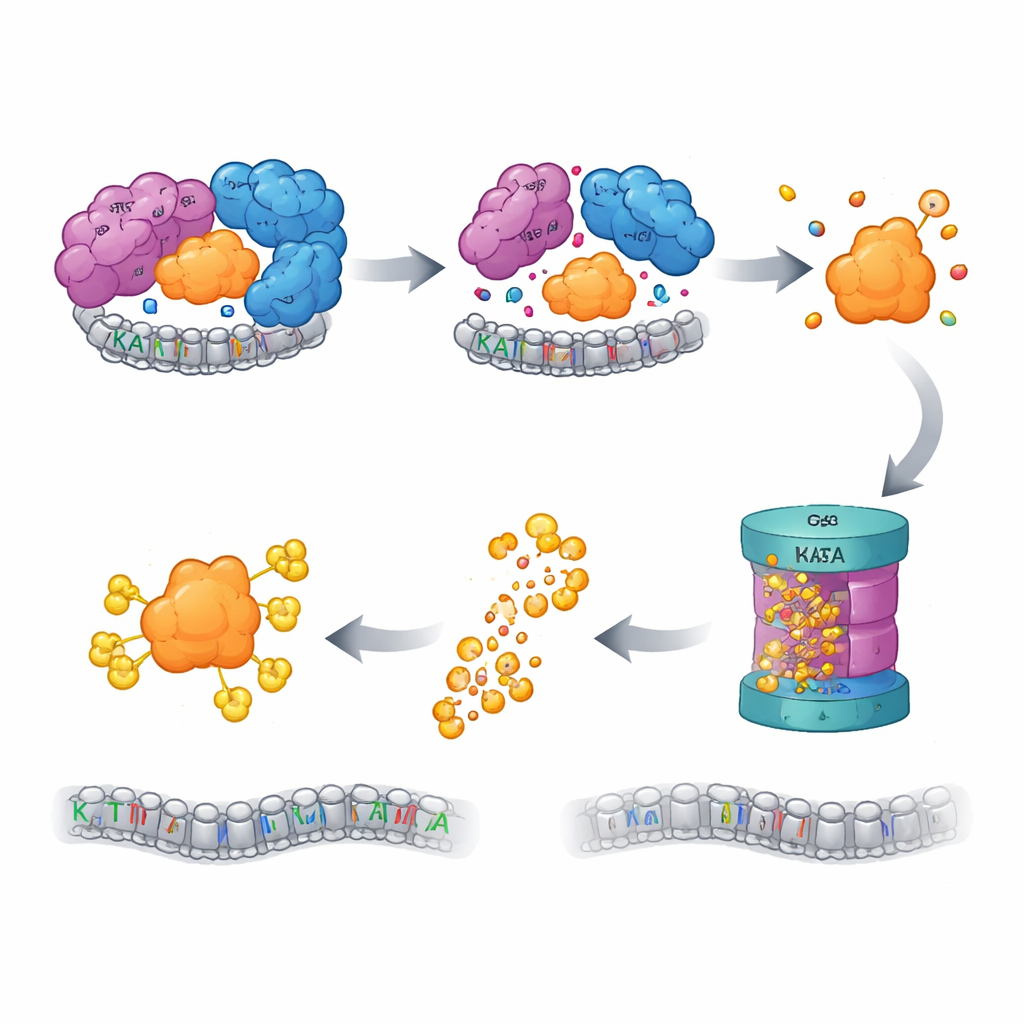
O Controle de Qualidade Aciona o Triturador
As células possuem sistemas de controle de qualidade que vigiam por proteínas “órfãs” — componentes que perderam seus parceiros e correm o risco de causar danos se ficarem desnaturadas ou agregarem. Os autores descobriram que, quando o CORE do SAGA é interrompido, a KAT2A livre é marcada para destruição pelo sistema ubiquitina–proteassoma, a principal máquina de eliminação de proteínas da célula. Bloquear o proteassoma, ou etapas anteriores nessa cascata de marcação, restaurou os níveis de KAT2A. Uma triagem CRISPR focada em mais de mil genes relacionados à ubiquitina identificou uma E3 ligase chamada UBR5, juntamente com sua desubiquitinase auxiliar OTUD5, como peças-chave no reconhecimento e degradação da KAT2A órfã. Curiosamente, a parente próxima KAT2B permaneceu estável nas mesmas condições, e mutar uma curta sequência específica de KAT2A perto de sua extremidade inicial foi suficiente para tornar a proteína mais resistente à destruição, identificando um “degron” minimal e específico de paralog que marca KAT2A para eliminação.
Uma Vulnerabilidade Oculta com Potencial Terapêutico
No conjunto, o trabalho mostra que a estabilidade e a atividade de KAT2A estão intimamente ligadas à arquitetura intacta do complexo SAGA. Quando componentes estruturais do CORE são perdidos, o SAGA se desassocia, KAT2A é liberada como uma órfã desprotegida, e o sistema de vigilância UBR5–OTUD5 rapidamente a direciona ao triturador celular, reduzindo marcas de acetilação que ativam genes por todo o genoma. Como KAT2A é uma vulnerabilidade conhecida em vários tipos de câncer, essa ligação intrínseca entre estrutura, montagem e degradação seletiva sugere uma nova estratégia: em vez de mirar diretamente no sítio ativo de KAT2A, fármacos poderiam desestabilizar proteínas de andaime não enzimáticas do SAGA, bloqueando simultaneamente o acesso de KAT2A à cromatina e promovendo sua destruição colateral.
Citação: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Palavras-chave: complexo SAGA, KAT2A, controle de qualidade de proteínas, sistema ubiquitina-proteassoma, epigenética do câncer