Clear Sky Science · nl
Ontregeling van de SAGA-CORE veroorzaakt collaterale afbraak van KAT2A
Als de celmachines uit elkaar vallen
In elke cel voeren grote moleculaire machines, opgebouwd uit veel verschillende eiwitonderdelen, essentiële taken uit, zoals het aan- en uitzetten van genen. Deze studie onderzoekt een van die machines, het SAGA-complex, dat helpt bij genactivatie en vaak door kanker wordt gekaapt. De onderzoekers ontdekten dat wanneer je sleutelstructuurelementen van SAGA beschadigt, je niet alleen de machine verzwakt, maar ook de selectieve vernietiging van een van zijn belangrijkste werkende onderdelen veroorzaakt: een eiwit genaamd KAT2A. Dit onthult een verborgen zwakte die mogelijk door geneesmiddelen kan worden benut.
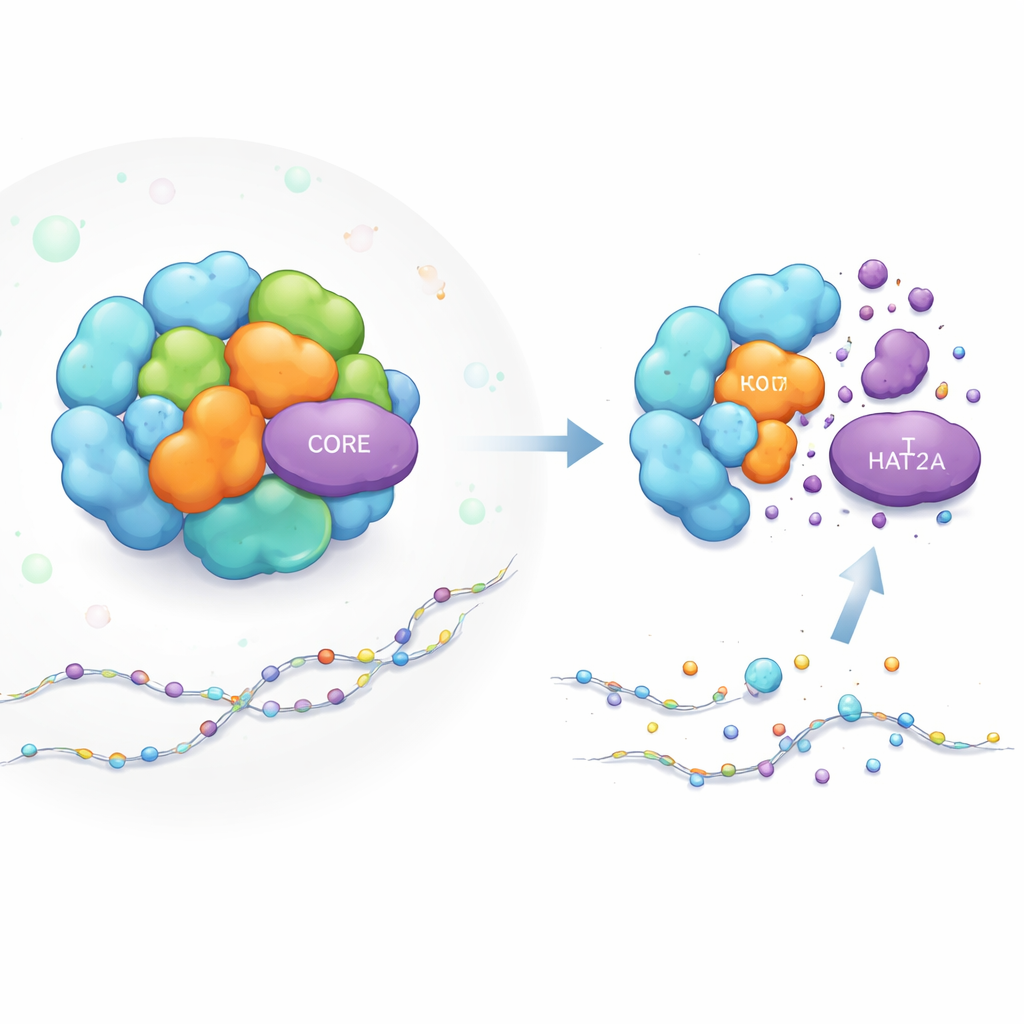
Hoe een genschakelmachine is opgebouwd
Het SAGA-complex werkt als een modulaire werkplaats voor genactivatie. Sommige onderdelen voeren chemische taken uit, zoals het toevoegen van acetyl-“labels” aan histonen (de spoelen die DNA verpakken), wat het makkelijker maakt om nabijgelegen genen aan te zetten. KAT2A is de acetyltoevoegende werker in één van SAGA’s belangrijke modules. Andere SAGA-onderdelen fungeren meer als steigers die de hele structuur vormgeven en de modules op de juiste plek bij het DNA houden. Hoewel wetenschappers veel wisten over wat SAGA doet, begrepen ze niet hoe de stabiliteit van individuele componenten zoals KAT2A in deze drukke, dynamische machine wordt gehandhaafd.
Onderzoeken wat er gebeurt als onderdelen worden verwijderd
Om de binnenkant van SAGA te onderzoeken, bouwden de auteurs een fluorescente reporter die oplicht in verhouding tot de hoeveelheid KAT2A in levende cellen. Met CRISPR-genbewerking schakelden ze elk SAGA-onderdeel een voor een uit en volgden hoe de KAT2A-niveaus veranderden. Het verwijderen van meerdere nabije partners in dezelfde acetylatiemodule verminderde de hoeveelheid KAT2A, zoals verwacht. Verrassend genoeg leidde het uitschakelen van een specifiek trio structurele CORE-eiwitten—TADA1, TAF5L en TAF6L—ook tot een sterke daling van KAT2A-eiwit, hoewel deze delen geen directe chemische reacties uitvoeren. Het effect werd gezien in meerdere menselijke celtypen, waaronder leukemiecellen, wat aantoont dat het een algemeen kenmerk is en geen eigenaardigheid van één cellijn.
Van gebroken structuur naar verloren genactiviteit
Door de moleculaire nasleep nauwkeuriger te onderzoeken, liet het team zien dat het verlies van deze CORE-eiwitten meer doet dan alleen KAT2A-niveaus verlagen. Het SAGA-complex valt zelf uiteen en de acetylatiemodule scheidt zich van het grotere complex. Toen ze cellulaire componenten naar grootte scheidden, verschoof KAT2A van hoogmoleculaire fracties, die intact SAGA vertegenwoordigen, naar lichtere fracties die overeenkomen met losstaand eiwit. Tegelijkertijd verdween KAT2A grotendeels van DNA-startplaatsen in het hele genoom en werden de gebruikelijke acetylmerken die het aan histon H3 zet (op een positie genoemd K9) aanzienlijk verminderd. Belangrijk is dat het ontregelen van de CORE de gebruikelijke back-upreactie blokkeerde waarbij een verwant enzym, KAT2B, kan compenseren, waardoor het verlies van acetylatie dieper en moeilijker voor de cel herstelbaar werd.
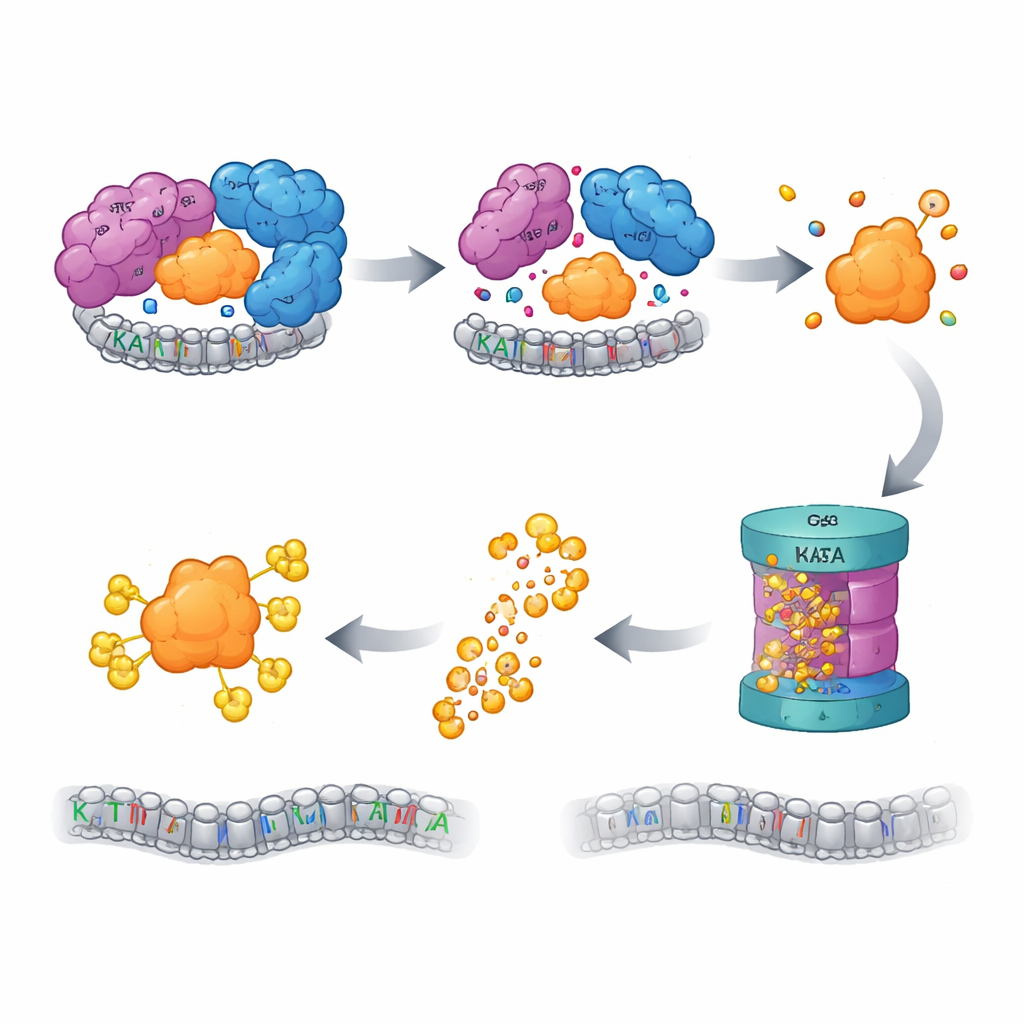
Kwaliteitscontrole schakelt de versnipperaar in
Cellen beschikken over kwaliteitscontroledystemen die letten op “wees”-eiwitten—componenten die hun partners hebben verloren en, als ze worden achtergelaten, risico lopen verkeerd op te vouwen of samen te klonteren. De auteurs vonden dat wanneer de SAGA-CORE wordt verstoord, vrijgekomen KAT2A wordt gemarkeerd voor vernietiging door het ubiquitine–proteasoomsysteem, het belangrijkste eiwitverwijderingssysteem van de cel. Het blokkeren van het proteasoom, of eerdere stappen in deze merkcyclus, herstelde de KAT2A-niveaus. Een gerichte CRISPR-screen van meer dan duizend ubiquitine-gerelateerde genen identificeerde een E3-ligase genaamd UBR5, samen met zijn hulpende deubiquitinase OTUD5, als sleutelspelers in het herkennen en afbreken van weeskind-KAT2A. Intrigerend genoeg bleef KAT2A’s nauwe verwant KAT2B onder dezelfde omstandigheden stabiel, en het muteren van een korte, KAT2A-specifieke sequentie nabij het begin maakte het eiwit al weerbaarder tegen vernietiging. Daarmee werd een minimaal, paraloge-specifiek “degron” geïdentificeerd dat KAT2A markeert voor afvoer.
Een verborgen zwakte met therapeutische belofte
Al met al toont dit werk aan dat de stabiliteit en activiteit van KAT2A nauw verbonden zijn met de intacte architectuur van het SAGA-complex. Wanneer structurele CORE-componenten verloren gaan, valt SAGA uiteen, komt KAT2A vrij als een onbeschermd wees en leidt het UBR5–OTUD5-surveillancesysteem het snel naar de cellulair versnipperaar, waardoor genactiverende acetylmerken in het hele genoom verminderen. Omdat KAT2A een bekende kwetsbaarheid is in meerdere vormen van kanker, suggereert deze ingebouwde koppeling tussen structuur, assemblage en selectieve afbraak een nieuwe strategie: in plaats van KAT2A’s actieve plaats direct te remmen, zouden geneesmiddelen niet-enzymatische SAGA-steigereiwitten kunnen destabiliseren, waardoor KAT2A’s toegang tot chromatine wordt geblokkeerd en tegelijk zijn collaterale afbraak wordt bevorderd.
Bronvermelding: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Trefwoorden: SAGA-complex, KAT2A, eiwitkwaliteitscontrole, ubiquitine-proteasoomsysteem, kanker-epigenetica