Clear Sky Science · ru
Нарушение CORE-компонента SAGA вызывает сопутствующую деградацию KAT2A
Когда клеточный механизм распадается
Внутри каждой клетки важные функции, такие как включение и выключение генов, выполняют гигантские молекулярные машины, собранные из множества различных белковых компонентов. В этом исследовании рассматривается одна такая машина, называемая комплексом SAGA, который помогает активировать гены и часто используется в корыстных целях при раке. Исследователи обнаружили, что при повреждении ключевых структурных частей SAGA вы не просто ослабляете машину — вы запускаете селективное уничтожение одного из её основных рабочих звеньев, белка KAT2A, что выявляет скрытую уязвимость, которую потенциально можно использовать лекарствами.
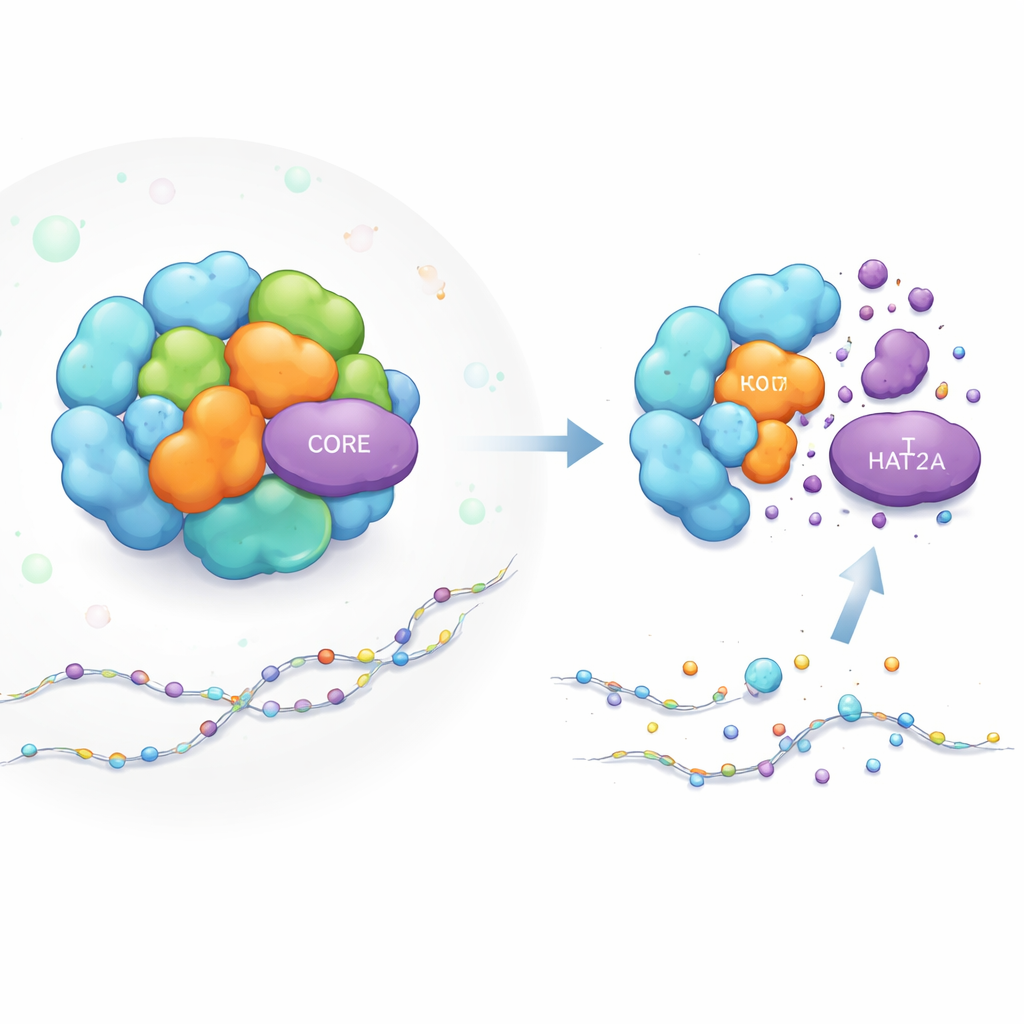
Как устроена машина переключения генов
Комплекс SAGA подобен модульной мастерской для активации генов. Некоторые части выполняют химические задачи, например добавляют ацетильные «метки» на гистоны (катушки, в которые упакована ДНК), что облегчает включение соседних генов. KAT2A — это «работник», добавляющий ацетильные метки в одном из ключевых модулей SAGA. Другие компоненты SAGA выполняют роль каркаса, придавая всей структуре форму и удерживая модули в нужном положении рядом с ДНК. Хотя учёным было многое известно о функциях SAGA, оставалось непонятным, как обеспечивается стабильность отдельных компонентов, таких как KAT2A, внутри этого плотного и динамичного комплекса.
Проверка того, что происходит при удалении частей
Чтобы исследовать внутреннее устройство SAGA, авторы построили флуоресцентный репортер, который светится в зависимости от количества KAT2A в живых клетках. С помощью редактирования генома CRISPR они поочерёдно выводили из строя каждый компонент SAGA и наблюдали за изменением уровня KAT2A. Удаление нескольких соседних партнёров в том же ацетилирующем модуле снизило количество KAT2A, как и ожидалось. Однако неожиданно вывод из строя конкретного трио структурных CORE-белков — TADA1, TAF5L и TAF6L — также резко уменьшал содержание белка KAT2A, хотя эти компоненты напрямую не выполняют химические реакции. Эффект наблюдали в нескольких типах человеческих клеток, включая клетки лейкемии, что указывает на общую закономерность, а не на уникальность одной клеточной линии.
От разрушенной структуры к утрате активности генов
При более детальном анализе молекулярных последствий команда показала, что потеря этих CORE-белков влечёт за собой не просто снижение уровня KAT2A. Сам комплекс SAGA распадается, и ацетилирующий модуль отсоединяется от большей сборки. При разделении клеточных компонентов по размеру KAT2A смещался из фракций с высокой молекулярной массой, соответствующих целому комплексу SAGA, в более лёгкие фракции, характерные для свободного белка. Одновременно KAT2A в значительной степени исчезал со стартовых сайтов транскрипции по всему геному, а обычные ацетильные метки, которые он наносит на гистон H3 (в позиции K9), значительно уменьшались. Важно, что разрушение CORE блокировало обычный компенсаторный ответ, при котором родственный фермент KAT2B мог бы заменить функцию KAT2A, что делает утрату ацетилирования более глубокой и труднее восстановимой для клетки.
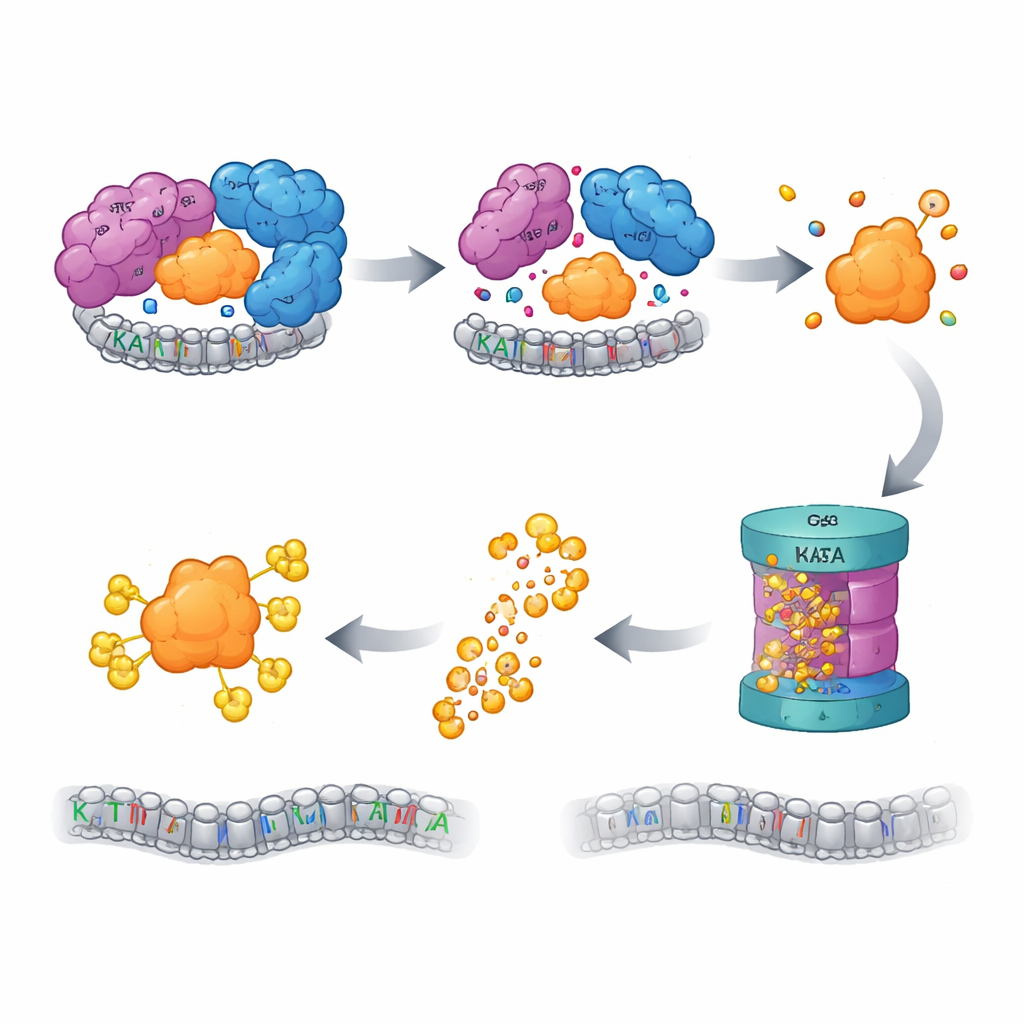
Система контроля качества включает утилизацию
Клетки располагают системами контроля качества, которые отслеживают «сиротские» белки — компоненты, потерявшие партнёров и рискующие причинить вред, если остаться незащищёнными и неправильно свернуться или агрегироваться. Авторы обнаружили, что при нарушении CORE SAGA свободный KAT2A помечается для разрушения системой убиквитин–протеасома, основной системой утилизации белков в клетке. Блокирование протеасомы или более ранних шагов этой маркирующей каскады восстанавливало уровни KAT2A. Целенаправлённый CRISPR-скрин более чем тысячи генов, связанных с убиквитинированием, указал на лигазу E3 под названием UBR5 и её вспомогательную декаббаку OTUD5 как ключевых участников в распознавании и деградации «сиротского» KAT2A. Любопытно, что близкий родственник KAT2A — KAT2B — оставался стабильным при тех же условиях, и мутация короткой последовательности, специфичной для KAT2A вблизи начала белка, оказалась достаточной, чтобы сделать белок более устойчивым к разрушению, что позволило выделить минимальный, паралог-специфичный «дегрон», помечающий KAT2A для утилизации.
Скрытая уязвимость с терапевтическим потенциалом
В целом работа показывает, что стабильность и активность KAT2A тесно связаны с целостной архитектурой комплекса SAGA. Когда теряются структурные CORE-компоненты, SAGA разрушается, KAT2A оказывается в состоянии незашищённого «сирака», и система наблюдения UBR5–OTUD5 быстро направляет его в клеточный шредер, снижая уровень ацетильных меток по всему геному. Поскольку KAT2A известен как уязвимость в нескольких типах рака, эта внутренняя связь между структурой, сборкой и селективной деградацией предлагает новую стратегию: вместо прямого нацеливания на активный центр KAT2A, препараты могли бы дестабилизировать неферментативные каркасные белки SAGA, одновременно блокируя доступ KAT2A к хроматину и способствуя его сопутствующей деградации.
Цитирование: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Ключевые слова: комплекс SAGA, KAT2A, контроль качества белков, система убиквитин-протеасома, эпигенетика рака