Clear Sky Science · es
La alteración del CORE de SAGA desencadena la degradación colateral de KAT2A
Cuando la maquinaria celular se descompone
Dentro de cada célula, tareas esenciales como activar o desactivar genes las llevan a cabo enormes máquinas moleculares formadas por muchas piezas proteicas distintas. Este estudio examina una de esas máquinas, llamada complejo SAGA, que ayuda a activar genes y que con frecuencia es secuestrada en el cáncer. Los investigadores descubrieron que si se dañan piezas estructurales clave de SAGA, no solo se debilita la máquina: se desencadena la destrucción selectiva de una de sus principales piezas funcionales, una proteína llamada KAT2A, lo que revela una vulnerabilidad oculta que los fármacos podrían aprovechar.
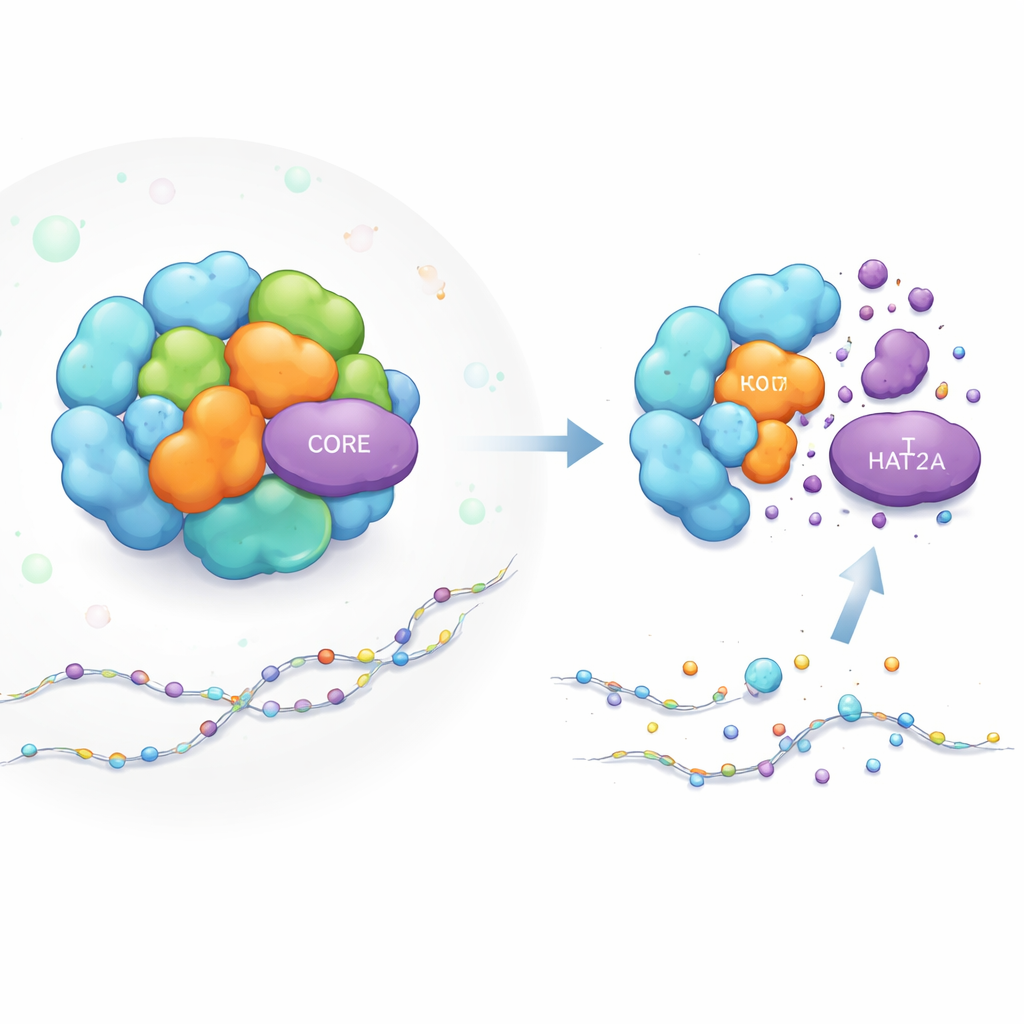
Cómo se construye una máquina de conmutación génica
El complejo SAGA es como un taller modular para la activación génica. Algunas partes realizan tareas químicas, como añadir “marcas” de acetilo a las histonas (los carretes que empaquetan el ADN), lo que facilita la activación de genes cercanos. KAT2A es el operario que añade acetilos en uno de los módulos clave de SAGA. Otras partes de SAGA actúan más como andamiaje, dando forma a la estructura y manteniendo los módulos en su posición cerca del ADN. Aunque los científicos sabían mucho sobre qué hace SAGA, no entendían cómo se mantiene la estabilidad de piezas individuales como KAT2A dentro de esta máquina tan concurrida y dinámica.
Probar qué ocurre cuando se quitan piezas
Para sondear el funcionamiento interno de SAGA, los autores construyeron un informe fluorescente que brilla en proporción a la cantidad de KAT2A en células vivas. Usando edición genética CRISPR, eliminaron cada componente de SAGA uno por uno y observaron cómo cambiaban los niveles de KAT2A. La eliminación de varios socios cercanos en el mismo módulo de acetilación redujo la abundancia de KAT2A, como era de esperar. Sorprendentemente, la eliminación de un trío específico de proteínas estructurales del CORE—TADA1, TAF5L y TAF6L—también provocó una caída pronunciada de la proteína KAT2A, aunque estas partes no realizan reacciones químicas directas. El efecto se observó en múltiples tipos de células humanas, incluidas células de leucemia, lo que indica que es una característica general y no una rareza de una línea celular concreta.
De la estructura rota a la pérdida de actividad génica
Al examinar más de cerca las consecuencias moleculares, el equipo mostró que la pérdida de estas proteínas del CORE hace más que reducir simplemente los niveles de KAT2A. El propio complejo SAGA se desensambla y el módulo de acetilación se separa del ensamblaje mayor. Cuando separaron los componentes celulares por tamaño, KAT2A pasó de fracciones de alto peso molecular, que representan a SAGA intacto, a fracciones más ligeras coherentes con la proteína en solitario. Al mismo tiempo, KAT2A desapareció en gran medida de los sitios de inicio del ADN en todo el genoma, y las marcas de acetilación que normalmente coloca en la histona H3 (en la posición llamada K9) se redujeron sustancialmente. De forma importante, la alteración del CORE bloqueó la respuesta de respaldo habitual en la que una enzima relacionada, KAT2B, puede compensar, haciendo que la pérdida de acetilación sea más profunda y más difícil de reparar para la célula.
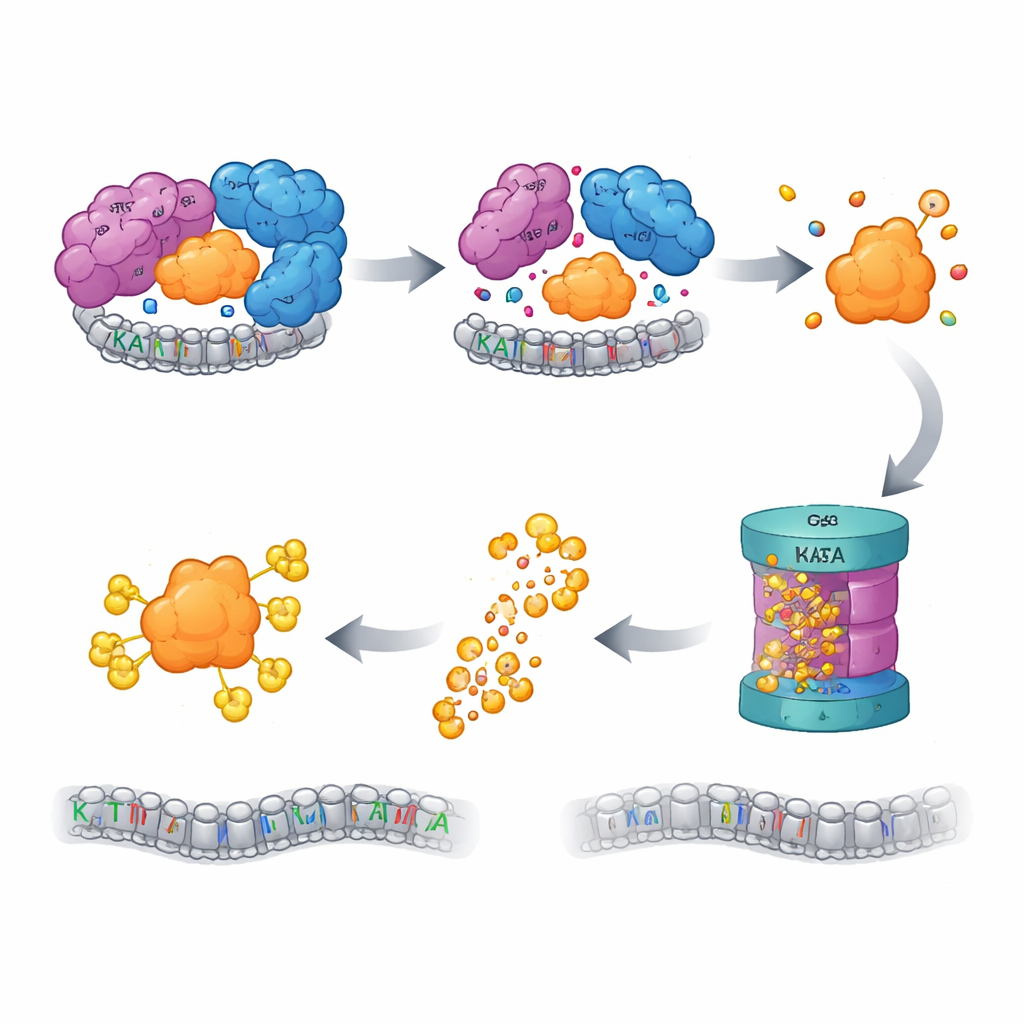
El control de calidad activa la trituradora
Las células poseen sistemas de control de calidad que vigilan las proteínas “huérfanas”: componentes que han perdido a sus socios y que corren el riesgo de plegarse mal o agregarse si se quedan sueltos. Los autores hallaron que cuando se altera el CORE de SAGA, la KAT2A libre es etiquetada para su destrucción por el sistema ubiquitina–proteasoma, la principal maquinaria celular de eliminación de proteínas. Bloquear el proteasoma, o pasos anteriores en esta cascada de etiquetado, restauró los niveles de KAT2A. Una pantalla CRISPR focalizada de más de mil genes relacionados con ubiquitina identificó a una ligasa E3 llamada UBR5, junto con su desubiquitinasa colaboradora OTUD5, como actores clave en el reconocimiento y la degradación de la KAT2A huérfana. De manera intrigante, la pariente cercana KAT2B se mantuvo estable en las mismas condiciones, y mutar una secuencia corta, específica de KAT2A, cerca de su extremo inicial fue suficiente para hacer la proteína más resistente a la destrucción, identificando un “degrón” mínimo y específico de parálogo que marca a KAT2A para su eliminación.
Una vulnerabilidad oculta con promesa terapéutica
En conjunto, el trabajo muestra que la estabilidad y la actividad de KAT2A están estrechamente ligadas a la arquitectura intacta del complejo SAGA. Cuando se pierden componentes estructurales del CORE, SAGA se desensambla, KAT2A queda liberada como una huérfana desprotegida y el sistema de vigilancia UBR5–OTUD5 la dirige rápidamente a la trituradora celular, reduciendo las marcas de acetilación activadoras de genes en todo el genoma. Dado que KAT2A es una vulnerabilidad conocida en varios cánceres, este vínculo incorporado entre estructura, ensamblaje y degradación selectiva sugiere una nueva estrategia: en lugar de dirigirse directamente al sitio activo de KAT2A, los fármacos podrían desestabilizar proteínas andamiaje no enzimáticas de SAGA, bloqueando simultáneamente el acceso de KAT2A a la cromatina y promoviendo su destrucción colateral.
Cita: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Palabras clave: complejo SAGA, KAT2A, control de calidad de proteínas, sistema ubiquitina-proteasoma, epigenética del cáncer