Clear Sky Science · fr
La perturbation du Noyau SAGA déclenche la dégradation collatérale de KAT2A
Quand la machinerie cellulaire se défait
À l’intérieur de chaque cellule, des tâches essentielles comme l’activation et la répression des gènes sont assurées par d’immenses machines moléculaires construites à partir de nombreuses pièces protéiques distinctes. Cette étude se penche sur l’une de ces machines, appelée complexe SAGA, qui facilite l’activation des gènes et est souvent détournée dans le cancer. Les chercheurs ont découvert que si l’on endommage des pièces structurelles clés de SAGA, on n’affaiblit pas seulement la machine : on déclenche la destruction sélective de l’un de ses principaux éléments actifs, une protéine nommée KAT2A, révélant une vulnérabilité cachée que des médicaments pourraient potentiellement exploiter.
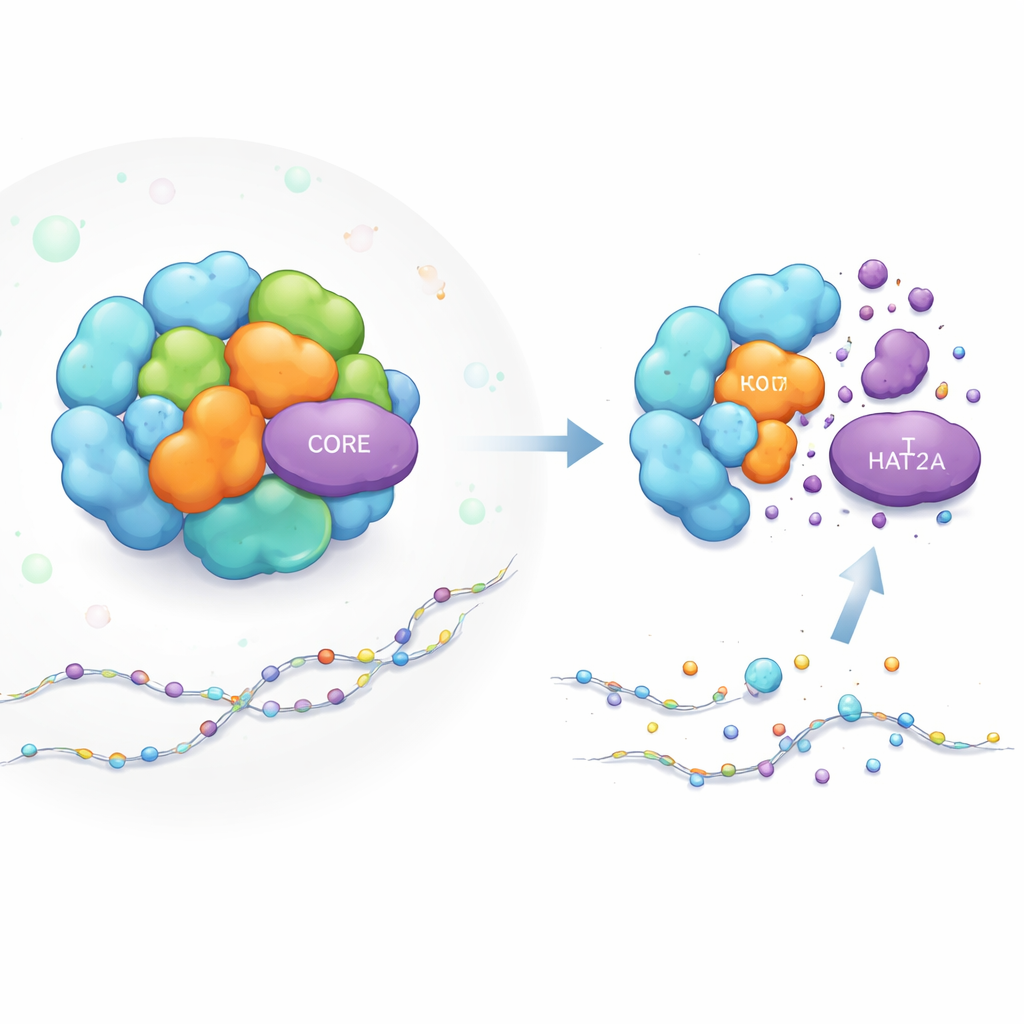
Comment une machine d’activation génique est construite
Le complexe SAGA fonctionne comme un atelier modulaire pour l’activation des gènes. Certaines parties accomplissent des tâches chimiques, comme ajouter des « étiquettes » acétyl aux protéines histones (les bobines qui emballent l’ADN), ce qui facilite l’activation des gènes voisins. KAT2A est l’agent acetylant dans l’un des modules clés de SAGA. D’autres composants de SAGA jouent plutôt un rôle de charpente, donnant à l’ensemble sa forme et maintenant les modules au bon emplacement près de l’ADN. Bien que les scientifiques connaissent bien les fonctions de SAGA, ils comprenaient moins comment la stabilité de composants individuels comme KAT2A est maintenue au sein de cette machine dense et dynamique.
Tester ce qui se passe lorsque des pièces sont retirées
Pour sonder l’architecture interne de SAGA, les auteurs ont construit un témoin fluorescent qui s’allume en proportion de la quantité de KAT2A dans des cellules vivantes. Grâce à l’édition génétique CRISPR, ils ont supprimé chaque composant de SAGA un par un et observé les variations du niveau de KAT2A. L’élimination de plusieurs partenaires proches dans le même module d’acétylation réduisait l’abondance de KAT2A, comme attendu. De manière surprenante, l’inactivation d’un trio spécifique de protéines structurelles du NOYAU—TADA1, TAF5L et TAF6L—a également provoqué une chute nette de la protéine KAT2A, bien que ces éléments n’effectuent pas directement de réactions chimiques. L’effet a été observé dans plusieurs types cellulaires humains, y compris des cellules leucémiques, montrant qu’il s’agit d’une caractéristique générale et non d’une curiosité liée à une lignée cellulaire.
D’une structure brisée à une activité génique perdue
En examinant de plus près les conséquences moléculaires, l’équipe a montré que la perte de ces protéines du NOYAU fait plus que simplement diminuer les niveaux de KAT2A. Le complexe SAGA lui‑même se désagrège, et le module d’acétylation se détache de l’assemblage plus large. En séparant les composants cellulaires par taille, KAT2A a basculé des fractions de haut poids moléculaire, représentant SAGA intact, vers des fractions plus légères compatibles avec la protéine isolée. Parallèlement, KAT2A a largement disparu des sites d’initiation de la transcription à travers le génome, et les marques d’acétylation qu’elle place habituellement sur l’histone H3 (en K9) ont été fortement réduites. De façon importante, la perturbation du NOYAU empêchait la réponse de secours habituelle dans laquelle une enzyme apparentée, KAT2B, peut compenser, rendant la perte d’acétylation plus profonde et plus difficile à réparer pour la cellule.
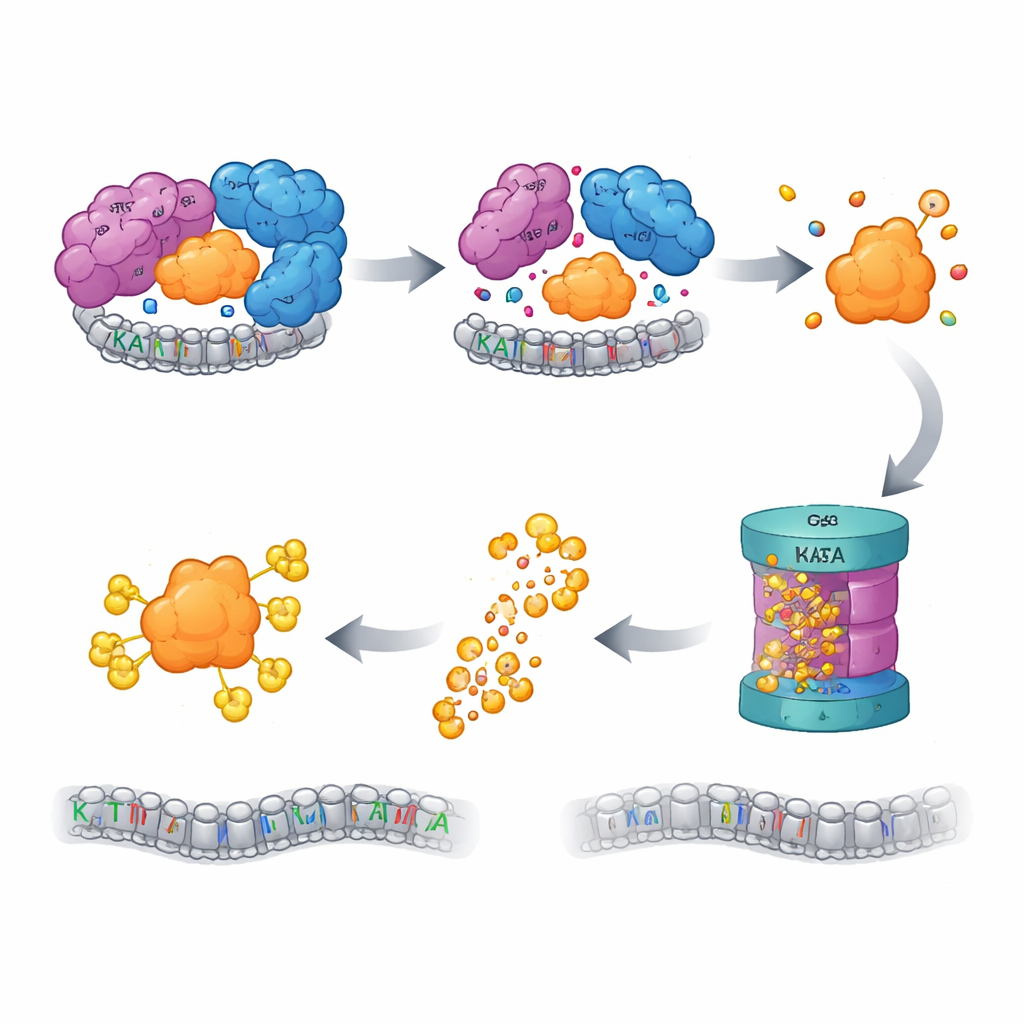
Le contrôle qualité active le broyeur
Les cellules disposent de systèmes de contrôle qualité qui surveillent les protéines « orphelines »—des composants ayant perdu leurs partenaires et risquant de se replier de façon incorrecte ou de s’agréger. Les auteurs ont constaté que lorsque le NOYAU de SAGA est perturbé, KAT2A libre est étiquetée pour destruction par le système ubiquitine–protéasome, la principale machinerie d’élimination des protéines de la cellule. Le blocage du protéasome, ou des étapes antérieures de cette cascade d’étiquetage, rétablissait les niveaux de KAT2A. Un criblage CRISPR ciblé de plus d’un millier de gènes liés à l’ubiquitine a identifié une ligase E3 nommée UBR5, ainsi que sa déubiquitinase associée OTUD5, comme acteurs clés dans la reconnaissance et la dégradation de KAT2A orpheline. Fait intrigant, le proche homologue KAT2B restait stable dans les mêmes conditions, et la mutation d’une courte séquence spécifique à KAT2A près de son extrémité N‑terminale suffisait à rendre la protéine plus résistante à la destruction, identifiant un « degron » minimal et spécifique au paralogue qui signale KAT2A pour élimination.
Une faiblesse cachée porteuse d’espoir thérapeutique
Dans l’ensemble, ce travail montre que la stabilité et l’activité de KAT2A sont étroitement liées à l’architecture intacte du complexe SAGA. Lorsque des composants structurels du NOYAU sont perdus, SAGA se désassemble, KAT2A se retrouve libérée et vulnérable, et le système de surveillance UBR5–OTUD5 la dirige rapidement vers le broyeur cellulaire, réduisant les marques d’acétylation activatrices des gènes à l’échelle du génome. Étant donné que KAT2A représente une vulnérabilité connue dans plusieurs cancers, ce lien intrinsèque entre structure, assemblage et dégradation sélective suggère une nouvelle stratégie : plutôt que de cibler directement le site actif de KAT2A, des médicaments pourraient déstabiliser des protéines d’échafaudage non enzymatiques de SAGA, bloquant simultanément l’accès de KAT2A à la chromatine et favorisant sa destruction collatérale.
Citation: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Mots-clés: complexe SAGA, KAT2A, contrôle qualité des protéines, système ubiquitine–protéasome, épigénétique du cancer