Clear Sky Science · it
La disgregazione del CORE di SAGA provoca la degradazione collaterale di KAT2A
Quando la macchina cellulare si sfalda
All’interno di ogni cellula, compiti essenziali come l’attivazione e la repressione dei geni sono svolti da enormi macchine molecolari composte da molteplici parti proteiche. Questo studio analizza una di queste macchine, chiamata complesso SAGA, che facilita l’accensione dei geni ed è spesso sfruttata nel cancro. I ricercatori hanno scoperto che se si danneggiano pezzi strutturali chiave di SAGA, non si indebolisce solo la macchina: si innesca la distruzione selettiva di una delle sue principali componenti operative, una proteina chiamata KAT2A, rivelando una vulnerabilità nascosta che i farmaci potrebbero potenzialmente sfruttare.
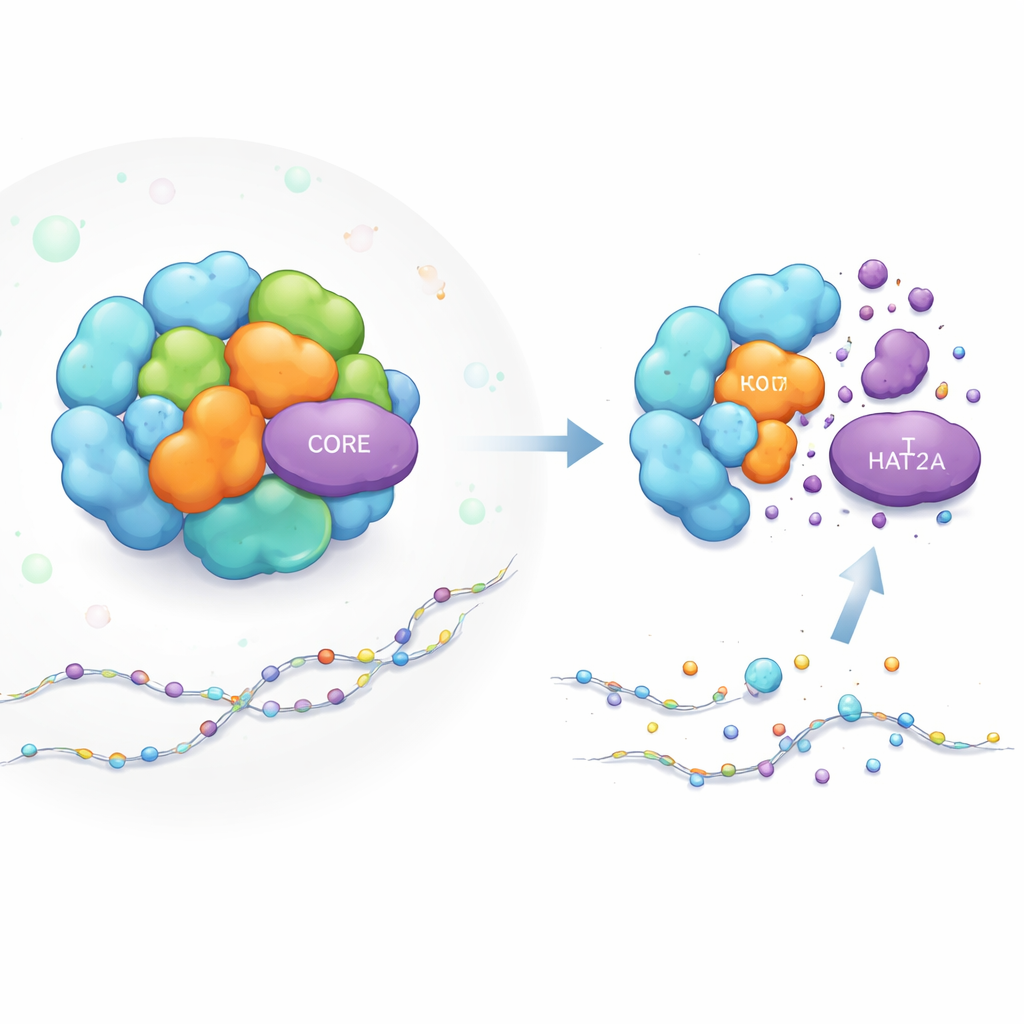
Come è assemblata una macchina per l’accensione dei geni
Il complesso SAGA funziona come un’officina modulare per l’attivazione genica. Alcune parti svolgono compiti chimici, come l’aggiunta di “marchi” acetilici alle proteine istoniche (i supporti che impacchettano il DNA), rendendo più facile l’attivazione dei geni vicini. KAT2A è l’enzima che aggiunge questi gruppi acetilici in uno dei moduli chiave di SAGA. Altri componenti di SAGA agiscono più come impalcature, dando forma all’intera struttura e mantenendo i moduli nella posizione corretta vicino al DNA. Pur conoscendo molto sulle funzioni di SAGA, gli scienziati non capivano pienamente come venga mantenuta la stabilità di singole componenti come KAT2A all’interno di questa macchina affollata e dinamica.
Mettere alla prova cosa succede quando si rimuovono i pezzi
Per sondare il funzionamento interno di SAGA, gli autori hanno costruito un reporter fluorescente che brilla in proporzione alla quantità di KAT2A nelle cellule vive. Usando l’editing genico CRISPR, hanno eliminato uno per uno i componenti di SAGA e osservato come cambiavano i livelli di KAT2A. La rimozione di diversi partner vicini nello stesso modulo di acetilazione riduceva l’abbondanza di KAT2A, come previsto. Sorprendentemente, l’eliminazione di un trio specifico di proteine strutturali del CORE—TADA1, TAF5L e TAF6L—ha anch’essa causato un netto calo della proteina KAT2A, nonostante queste parti non svolgano direttamente reazioni chimiche. L’effetto è stato riscontrato in diversi tipi di cellule umane, incluse cellule leucemiche, indicando che si tratta di una caratteristica generale piuttosto che di una peculiarità di una singola linea cellulare.
Da struttura compromessa a perdita di attività genica
Analizzando più da vicino le conseguenze molecolari, il gruppo ha mostrato che la perdita di queste proteine del CORE fa più che ridurre i livelli di KAT2A. Il complesso SAGA stesso si disfa e il modulo di acetilazione si disconnette dall’assemblaggio più ampio. Quando hanno separato i componenti cellulari per dimensione, KAT2A è passata dalle frazioni ad alto peso molecolare, rappresentative di SAGA intatto, a frazioni più leggere coerenti con la proteina solitaria. Allo stesso tempo, KAT2A è risultata in gran parte assente dai siti di inizio della trascrizione nel genoma, e i marchi acetilici che normalmente deposita sull’istone H3 (in corrispondenza della posizione K9) sono stati sostanzialmente ridotti. È importante che la disgregazione del CORE bloccasse la risposta di compensazione usuale, in cui un enzima correlato, KAT2B, può subentrare: questo rende la perdita di acetilazione più pronunciata e più difficile da riparare per la cellula.
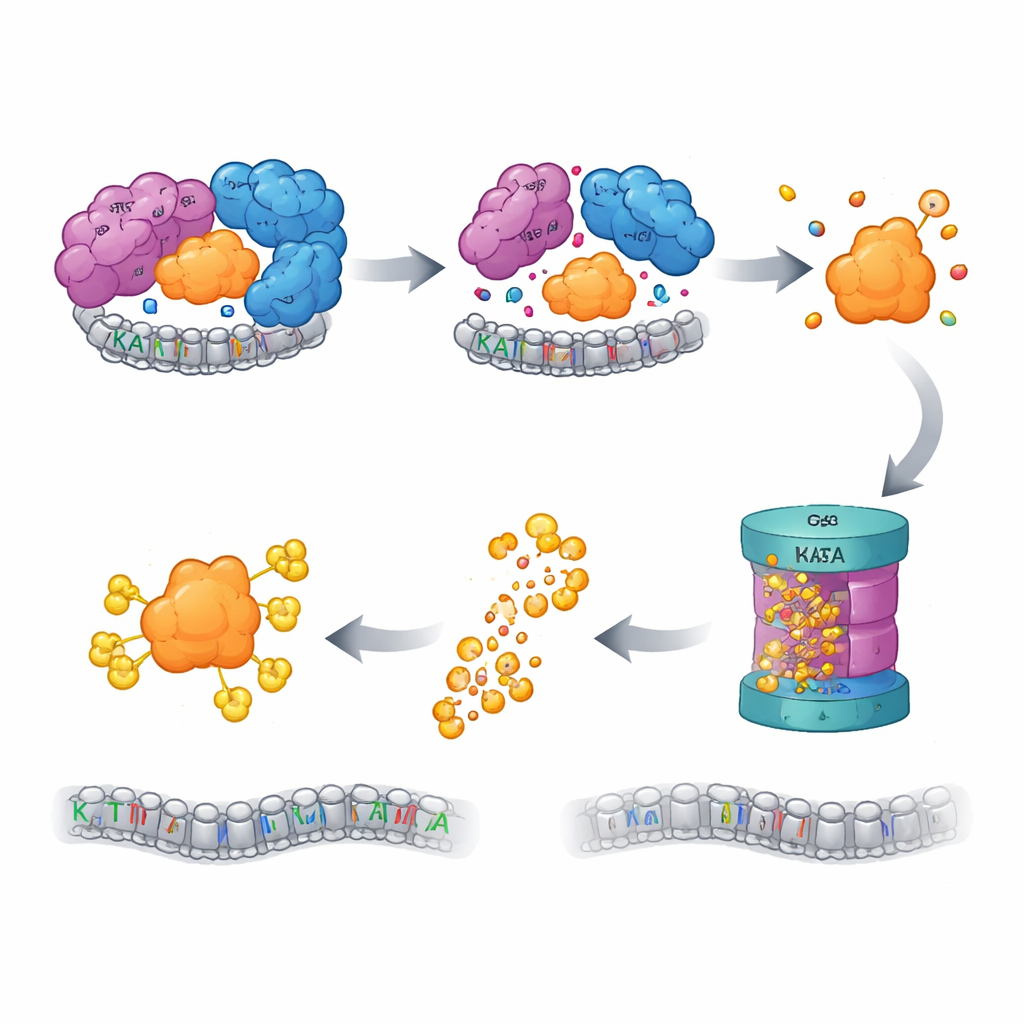
Il controllo qualità attiva il trituratore
Le cellule dispongono di sistemi di controllo qualità che sorvegliano le proteine “orfane”—componenti che hanno perso i partner e rischiano di causare danni se si ripiegano in modo errato o si aggregano. Gli autori hanno scoperto che quando il CORE di SAGA è compromesso, la KAT2A libera viene etichettata per la distruzione dal sistema ubiquitina–proteasoma, la principale macchina cellulare di smaltimento delle proteine. Bloccare il proteasoma, oppure i passaggi iniziali di questa cascata di etichettatura, ripristinava i livelli di KAT2A. Uno screening CRISPR mirato su più di mille geni correlati all’ubiquitina ha identificato una ligasi E3 chiamata UBR5, insieme alla sua deubiquitinasi collaboratrice OTUD5, come attori chiave nel riconoscere e degradare la KAT2A orfana. È interessante che la cugina ravvicinata KAT2B rimanesse stabile nelle stesse condizioni, e che la mutazione di una breve sequenza specifica di KAT2A vicino all’inizio fosse sufficiente a rendere la proteina più resistente alla distruzione, identificando un “degron” minimo, specifico per il paralogo, che segnala KAT2A per lo smaltimento.
Una vulnerabilità nascosta con potenziale terapeutico
Nel complesso, il lavoro mostra che la stabilità e l’attività di KAT2A sono intimamente legate all’architettura intatta del complesso SAGA. Quando componenti strutturali del CORE vanno perduti, SAGA si disassembla, KAT2A viene rilasciata come orfana non protetta e il sistema di sorveglianza UBR5–OTUD5 la indirizza rapidamente al trituratore cellulare, riducendo i marchi acetilici attivatori dei geni in tutto il genoma. Poiché KAT2A è una vulnerabilità nota in diversi tumori, questo legame intrinseco tra struttura, assemblaggio e degradazione selettiva suggerisce una nuova strategia: invece di mirare direttamente al sito attivo di KAT2A, i farmaci potrebbero destabilizzare le proteine impalcatura non enzimatiche di SAGA, bloccando contemporaneamente l’accesso di KAT2A alla cromatina e promuovendone la distruzione collaterale.
Citazione: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Parole chiave: Complesso SAGA, KAT2A, controllo qualità delle proteine, sistema ubiquitina-proteasoma, epigenetica del cancro