Clear Sky Science · sv
Störning av SAGA CORE utlöser kollateral nedbrytning av KAT2A
När cellmaskineriet faller samman
Inuti varje cell utförs viktiga uppgifter, som att slå av och på gener, av stora molekylära maskiner sammansatta av många olika proteindelar. Denna studie granskar en sådan maskin, kallad SAGA-komplexet, som hjälper till att aktivera gener och ofta kapras vid cancer. Forskarna upptäckte att om man skadar viktiga strukturella delar av SAGA så försvagas inte bara maskinen — man utlöser också selektiv destruktion av en av dess huvudarbetskomponenter, ett protein kallat KAT2A, vilket blottlägger en dold sårbarhet som läkemedel potentiellt skulle kunna utnyttja.
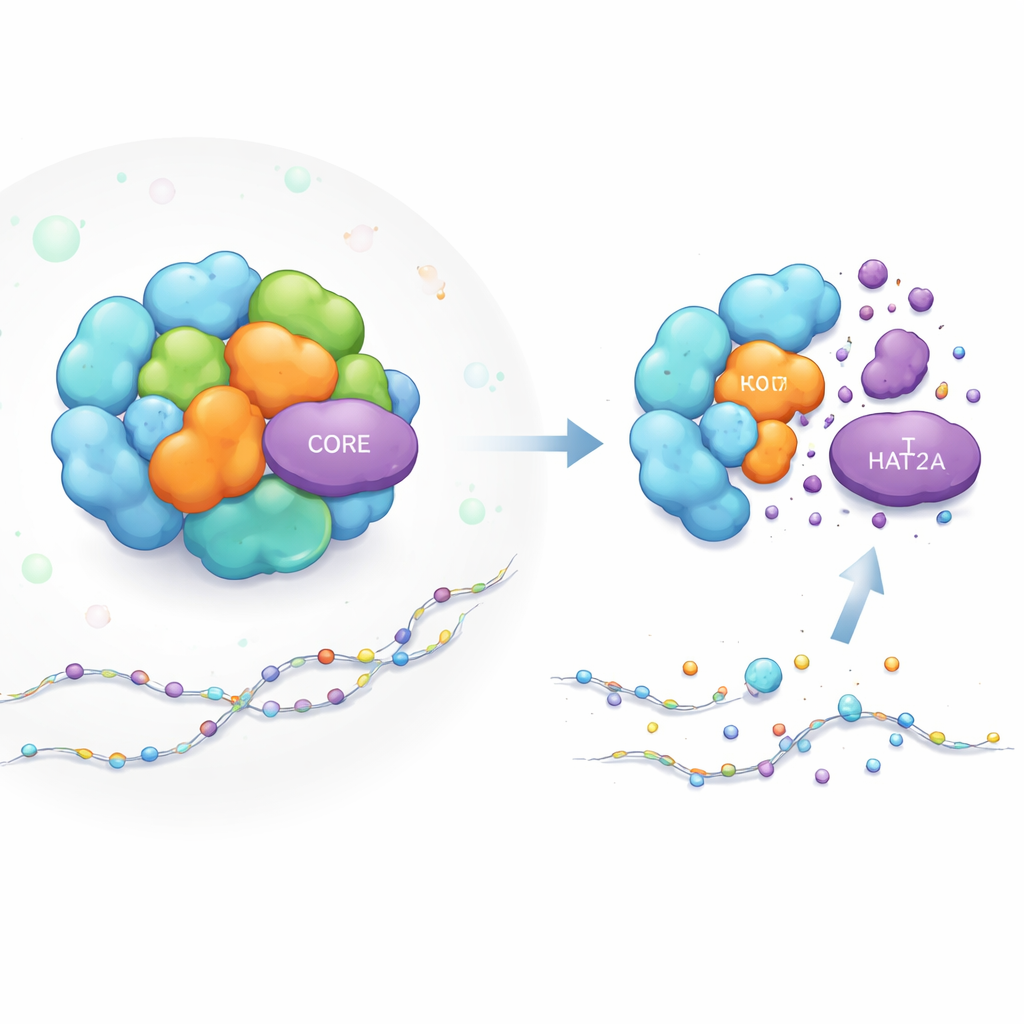
Hur en genaktiverande maskin är uppbyggd
SAGA-komplexet är som en modulär verkstad för genaktivering. Vissa delar utför kemiska uppgifter, till exempel att fästa acetyl-“taggar” på histonproteiner (spolarna som paketerar DNA), vilket gör närliggande gener lättare att slå på. KAT2A är acetylsättaren i en av SAGA:s viktiga moduler. Andra SAGA-delar fungerar mer som ställningar och ger hela strukturen dess form och håller modulerna på rätt plats nära DNA. Medan forskare visste mycket om vad SAGA gör, förstod de inte hur stabiliteten hos individuella delar som KAT2A bevaras inne i denna trånga, dynamiska maskin.
Tester av vad som händer när delar tas bort
För att undersöka SAGA:s inre funktion byggde författarna en fluorescerande rapportör som lyser i proportion till mängden KAT2A i levande celler. Med CRISPR-genredigering slog de ut varje SAGA-komponent en efter en och följde hur KAT2A-nivåerna förändrades. Att ta bort flera närliggande partners i samma acetyleringsmodul minskade KAT2A-mängden, som väntat. Överraskande nog orsakade utslagning av en specifik trio av strukturella CORE-proteiner — TADA1, TAF5L och TAF6L — också en kraftig minskning av KAT2A-protein, trots att dessa delar inte direkt utför kemiska reaktioner. Effekten sågs i flera mänskliga celltyper, inklusive leukemiceller, vilket visar att det är en generell egenskap snarare än ett cellinje-specifikt fenomen.
Från brutet bygge till förlorad genaktivitet
Genom att granska de molekylära följderna närmare visade teamet att förlust av dessa CORE-proteiner gör mer än att bara sänka KAT2A-nivåerna. SAGA-komplexet självt faller isär och acetyleringsmodulen lossnar från den större sammansättningen. När de separerade cellulära komponenter efter storlek, skiftade KAT2A från fraktioner med hög molekylvikt, som motsvarar intakt SAGA, till lättare fraktioner förenliga med ensamt protein. Samtidigt försvann KAT2A i stor utsträckning från DNA:s startställen över genomet, och de vanliga acetylmärkena som det sätter på histon H3 (vid positionen kallad K9) var avsevärt reducerade. Viktigt är att störning av CORE blockerade den normala backup-respons där det närbesläktade enzymet KAT2B kan kompensera, vilket gör förlusten av acetylering mer djupgående och svårare för cellen att reparera.
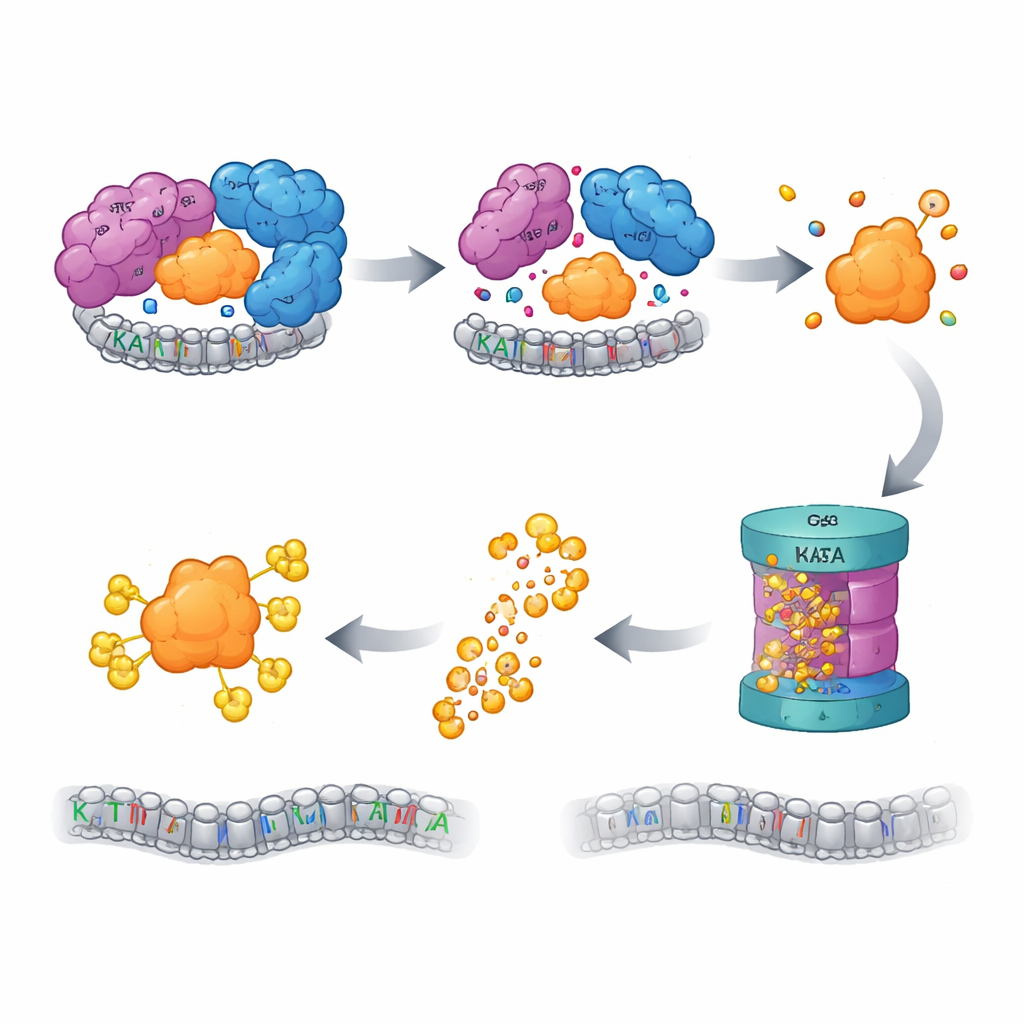
Kvalitetskontrollen kopplar på shreddaren
Celler har kvalitetskontrollsystem som vakta över “föräldralösa” proteiner — komponenter som förlorat sina partners och riskerar att skada genom att felveckas eller klumpa ihop sig. Författarna fann att när SAGA CORE störs så taggas fritt KAT2A för nedbrytning av ubiquitin–proteasomsystemet, cellens huvudsakliga proteinborttagningsmaskineri. Att blockera proteasomen, eller tidigare steg i denna taggningskedja, återställde KAT2A-nivåerna. En fokuserad CRISPR-skärm av mer än tusen ubiquitinrelaterade gener pekade ut en E3-ligas kallad UBR5, tillsammans med dess hjälpar-deubiquitinase OTUD5, som nyckelspelare i igenkänning och nedbrytning av föräldralöst KAT2A. Intressant nog förblev KAT2A:s nära kusin KAT2B stabil under samma förhållanden, och mutation av en kort, KAT2A-specifik sekvens nära dess början var tillräcklig för att göra proteinet mer motståndskraftigt mot destruktion, vilket identifierar en minimal, paralogspecifik “degron” som flaggar KAT2A för borttagning.
En dold svaghet med terapeutiskt löfte
Sammantaget visar arbetet att KAT2A:s stabilitet och aktivitet är tätt kopplade till SAGA-komplexets intakta arkitektur. När strukturella CORE-komponenter förloras, disassembleras SAGA, KAT2A frigörs som en oskyddad föräldralös och övervakningssystemet UBR5–OTUD5 lotsar snabbt proteinet till cellens shreddare, vilket minskar genaktiverande acetylmärken över genomet. Eftersom KAT2A är en känd sårbarhet i flera cancerformer, antyder denna inneboende koppling mellan struktur, montering och selektiv nedbrytning en ny strategi: istället för att rikta in sig mot KAT2A:s aktiva yta direkt, skulle läkemedel kunna destabilisera icke-enzymatiska SAGA-stommeproteiner, samtidigt som KAT2A:s tillgång till kromatin blockeras och dess kollaterala nedbrytning främjas.
Citering: Batty, P., Beneder, H., Schätz, C. et al. Disruption of the SAGA CORE triggers collateral degradation of KAT2A. Nat Commun 17, 3410 (2026). https://doi.org/10.1038/s41467-026-71613-7
Nyckelord: SAGA-komplexet, KAT2A, proteinernas kvalitetskontroll, ubiquitin–proteasomsystemet, cancerepigenetik