Clear Sky Science · tr
Kationların elektrokatalizde iki yüzlü etkilerini çözümlemek
Temiz Enerjide İki Yüzlü Yardımcılar
Sudan temiz hidrojen yakıtı üretimi genellikle tuzlu çözeltilerle kaplı yüklü metal yüzeylerde gerçekleşen reaksiyonlara dayanır. Çözünen pozitif yüklü atomlar, yani katyonlar, genellikle pasif bir arka plan olarak ele alınır. Bu makale onların öyle olmadığını gösteriyor: bazen hidrojen üretimini hızlandıran aynı katyonlar, biraz farklı koşullarda yavaşlatıcı olabilir. Bu çift yönlü doğanın anlaşılması, daha iyi elektrolizörler ve düşük karbonlu bir gelecek için diğer elektrokimyasal teknolojilerin tasarlanması açısından hayati öneme sahiptir.
Elektrotlarda Tuz İyonları Neden Önemli?
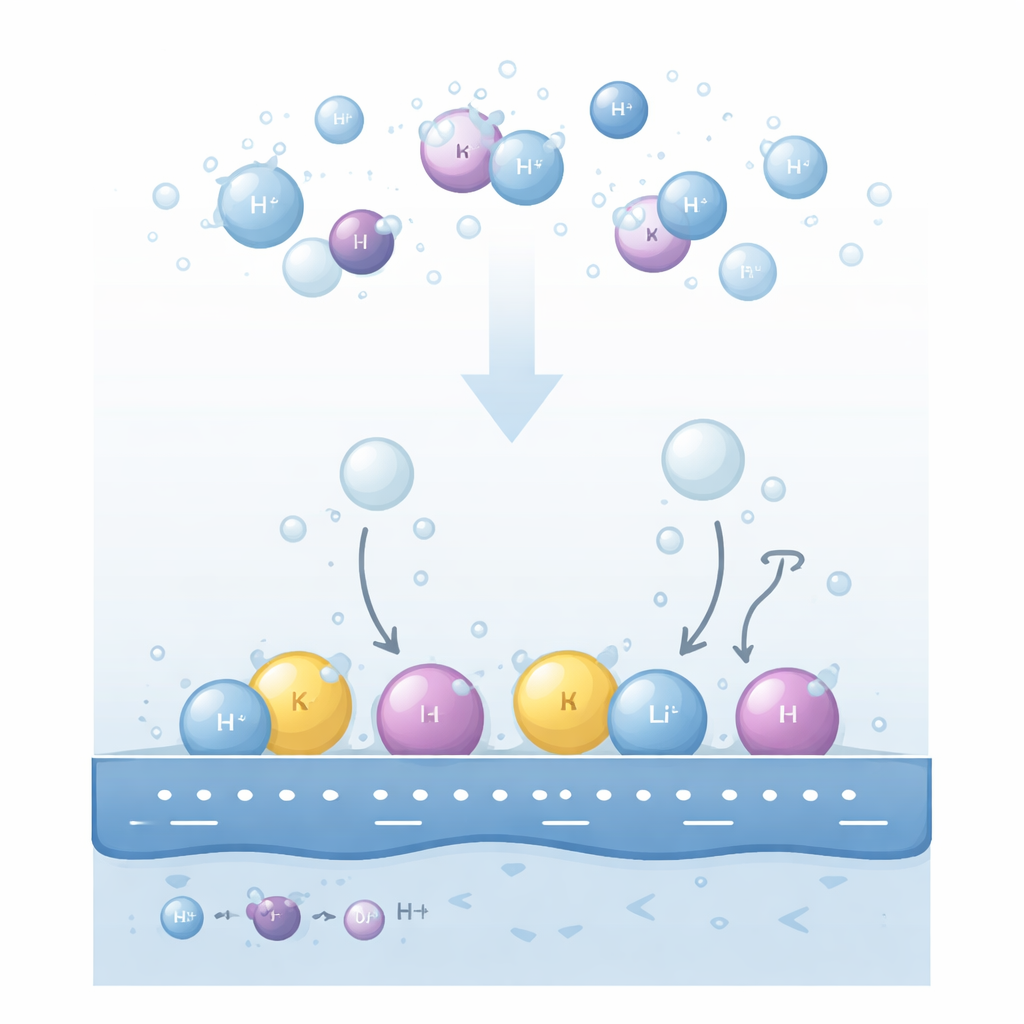
Bir metal elektrota alkalin bir çözeltide voltaj uygulandığında, yüzeye yakın su molekülleri parçalanarak hidrojen gazı oluşturur. Deneyler uzun süredir çözünen katyonun türünün (lityum, sodyum veya potasyum gibi) ve konsantrasyonunun hidrojen üretim hızını dramatik şekilde değiştirebildiğini gösteriyor. Daha da şaşırtıcı olarak, eğilimler tersine dönebiliyor: altın yüzeylerde, bir katyon sıralaması düşük voltajlarda ortaya çıkarken daha yüksek voltajlarda tersine çevriliyor; çözeltinin pH'ını veya katyon konsantrasyonunu değiştirmek görünürde bir teşvik ediciyi inhibitöre dönüştürebiliyor. Mevcut açıklamalar hidrojeni metal üzerinde ne kadar güçlü şekilde tuttuğuna veya yüklü türlerin ne kadar kolay uzaklaştığına odaklanmıştı, fakat bu fikirler gözlemlenen tüm tersine dönüşleri tutarlı biçimde açıklayamıyordu.
Katyonlar için İki Bölge
Yazarlar anahtarın katyonların elektrot yakınındaki ince sıvı tabakasında gerçekte nerede bulunduğunda yattığını öne sürüyor. İki ana bölge ayırt ediyorlar. Bazı katyonlar su molekülleriyle tamamen çevrili kalır ve yüzeyden biraz uzakta “dağılmış” bir bölgede süzülür. Diğerleri ise metale uygulanan güçlü negatif yük tarafından kısmen su kabuğunu kaybeder ve ara yüzeyin ilk su tabakasına sıkıca yaklaşarak kompakt bir “spesifik adsorbe” tabakası oluşturur. Bu iki katyon popülasyonu yerel elektrik alanını zıt yönlerde yeniden düzenler. Dağınık katyonlar yakınlardaki su moleküllerinin hissettiği alanı güçlendirirken, adsorbe olmuş katyonlar metalin yükünü kısmen ekranlayarak bu alanı zayıflatır.
Görünmez Kaldıraçlar Olarak Elektrik Alanları
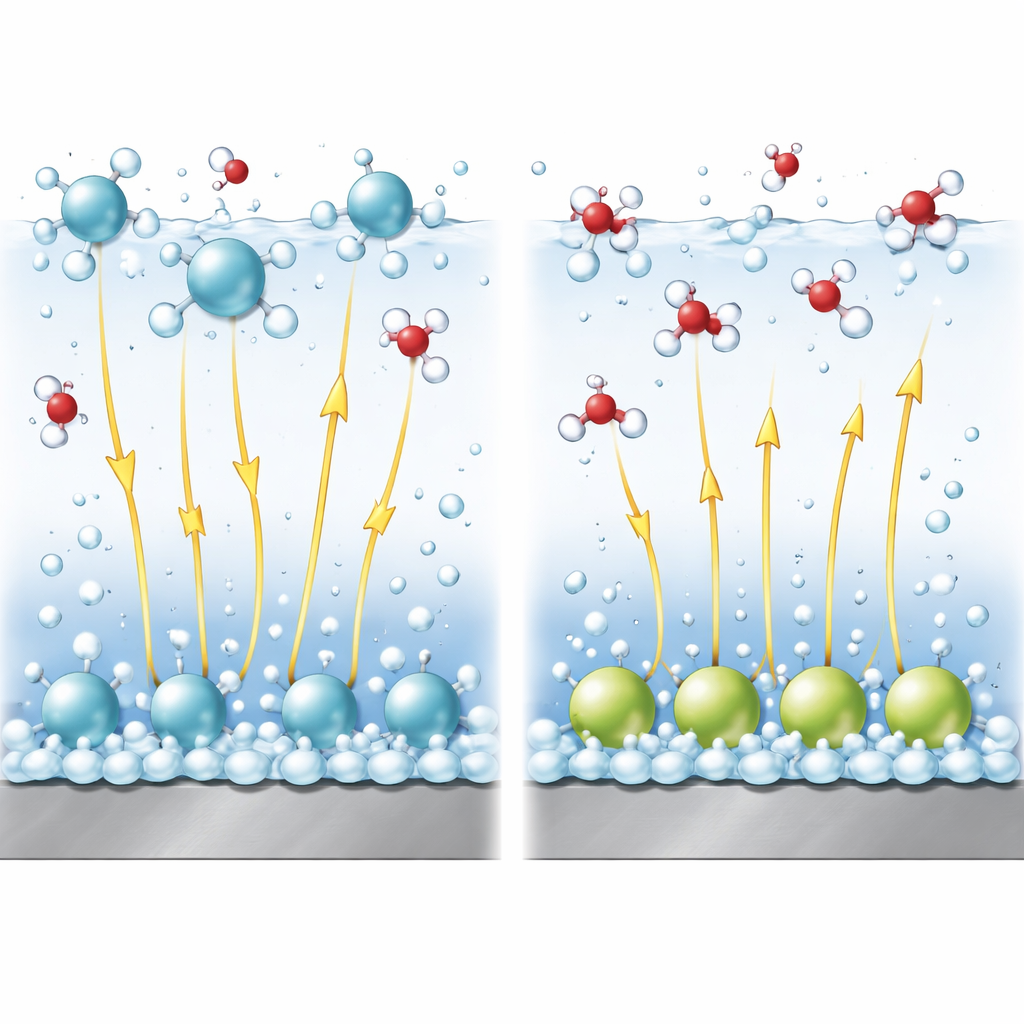
Alkalin çözeltilerde suyu bölüp hidrojen oluşturmak, basit protonları indirgemekten daha zordur. Reaksiyonun kritik bir parçası bir su molekülü içindeki bağı koparmaktır. Yüzeye yakın güçlü elektrik alanları bu bağı germeye ve koparmaya yardımcı olur; tıpkı bir yayı zıt uçlarından çekmek gibi. İyileştirilmiş bir teorik model kullanan yazarlar, katyon düzenini bu alanın gücü ve bağ kırılmasının enerji bariyeriyle ilişkilendirir. Dağınık tabakadaki katyonların yerel potansiyeli reaksiyonu destekleyecek şekilde yükseltme ve elektrik alanı güçlü tutma eğiliminde olduğunu, dolayısıyla hidrojen oluşumunu teşvik ettiğini gösterirler. Buna karşılık, spesifik olarak adsorbe olmuş katyonlar reaksiyonun gerçekleştiği su tabakasındaki etkin alanı azaltır, bağ kırmayı zorlaştırır ve reaksiyonu yavaşlatır.
Karmaşık Deneysel Eğilimleri Açıklamak
Model, voltaj, pH, katyon boyutu ve katyon–yüzey afinitesiyle dağınık ve adsorbe katyonlar arasındaki dengeyi kaydırmaya izin vererek çok çeşitli kafa karıştırıcı verileri yeniden üretiyor. Örneğin potasyum iyonları daha zayıf hidrate olur ve lityum iyonlarına göre daha kolay adsorbe olma eğilimindedir. Orta düzey voltajlarda boyut ve konumlandırma etkileri potasyumu daha faydalı gösterir. Ancak daha yüksek voltajlarda potasyumun yoğun adsorpsiyonu alanı o kadar etkili bir şekilde ekranlar ki lityum daha iyi “yardımcı” olur ve aktivite sıralaması tersine döner. Benzer şekilde, lityum tuzlarının konsantrasyonu artırıldığında dağınık katyonlar hakim olur ve reaksiyon hızlanır; fakat sodyum veya potasyum konsantrasyonunun artırılması adsorbe katyonları destekler ve reaksiyonu yavaşlatır. Modelde katyonların bağlanma gücünü ayarlamak, elektrot malzemeleri ve çözeltinin pH'ı arasındaki farkları taklit eder ve altın ve platin yüzeylerinde çeşitli alkalin koşullardaki deneysel davranışla eşleşir.
Gelecekteki Cihazlar İçin Ne Anlama Geliyor
Basitçe söylemek gerekirse, çalışma çözünen katyonların hidrojen üretiminde çift rol oynadığını ortaya koyuyor: su moleküllerini çekerek onların parçalanmasına yardımcı olabilirler ya da yüzeyi doldurup reaksiyonu tetikleyen elektrik alanını boğabilirler. Hangi yüzü gösterecekleri ise boyutlarına, suyu ne kadar sıkı tuttuklarına, elektrota ne kadar güçlü yapıştıklarına ve ne kadar yoğun olduklarına bağlıdır. Bu birleşik resim onlarca yıllık kafa karıştırıcı gözlemi açıklamaya yardımcı olur ve elektrolizörler ile ilgili teknolojiler için yeni tasarım kuralları önerir. Tek bir “en iyi” katyon seçmek yerine, mühendisler karışımları ve koşulları öyle ayarlayabilir ki çoğu katyon yüzeye tam doğru mesafede otursun—elektrik alanını güçlendirecek kadar yakın, fakat onu boğmayacak kadar bağlı olmayan bir konumda.
Atıf: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Anahtar kelimeler: hidrojen açılma reaksiyonu, elektrik çift tabaka, alkali metal katyonları, su elektrolizi, elektrokataliz