Clear Sky Science · de
Die zwei Gesichter der Kationen in der Elektrokatalyse entschlüsseln
Zweiseitige Helfer in der sauberen Energie
Die Erzeugung von sauberem Wasserstoff aus Wasser beruht häufig auf Reaktionen an geladenen Metalloberflächen, die in salzhaltigen Lösungen liegen. Die gelösten positiv geladenen Atome, also Kationen, werden meist als passiver Hintergrund betrachtet. Diese Arbeit zeigt, dass dem nicht so ist: dieselben Kationen, die unter bestimmten Bedingungen die Wasserstoffbildung beschleunigen, können unter leicht veränderten Bedingungen selbige verlangsamen. Das Verständnis dieser doppelten Natur ist entscheidend für das Design besserer Elektrolyseure und anderer elektrochemischer Technologien für eine CO2‑ärmere Zukunft.
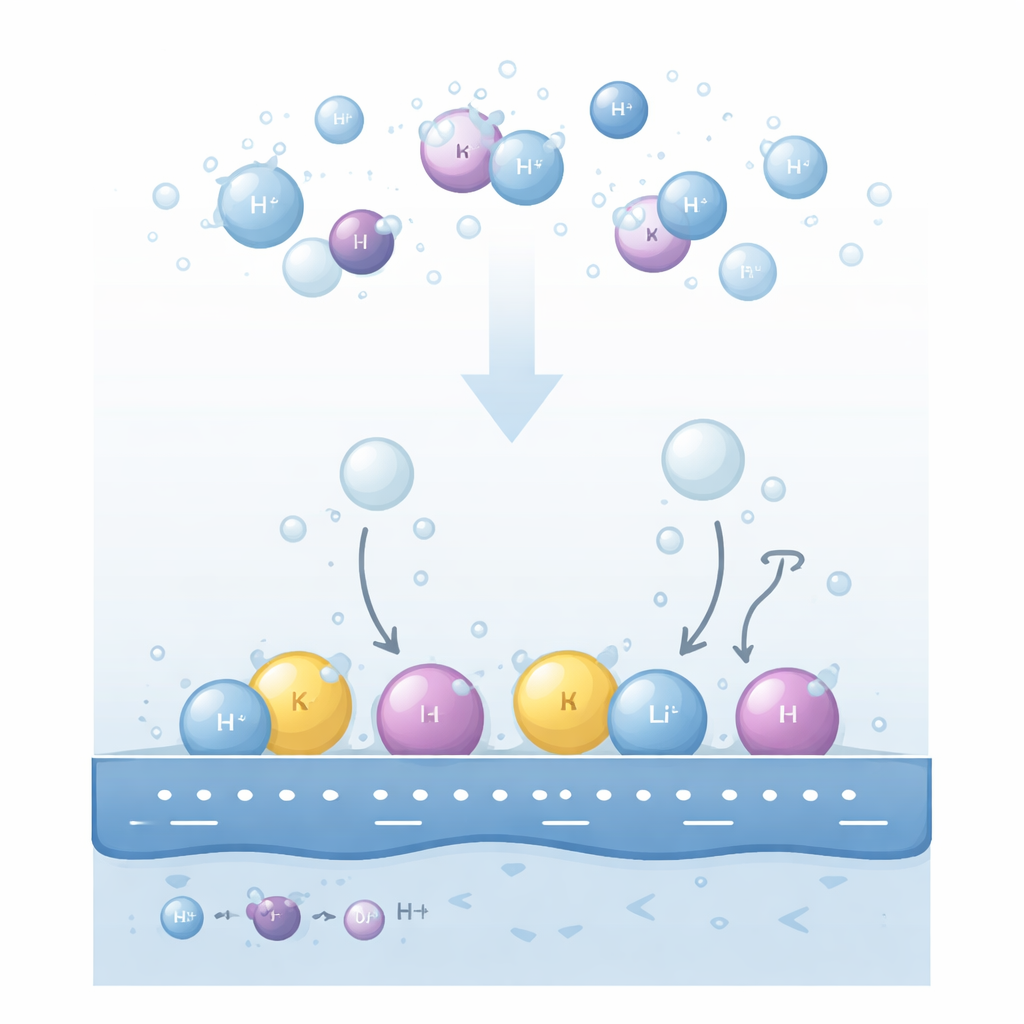
Warum Salzionen an Elektroden wichtig sind
Wenn an eine Metall‑Elektrode in einer alkalischen Lösung eine Spannung angelegt wird, spalten sich Wassermoleküle in der Nähe der Oberfläche und bilden Wasserstoffgas. Experimente zeigen seit Langem, dass sowohl die Art des gelösten Kations (etwa Lithium, Natrium oder Kalium) als auch dessen Konzentration die Geschwindigkeit der Wasserstoffproduktion drastisch verändern können. Noch rätselhafter ist, dass sich die Trends umkehren können: auf Goldoberflächen tritt eine Kationenreihenfolge bei schwächeren Spannungen auf, die sich bei stärkeren Spannungen umkehrt; Änderungen des pH‑Werts oder der Kationenkonzentration können einen vermeintlichen Förderer in einen Hemmer verwandeln. Bisherige Erklärungen konzentrierten sich darauf, wie stark Wasserstoff am Metall haftet oder wie leicht geladene Spezies wegdiffundieren, konnten aber nicht konsistent alle beobachteten Umkehrungen erklären.
Zwei Nachbarschaften für Kationen
Die Autoren schlagen vor, dass der Schlüssel darin liegt, wo sich Kationen tatsächlich in der dünnen Flüssigkeitsschicht neben der Elektrode aufhalten. Sie unterscheiden zwei Hauptbereiche. Einige Kationen bleiben vollständig von Wassermolekülen umgeben und schweben etwas entfernt von der Oberfläche in einer „diffusen“ Region. Andere, durch die starke negative Ladung des Metalls angezogen, geben teilweise ihre Wasserschale ab und rücken direkt an die erste Lage interfacialen Wassers heran und bilden eine kompakte „spezifisch adsorbierte“ Schicht. Diese beiden Kationenpopulationen verändern das lokale elektrische Feld in entgegengesetzter Weise. Diffuse Kationen verstärken das Feld, das von benachbarten Wassermolekülen empfunden wird, während adsorbierte Kationen die Metallladung teilweise abschirmen und dieses Feld abschwächen.
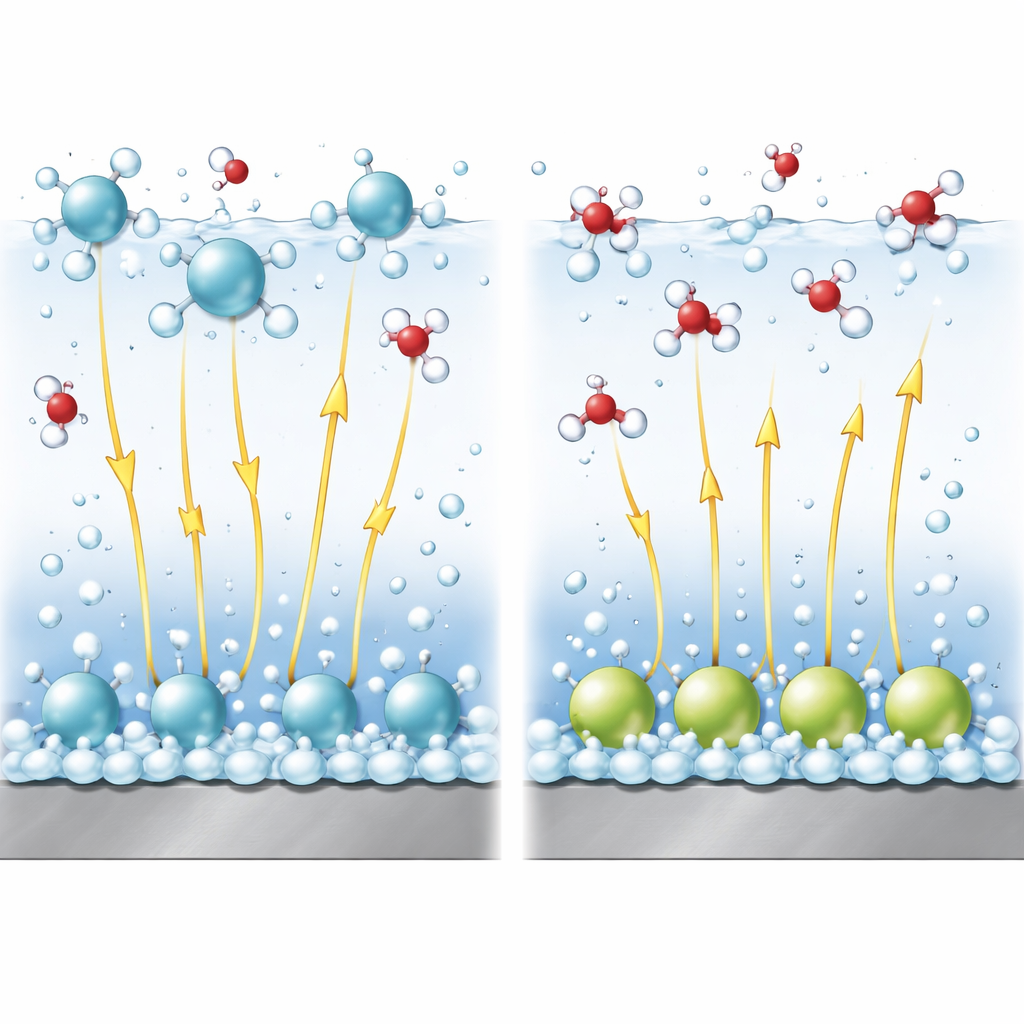
Elektrische Felder als unsichtbare Hebel
In alkalischen Lösungen ist die Wasserspaltung zur Wasserstoffbildung schwieriger als die Reduktion einfacher Protonen. Ein entscheidender Teil der Reaktion ist das Aufbrechen der Bindung innerhalb eines Wassermoleküls. Starke elektrische Felder in der Nähe der Oberfläche helfen dabei, diese Bindung zu dehnen und zu brechen, ähnlich wie beim Auseinanderziehen der Enden einer Feder. Mit einem verfeinerten theoretischen Modell koppeln die Autoren die Anordnung der Kationen an die Stärke dieses Feldes und an die energetische Barriere für das Bindungsbrechen. Sie zeigen, dass Kationen in der diffusen Schicht dazu neigen, das lokale Potential so anzuheben, dass die Reaktion begünstigt wird, und das elektrische Feld stark zu halten, wodurch die Wasserstoffbildung gefördert wird. Im Gegensatz dazu reduzieren spezifisch adsorbierte Kationen das effektive Feld in der Wasserschicht, in der die Reaktion stattfindet, machen das Brechen der Bindung schwieriger und verlangsamen die Reaktion.
Erklärung verwirrender experimenteller Trends
Indem das Modell erlaubt, dass sich das Gleichgewicht zwischen diffusen und adsorbierten Kationen mit Spannung, pH, Kationengröße und Kation‑Oberflächen‑Affinität verschiebt, reproduziert es eine breite Palette rätselhafter Daten. Zum Beispiel sind Kaliumionen schwächer hydratisiert und eher zur Adsorption geneigt als Lithiumionen. Bei moderaten Spannungen erscheinen Kalium‑Effekte durch Größen‑ und Positionsfaktoren vorteilhafter. Bei stärkeren Spannungen jedoch schirmt die dichte Adsorption von Kalium das elektrische Feld so effektiv ab, dass Lithium zum besseren „Helfer“ wird und die Aktivitätsreihenfolge umkehrt. Ebenso führt eine Erhöhung der Lithiumsalzkonzentration dazu, dass diffuse Kationen dominieren und die Reaktion beschleunigt wird, während eine Erhöhung der Natrium‑ oder Kaliumkonzentration adsorbierte Kationen begünstigt und die Reaktion verlangsamt. Die Anpassung der Kationsbindungsstärke im Modell ahmt auch Unterschiede zwischen Elektrodenmaterialien und LösungspH nach und stimmt mit experimentellem Verhalten auf Gold und Platin unter verschiedenen alkalischen Bedingungen überein.
Was das für zukünftige Geräte bedeutet
Kurz gesagt zeigt die Studie, dass gelöste Kationen eine doppelte Rolle bei der Wasserstoffproduktion spielen: Sie können entweder an Wassermolekülen ziehen und so deren Zerfall erleichtern, oder die Oberfläche bevölkern und das elektrische Feld dämpfen, das die Reaktion antreibt. Welche Seite sie zeigen, hängt von ihrer Größe, davon ab, wie fest sie Wasser binden, wie stark sie an der Elektrode haften und wie konzentriert sie sind. Dieses vereinheitlichte Bild hilft, jahrzehntelange verwirrende Beobachtungen zu erklären, und legt neue Gestaltungsprinzipien für Elektrolyseure und verwandte Technologien nahe. Anstatt ein einzelnes „bestes“ Kation zu wählen, könnten Ingenieure Mischungen und Bedingungen so abstimmen, dass die meisten Kationen in genau dem richtigen Abstand zur Oberfläche sitzen — stark genug, um das elektrische Feld zu verstärken, aber nicht so stark gebunden, dass sie es ersticken.
Zitation: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Schlüsselwörter: Wasserstoffentwicklungsreaktion, elektrische Doppelschicht, Alkali-Metallkationen, Wasserelektrolyse, Elektrokatalyse