Clear Sky Science · fr
Démêler les effets à deux visages des cations en électrocatalyse
Des aides à deux faces pour les énergies propres
La production d'hydrogène propre à partir de l'eau repose souvent sur des réactions à la surface de métaux chargés plongés dans des solutions salines. Les atomes dissous chargés positivement, ou cations, sont généralement considérés comme un arrière‑plan passif. Cet article montre qu'il n'en est rien : les mêmes cations qui accélèrent parfois la production d'hydrogène peuvent, dans des conditions légèrement différentes, la ralentir. Comprendre cette double nature est essentiel pour concevoir de meilleurs électrolyseurs et autres technologies électrochimiques pour un avenir à faible émission de carbone.
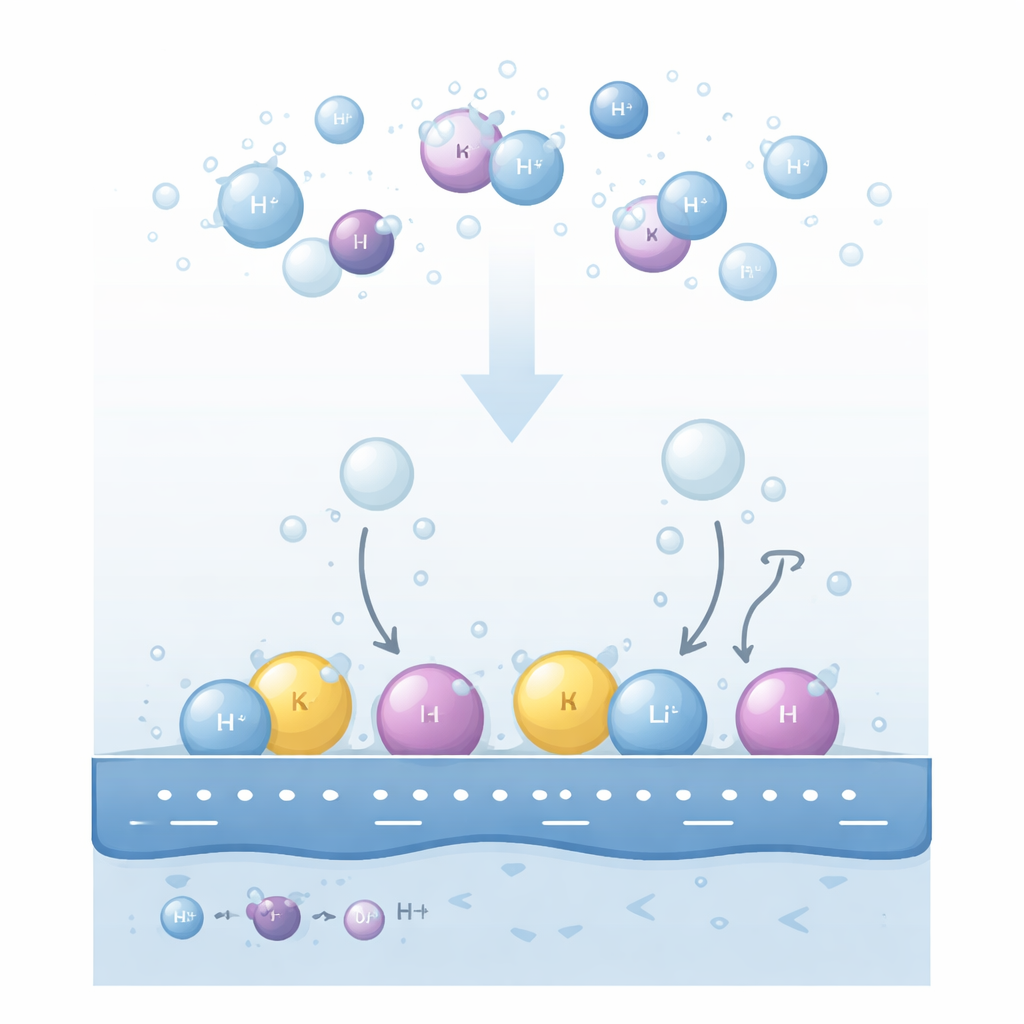
Pourquoi les ions de sel comptent aux électrodes
Quand une tension électrique est appliquée à une électrode métallique dans une solution alcaline, les molécules d'eau proches de la surface se scindent pour former du gaz hydrogène. Les expériences montrent depuis longtemps que le type de cation dissous (comme le lithium, le sodium ou le potassium) et sa concentration peuvent modifier de façon spectaculaire la vitesse de production d'hydrogène. Plus étonnant encore, les tendances peuvent s'inverser : sur l'or, un ordre des cations apparaît à faibles tensions mais se renverse à tensions plus élevées ; changer le pH de la solution ou la concentration en cations peut transformer un promoteur apparent en inhibiteur. Les explications existantes mettaient l'accent sur la force d'adsorption de l'hydrogène sur le métal ou sur la mobilité des espèces chargées, mais ces idées ne permettaient pas d'expliquer de manière cohérente toutes les inversions observées.
Deux quartiers pour les cations
Les auteurs proposent que la clé réside dans l'endroit où les cations se trouvent réellement dans la mince couche liquide adjacente à l'électrode. Ils distinguent deux principaux « quartiers ». Certains cations restent entièrement entourés de molécules d'eau et flottent un peu à l'écart de la surface dans une région « diffuse ». D'autres, attirés par une forte charge négative du métal, abandonnent partiellement leur coque d'eau et se blottissent contre la première couche d'eau interfaciale, formant une couche compacte « spécifiquement adsorbée ». Ces deux populations de cations réarrangent le champ électrique local de manières opposées. Les cations diffus renforcent le champ ressenti par les molécules d'eau voisines, tandis que les cations adsorbés atténuent partiellement la charge du métal et affaiblissent ce champ.
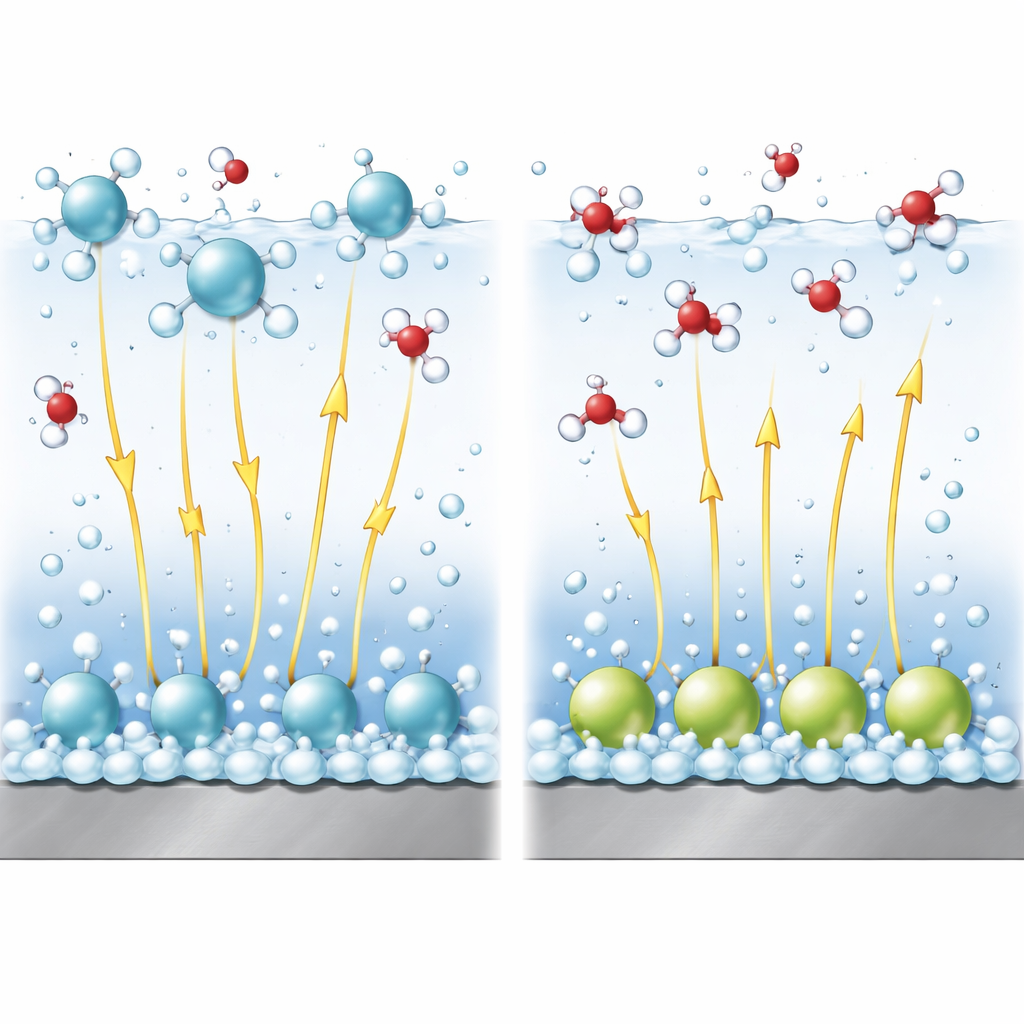
Les champs électriques comme leviers invisibles
Dans les solutions alcalines, scinder l'eau pour produire de l'hydrogène est plus difficile que réduire de simples protons. Une étape cruciale de la réaction est la rupture de la liaison au sein d'une molécule d'eau. Des champs électriques intenses près de la surface aident à étirer et rompre cette liaison, un peu comme tirer sur les deux extrémités d'un ressort. En utilisant un modèle théorique raffiné, les auteurs relient l'arrangement des cations à la force de ce champ et à la barrière d'énergie pour la cassure de la liaison. Ils montrent que les cations situés dans la couche diffuse ont tendance à élever le potentiel local d'une manière qui favorise la réaction et à maintenir le champ électrique fort, favorisant ainsi la formation d'hydrogène. En revanche, les cations spécifiquement adsorbés réduisent le champ effectif dans la couche d'eau où la réaction a lieu, rendant la rupture de la liaison plus difficile et ralentissant la réaction.
Expliquer des tendances expérimentales déroutantes
En permettant à l'équilibre entre cations diffus et adsorbés de varier avec la tension, le pH, la taille des cations et l'affinité cation‑surface, le modèle reproduit un large éventail de données énigmatiques. Par exemple, les ions potassium sont moins hydratés et plus enclins à s'adsorber que les ions lithium. À des tensions modestes, les effets de taille et de position font paraître le potassium plus bénéfique. À des tensions plus élevées, cependant, une adsorption dense du potassium écrante si efficacement le champ électrique que le lithium devient le « meilleur » aide, inversant l'ordre d'activité. De même, lorsque la concentration des sels de lithium augmente, les cations diffus dominent et la réaction s'accélère, mais augmenter la concentration en sodium ou potassium favorise les cations adsorbés et ralentit la réaction. Ajuster la force de liaison des cations dans le modèle imite aussi les différences entre matériaux d'électrode et pH de la solution, reproduisant le comportement expérimental sur l'or et le platine dans diverses conditions alcalines.
Ce que cela signifie pour les dispositifs futurs
En termes simples, l'étude révèle que les cations dissous jouent un double rôle dans la production d'hydrogène : ils peuvent soit tirer sur les molécules d'eau pour les aider à se dissocier, soit encombrer la surface et étouffer le champ électrique même qui pilote la réaction. La face qu'ils montrent dépend de leur taille, de la force avec laquelle ils retiennent l'eau, de leur affinité pour l'électrode et de leur concentration. Ce tableau unifié aide à expliquer des décennies d'observations déroutantes et suggère de nouvelles règles de conception pour les électrolyseurs et technologies apparentées. Plutôt que de choisir un unique cation « idéal », les ingénieurs pourraient ajuster les mélanges et les conditions pour que la plupart des cations se placent à la bonne distance de la surface : assez proches pour renforcer le champ électrique, mais pas tellement attachés qu'ils l'étouffent.
Citation: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Mots-clés: réaction d'évolution de l'hydrogène, double couche électrique, cations des métaux alcalins, électrolyse de l'eau, électrocatalyse