Clear Sky Science · es
Desenredando los efectos ambivalentes de los cationes en la electrocatalisis
Ayudantes de doble filo en la energía limpia
Producir hidrógeno limpio a partir del agua a menudo depende de reacciones en superficies metálicas cargadas bañadas por soluciones salinas. Los átomos disueltos con carga positiva, o cationes, suelen considerarse un trasfondo pasivo. Este artículo demuestra que están lejos de serlo: los mismos cationes que a veces aceleran la producción de hidrógeno pueden, en condiciones ligeramente distintas, ralentizarla. Comprender esta doble naturaleza es vital para diseñar electrolizadores y otras tecnologías electroquímicas más eficientes para un futuro bajo en carbono.
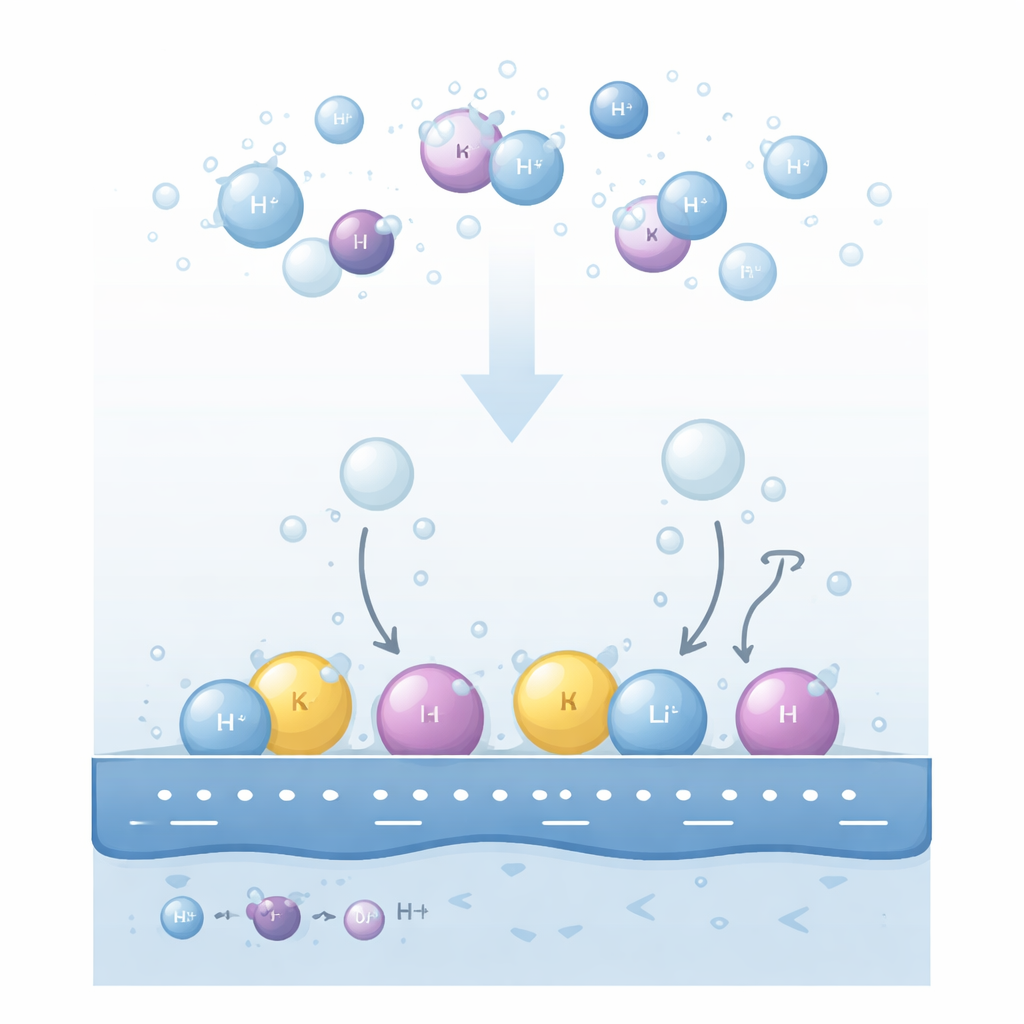
Por qué importan los iones de sal en los electrodos
Cuando se aplica un voltaje eléctrico a un electrodo metálico en una solución alcalina, las moléculas de agua cerca de la superficie se rompen para formar gas hidrógeno. Experimentos han mostrado durante mucho tiempo que tanto el tipo de catión disuelto (como litio, sodio o potasio) como su concentración pueden cambiar drásticamente la velocidad de producción de hidrógeno. Aún más desconcertante, las tendencias pueden invertirse: en superficies de oro, un ordenamiento de cationes aparece a voltajes suaves pero se revierte a voltajes más fuertes; cambiar el pH de la solución o la concentración de cationes puede convertir un aparente promotor en un inhibidor. Las explicaciones existentes se centraban en cuán fuertemente se adhiere el hidrógeno al metal, o en la facilidad con que las especies cargadas se alejan, pero estas ideas no lograban explicar de forma coherente todas las inversiones observadas.
Dos vecindarios para los cationes
Los autores proponen que la clave está en dónde residen realmente los cationes en la delgada capa líquida junto al electrodo. Distinguen dos vecindarios principales. Algunos cationes permanecen totalmente rodeados por moléculas de agua y flotan algo alejados de la superficie en una región “difusa”. Otros, atraídos por una carga negativa fuerte en el metal, desprenden parcialmente su capa de agua y se acoplan justo a la primera capa de agua interfacial, formando una capa compacta “específicamente adsorbida”. Estas dos poblaciones de cationes reorganizan el campo eléctrico local de manera opuesta. Los cationes difusos refuerzan el campo que sienten las moléculas de agua cercanas, mientras que los cationes adsorbidos en parte apantallan la carga del metal y debilitan ese campo.
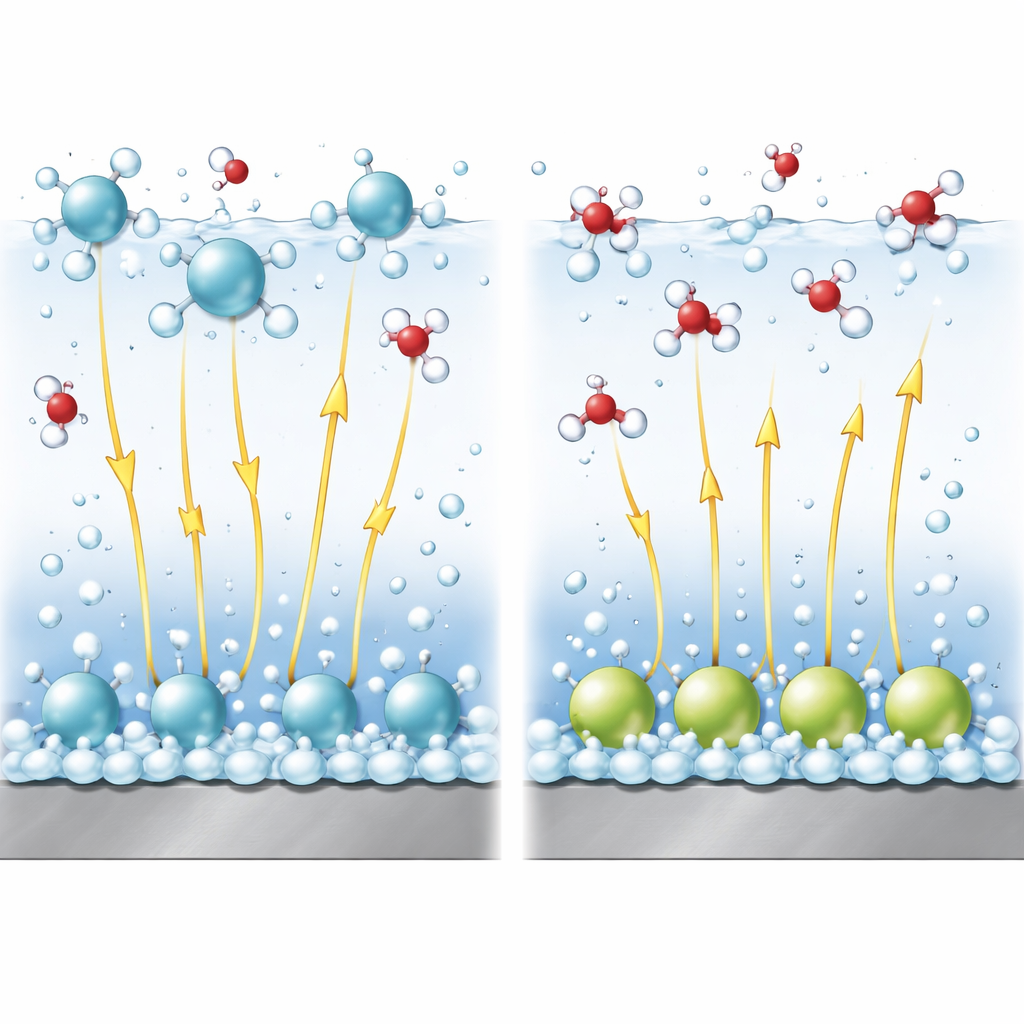
Campos eléctricos como palancas invisibles
En soluciones alcalinas, dividir el agua para producir hidrógeno es más difícil que reducir protones simples. Una parte crucial de la reacción es romper el enlace dentro de una molécula de agua. Los campos eléctricos fuertes cerca de la superficie ayudan a estirar y romper este enlace, de modo similar a tirar de los extremos opuestos de un resorte. Usando un modelo teórico refinado, los autores acoplan la disposición de los cationes con la intensidad de este campo y con la barrera energética para romper el enlace. Muestran que los cationes situados en la capa difusa tienden a elevar el potencial local de una manera que favorece la reacción y mantienen el campo eléctrico fuerte, promoviendo así la formación de hidrógeno. En contraste, los cationes específicamente adsorbidos reducen el campo efectivo en la capa de agua donde ocurre la reacción, haciendo más difícil la ruptura del enlace y ralentizando la reacción.
Explicando tendencias experimentales confusas
Al permitir que el equilibrio entre cationes difusos y adsorbidos cambie con el voltaje, el pH, el tamaño del catión y la afinidad catión‑superficie, el modelo reproduce una amplia gama de datos desconcertantes. Por ejemplo, los iones potasio están menos hidratados y son más propensos a adsorberse que los iones litio. A voltajes modestos, los efectos de tamaño y posicionamiento hacen que el potasio parezca más beneficioso. Sin embargo, a voltajes más fuertes, la adsorción densa de potasio apantalla el campo eléctrico de tal manera que el litio se convierte en el mejor “ayudante”, invirtiendo el orden de actividad. De forma similar, cuando se aumenta la concentración de sales de litio, predominan los cationes difusos y la reacción se acelera, pero aumentar la concentración de sodio o potasio favorece a los cationes adsorbidos y ralentiza la reacción. Ajustar cuán fuertemente se unen los cationes en el modelo también imita las diferencias entre materiales de electrodo y el pH de la solución, coincidiendo con el comportamiento experimental en oro y platino bajo diversas condiciones alcalinas.
Qué significa esto para dispositivos futuros
En términos simples, el estudio revela que los cationes disueltos desempeñan un doble papel en la producción de hidrógeno: pueden tirar de las moléculas de agua para ayudar a que se rompan, o apiñarse en la superficie y amortiguar el propio campo eléctrico que impulsa la reacción. Qué faceta muestran depende de su tamaño, de cuán fuertemente retienen el agua, de cuán fuertemente se adhieren al electrodo y de su concentración. Esta imagen unificada ayuda a explicar décadas de observaciones confusas y sugiere nuevas reglas de diseño para electrolizadores y tecnologías relacionadas. En lugar de elegir un único catión “mejor”, los ingenieros podrían ajustar mezclas y condiciones para que la mayoría de los cationes se sitúen a la distancia adecuada de la superficie: lo bastante fuertes para reforzar el campo eléctrico, pero no tan ligados que lo asfixien.
Cita: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Palabras clave: reacción de evolución de hidrógeno, doble capa eléctrica, cationes de metales alcalinos, electrólisis del agua, electrocatalisis