Clear Sky Science · pl
Rozplątywanie janusowych efektów kationów w elektrokatalizie
Dwubiegunowi pomocnicy w czystej energii
Wytwarzanie czystego paliwa wodorowego z wody często opiera się na reakcjach na naładowanych powierzchniach metalicznych zanurzonych w roztworach solnych. Rozpuszczone dodatnio naładowane atomy, czyli kationy, zwykle traktuje się jako bierne tło. Niniejszy artykuł pokazuje, że są one czymś zupełnie przeciwnym: te same kationy, które czasem przyspieszają produkcję wodoru, przy nieco innych warunkach mogą ją spowalniać. Zrozumienie tej podwójnej natury jest kluczowe dla projektowania lepszych elektrolizerów i innych technologii elektrochemicznych dla niskoemisyjnej przyszłości.
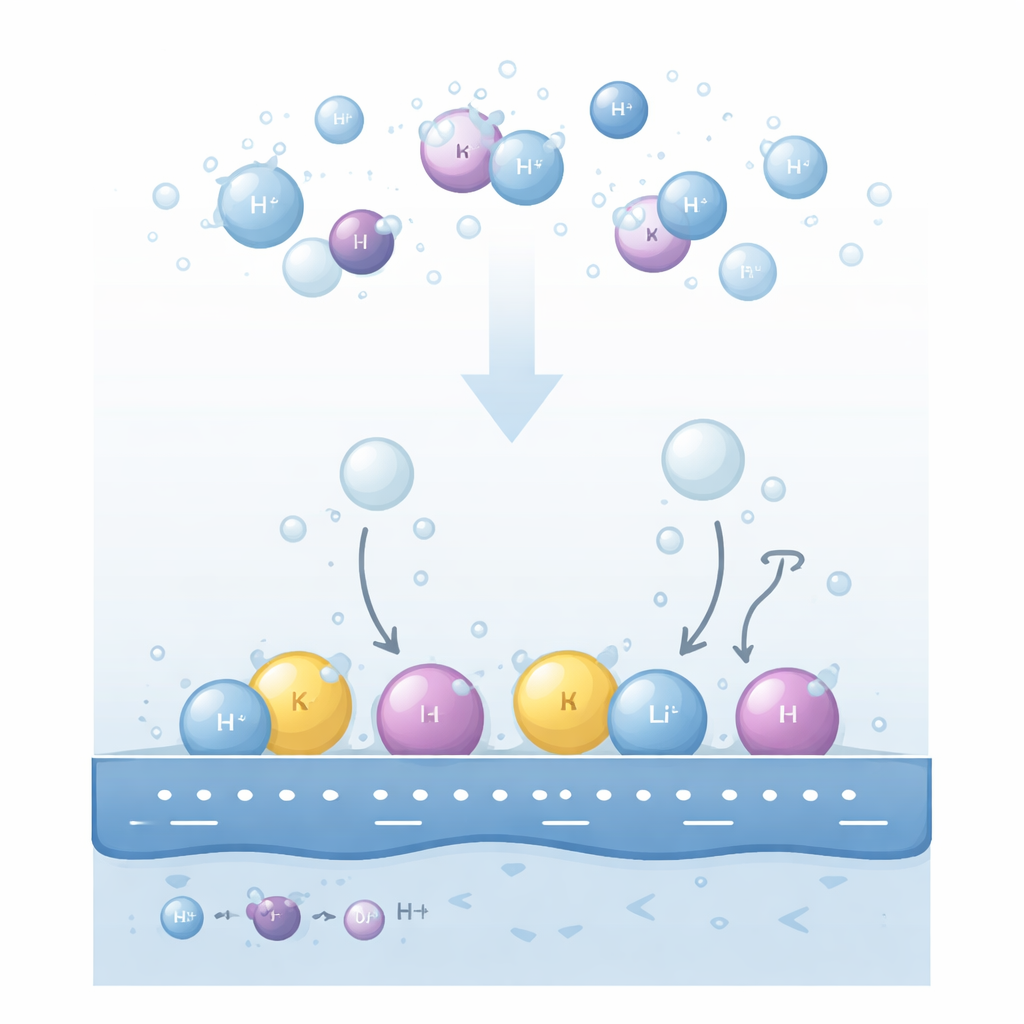
Dlaczego jony soli mają znaczenie przy elektrodach
Gdy do metalowej elektrody w roztworze alkalicznym przyłożone zostaje napięcie, cząsteczki wody blisko powierzchni rozpadają się, tworząc gazowy wodór. Eksperymenty od dawna wykazują, że zarówno rodzaj rozpuszczonego kationu (np. lit, sód czy potas), jak i jego stężenie mogą diametralnie zmieniać szybkość produkcji wodoru. Co bardziej zagadkowe, trendy te mogą się odwracać: na powierzchniach złota jedno uporządkowanie kationów widoczne jest przy łagodniejszych napięciach, lecz przy silniejszych ulega odwróceniu; zmiana pH roztworu lub stężenia kationu może przemienić pozornego promotora w inhibitor. Dotychczasowe wyjaśnienia skupiały się na sile wiązania wodoru z metalem lub na łatwości odprowadzania naładowanych cząstek, lecz te pomysły nie potrafiły konsekwentnie wytłumaczyć wszystkich obserwowanych odwróceń.
Dwie „okolicy” dla kationów
Autorzy proponują, że klucz tkwi w tym, gdzie kationy rzeczywiście zamieszkują w cienkiej warstwie cieczy przylegającej do elektrody. Wyróżniają dwie główne „okolicy”. Niektóre kationy pozostają całkowicie otoczone cząsteczkami wody i unoszą się nieco dalej od powierzchni w tzw. warstwie rozproszonej. Inne, wypychane przez silny ładunek ujemny metalu, częściowo zrzucają swoją powłokę wodną i przytulają się bezpośrednio do pierwszej warstwy wody międzyfazowej, tworząc zwartą, „specyficznie adsorbowaną” warstwę. Obie populacje kationów przekształcają lokalne pole elektryczne w przeciwny sposób. Kationy w warstwie rozproszonej wzmacniają pole odczuwane przez pobliskie cząsteczki wody, podczas gdy kationy adsorbowane częściowo ekranizują ładunek metalu i osłabiają to pole.
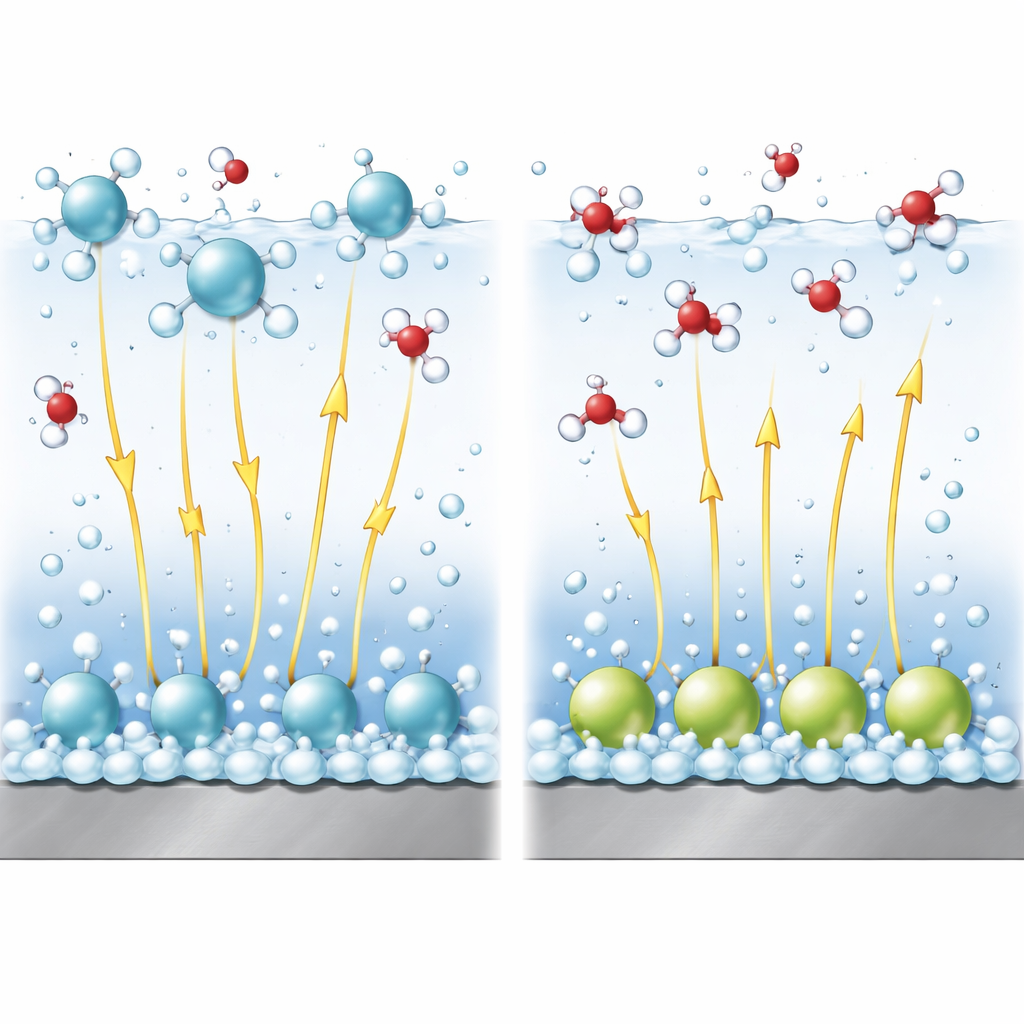
Pola elektryczne jako niewidzialne dźwignie
W roztworach zasadowych rozkład wody prowadzący do produkcji wodoru jest trudniejszy niż redukcja prostych protonów. Kluczowym elementem reakcji jest zerwanie wiązania wewnątrz cząsteczki wody. Silne pola elektryczne blisko powierzchni pomagają rozciągnąć i przerwać to wiązanie, podobnie jak pociąganie przeciwnych końców sprężyny. Wykorzystując udoskonalony model teoretyczny, autorzy łączą ułożenie kationów ze wzmocnieniem tego pola i z barierą energetyczną dla rozerwania wiązania. Pokazują, że kationy znajdujące się w warstwie rozproszonej mają tendencję do podnoszenia lokalnego potencjału w sposób sprzyjający reakcji i utrzymują silne pole elektryczne, co promuje powstawanie wodoru. Natomiast kationy specyficznie adsorbowane redukują efektywne pole w warstwie wodnej, gdzie zachodzi reakcja, utrudniając rozrywanie wiązania i spowalniając reakcję.
Wyjaśnianie mylących trendów eksperymentalnych
Pozwalając na przesunięcie równowagi między kationami rozproszonymi a adsorbowanymi w zależności od napięcia, pH, rozmiaru kationu i jego powinowactwa do powierzchni, model odtwarza szeroki zbiór zagadkowych danych. Na przykład jony potasu są słabiej hydratowane i bardziej podatne na adsorpcję niż jony litu. Przy umiarkowanych napięciach efekty rozmiaru i położenia sprawiają, że potas wydaje się korzystniejszy. Jednak przy silniejszych napięciach gęsta adsorpcja potasu tak skutecznie ekranizuje pole elektryczne, że lit staje się lepszym „pomocnikiem”, odwracając porządek aktywności. Podobnie, gdy zwiększa się stężenie soli litu, dominują kationy rozproszone i reakcja przyspiesza, ale wzrost stężenia sodu lub potasu faworyzuje kationy adsorbowane i spowalnia reakcję. Dostosowanie siły wiązania kationów w modelu również imituje różnice między materiałami elektrod i pH roztworu, odpowiadając obserwacjom na złocie i platynie w różnych warunkach zasadowych.
Co to oznacza dla przyszłych urządzeń
Mówiąc prościej, badanie ujawnia, że rozpuszczone kationy pełnią podwójną rolę w produkcji wodoru: mogą one albo „ciągnąć” cząsteczki wody, pomagając im się rozpaść, albo zagęszczać się przy powierzchni i tłumić samo pole elektryczne napędzające reakcję. To, którą twarz pokażą, zależy od ich rozmiaru, tego, jak mocno trzymają wodę, jak silnie wiążą się z elektrodą i od ich stężenia. Ta zunifikowana perspektywa pomaga wyjaśnić dekady mylących obserwacji i sugeruje nowe zasady projektowe dla elektrolizerów i pokrewnych technologii. Zamiast wybierać pojedynczy „najlepszy” kation, inżynierowie mogą dostosowywać mieszanki i warunki tak, aby większość kationów znajdowała się w odpowiedniej odległości od powierzchni — wystarczająco blisko, by wzmocnić pole elektryczne, ale nie tak mocno związana, by je stłumić.
Cytowanie: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Słowa kluczowe: reakcja ewolucji wodoru, elektryczna podwójna warstwa, kationy metali alkalicznych, elektroliza wody, elektrokataliza