Clear Sky Science · ru
Разгадка двуликого влияния катионов в электрокатализе
Двуликие помощники в чистой энергетике
Производство чистого водородного топлива из воды часто опирается на реакции на заряженных металлических поверхностях, погружённых в солёные растворы. Растворённые положительно заряженные ионы, или катионы, обычно рассматривают как пассивный фон. Эта статья показывает, что это далеко не так: те же катионы, которые в одних условиях ускоряют образование водорода, при чуть иных условиях могут его замедлять. Понимание этой двойственной природы важно для проектирования более эффективных электролизёров и других электрохимических технологий для перехода к низкоуглеродной энергетике.
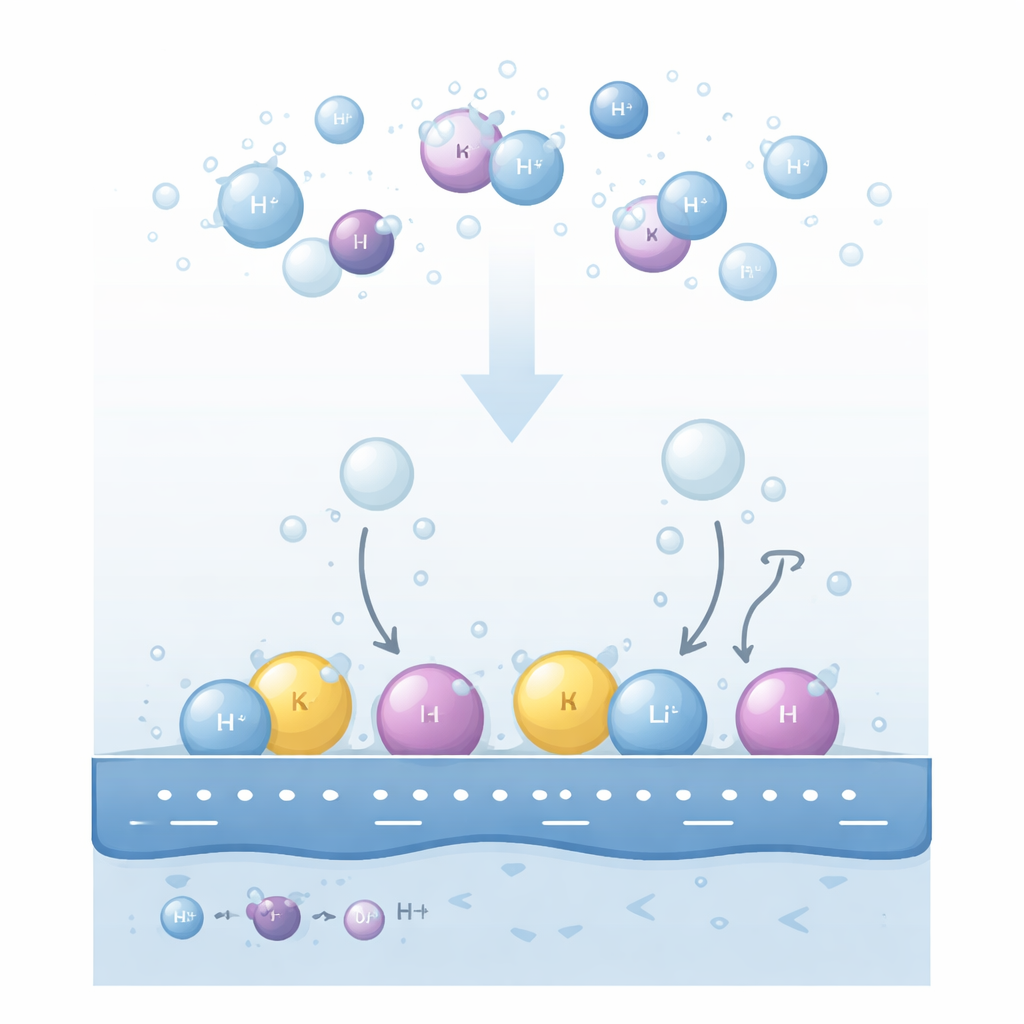
Почему ионы соли важны у электродов
Когда к металлическому электроду в щелочном растворе прикладывают напряжение, молекулы воды возле поверхности распадаются с образованием водорода. Эксперименты давно показали, что и тип растворённого катиона (например, литий, натрий или калий) и его концентрация могут сильно влиять на скорость выделения водорода. Ещё более загадочно: закономерности могут меняться местами — на золоте порядок активности катионов наблюдается один при слабых напряжениях, но при более сильных напряжениях он обращается; изменение pH раствора или концентрации катионов может превратить кажущегося способствуетеля в ингибитор. Существующие объяснения фокусировались на том, насколько сильно водород адсорбируется на металле, или на том, как легко зарядные частицы удаляются, но эти идеи не могли последовательно объяснить все наблюдаемые инверсии.
Два «района» для катионов
Авторы предлагают, что ключ к пониманию — в том, где именно катионы располагаются в тонком слое жидкости у электрода. Они выделяют два основных «района». Некоторые катионы остаются полностью окружёнными молекулами воды и располагаются немного отдалённо от поверхности в «диффузной» области. Другие, под действием сильного отрицательного заряда металла, частично теряют свою водную оболочку и плотно прилегают к первому слою интерфейсной воды, образуя компактный слой «специфически адсорбированных» ионов. Эти две популяции катионов по-разному перестраивают локальное электрическое поле. Диффузные катионы усиливают поле, воспринимаемое близлежащими молекулами воды, тогда как адсорбированные катионы частично экранируют заряд металла и ослабляют это поле.
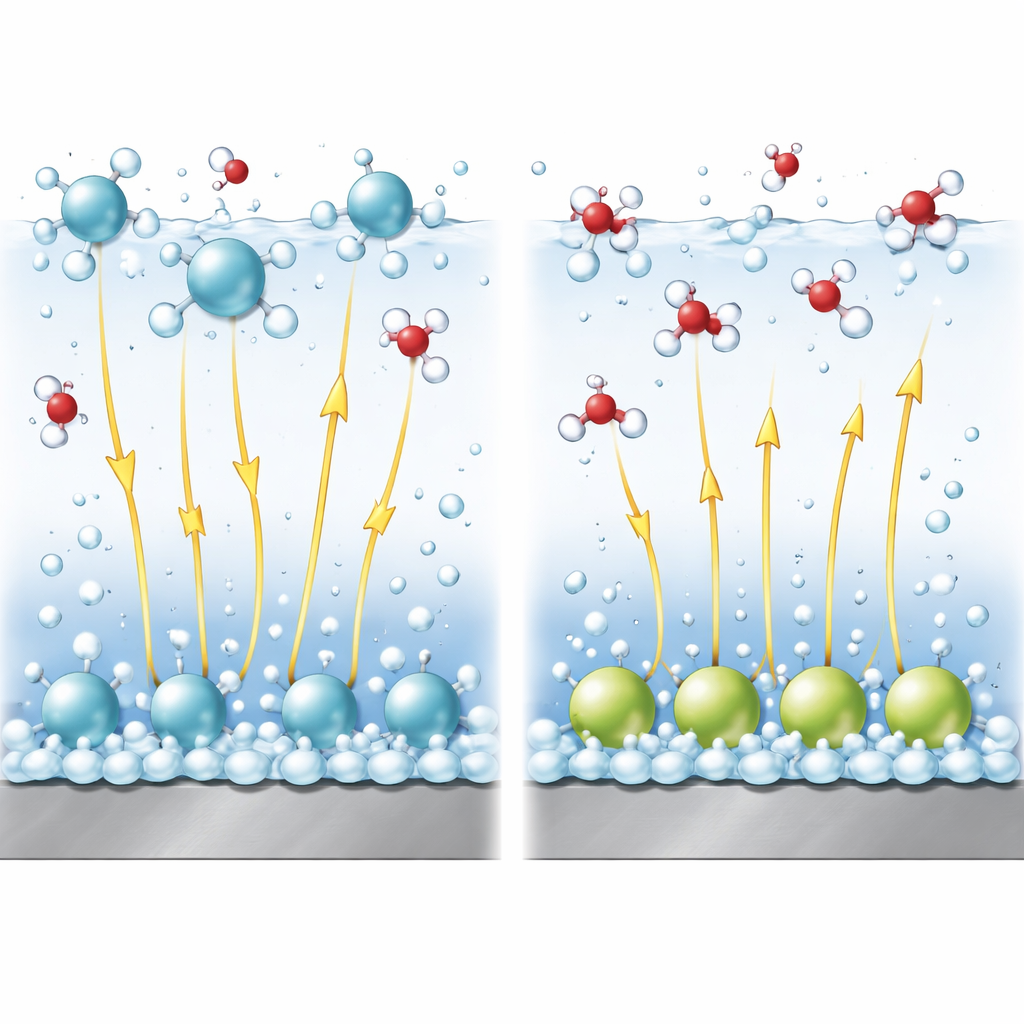
Электрические поля как невидимые рычаги
В щелочных растворах расщепление воды для образования водорода сложнее, чем восстановление простых протонов. Критическая часть реакции — разрыв связи внутри молекулы воды. Сильные электрические поля у поверхности помогают растягивать и разрывать эту связь, подобно тому как при натяжении пружины. Используя уточнённую теоретическую модель, авторы связывают расположение катионов с интенсивностью этого поля и с энергетическим барьером для разрыва связи. Они показывают, что катионы, находящиеся в диффузном слое, имеют тенденцию повышать локальный потенциал таким образом, что это благоприятствует реакции, и поддерживают сильное электрическое поле, таким образом стимулируя образование водорода. Напротив, специфически адсорбированные катионы снижают эффективное поле в водном слое, где протекает реакция, усложняя разрыв связи и замедляя реакцию.
Объяснение запутанных экспериментальных трендов
Позволяя соотношению между диффузными и адсорбированными катионами изменяться с напряжением, pH, размером катиона и его сродством к поверхности, модель воспроизводит широкий спектр загадочных данных. Например, ионы калия слабее гидратированы и более склонны к адсорбции, чем ионы лития. При умеренных напряжениях эффекты размера и положения делают калий более выгодным. Однако при более сильном напряжении плотная адсорбция калия так эффективно экранирует электрическое поле, что литий оказывается лучшим «помощником», и порядок активности меняется. Аналогично, при увеличении концентрации солей лития доминируют диффузные катионы и реакция ускоряется, тогда как повышение концентрации натрия или калия благоприятствует адсорбированным катионам и замедляет реакцию. Настройка силы связи катионов в модели также имитирует различия между материалами электродов и pH раствора, соответствуя экспериментальным наблюдениям на золоте и платине в разных щелочных условиях.
Что это значит для будущих устройств
Проще говоря, исследование показывает, что растворённые катионы играют двойную роль в образовании водорода: они либо «тянут» за молекулы воды, помогая им распасться, либо заполняют поверхность и заглушают то самое электрическое поле, которое приводит реакцию в действие. Каким лицом они предстанут, зависит от их размера, от того, насколько прочно они удерживают воду, как сильно они прилипают к электроду и насколько высока их концентрация. Эта единая картина помогает объяснить десятилетия запутанных наблюдений и предлагает новые правила проектирования для электролизёров и смежных технологий. Вместо того чтобы выбирать один «лучший» катион, инженеры могут настраивать смеси и условия так, чтобы большинство катионов располагались на оптимальном расстоянии от поверхности — достаточно близко, чтобы усилить электрическое поле, но не настолько прочно, чтобы его подавлять.
Цитирование: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Ключевые слова: реакция выделения водорода, электрический двойной слой, катионы щелочных металлов, электролиз воды, электрокатализ