Clear Sky Science · nl
Het ontwarren van de tweegezichtige effecten van kationen in elektrocatalyse
Tweezijdige helpers in schone energie
De productie van schone waterstofbrandstof uit water berust vaak op reacties aan geladen metalen oppervlakken die worden omspoeld door zoute oplossingen. De opgeloste positief geladen deeltjes, of kationen, worden meestal als passieve achtergrond beschouwd. Dit artikel laat zien dat ze dat allerminst zijn: dezelfde kationen die soms de waterstofproductie versnellen, kunnen onder iets andere omstandigheden juist vertragen. Het begrijpen van deze dubbele aard is essentieel voor het ontwerpen van betere electrolyzers en andere elektrochemische technologieën voor een laag-koolstof toekomst.
Waarom zoutionen ertoe doen bij elektroden
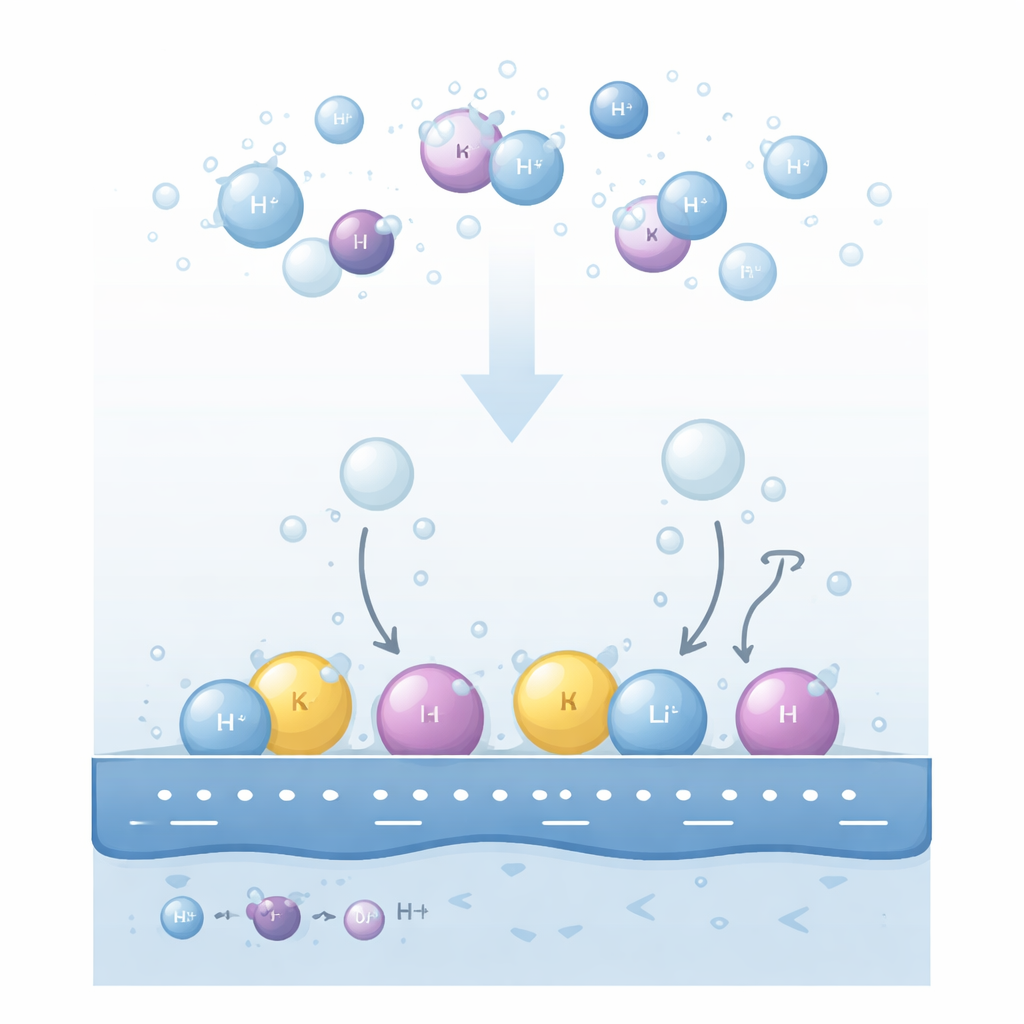
Als er een elektrische spanning op een metalelektrode in een alkalische oplossing wordt aangelegd, splitsen watermoleculen nabij het oppervlak om waterstofgas te vormen. Experimenteel is al lang bekend dat zowel het type opgeloste kation (zoals lithium, natrium of kalium) als de concentratie ervan drastisch kan veranderen hoe snel waterstof wordt geproduceerd. Nog verwarrender is dat de trends kunnen omslaan: op goudoppervlakken verschijnt één rangorde van kationen bij milde spanningen maar keert die om bij sterkere spanningen; het veranderen van de pH van de oplossing of de kationconcentratie kan een schijnbare bevorderaar in een remmer veranderen. Bestaande verklaringen richtten zich op hoe sterk waterstof aan het metaal hecht, of op hoe makkelijk geladen soorten wegbewegen, maar die ideeën konden niet consequent alle waargenomen omkeringen verklaren.
Twee buurten voor kationen
De auteurs stellen voor dat de kern ligt in waar kationen zich daadwerkelijk bevinden in de dunne vloeistoflaag naast de elektrode. Ze onderscheiden twee hoofd-buurten. Sommige kationen blijven volledig omringd door watermoleculen en zweven iets van het oppervlak in een “diffuse” regio. Andere, gedreven door een sterke negatieve lading op het metaal, geven gedeeltelijk hun waterschild op en nestelen zich vlak tegen de eerste laag interfaciaal water, waarmee ze een compacte “specifiek geadsorbeerde” laag vormen. Deze twee kationpopulaties herschikken het lokale elektrische veld op tegengestelde manieren. Diffuse kationen versterken het veld dat door nabijgelegen watermoleculen wordt gevoeld, terwijl geadsorbeerde kationen de lading van het metaal deels afschermen en dat veld verzwakken.
Elektrische velden als onzichtbare hefbomen
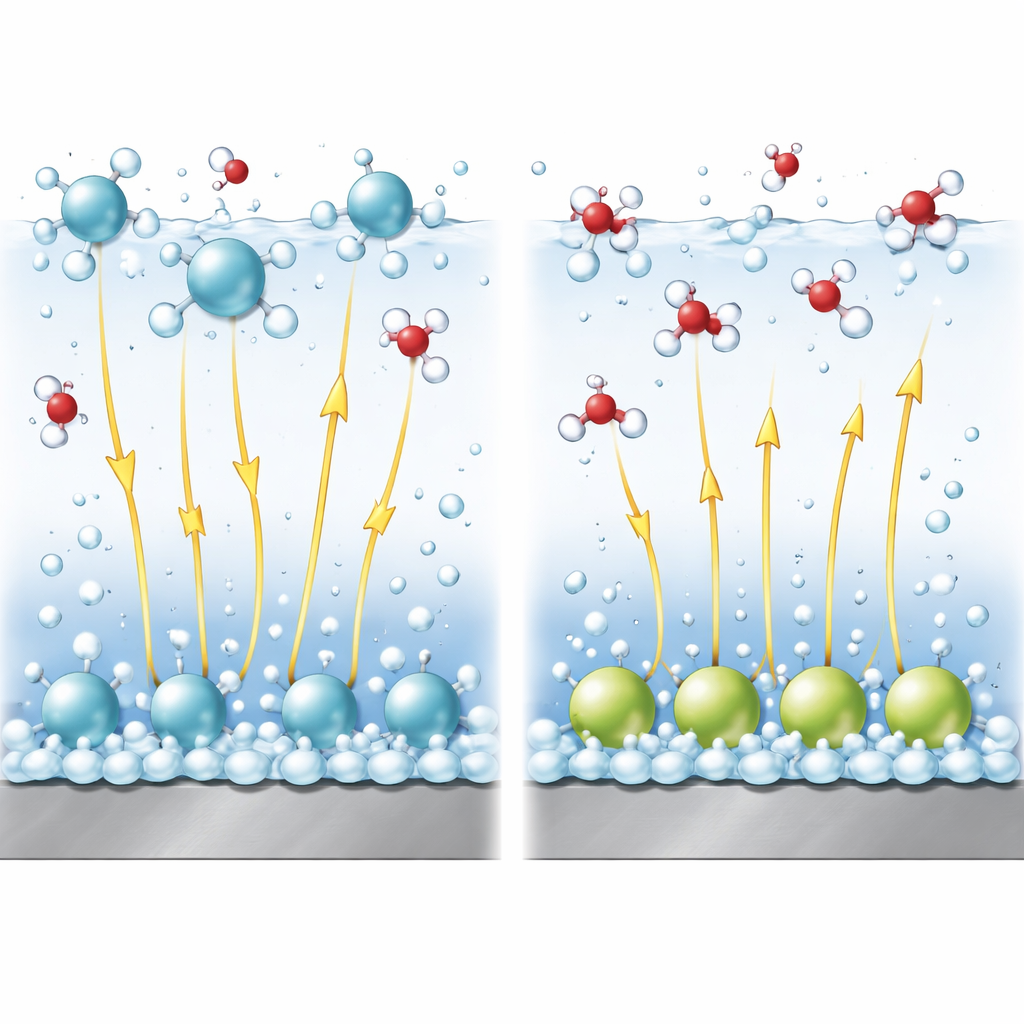
In alkalische oplossingen is het splitsen van water om waterstof te maken moeilijker dan het reduceren van eenvoudige protonen. Een cruciaal onderdeel van de reactie is het verbreken van de binding binnen een watermolecuul. Sterke elektrische velden nabij het oppervlak helpen deze binding te rekken en te breken, vergelijkbaar met het aan beide uiteinden van een veer trekken. Met een verfijnd theoretisch model koppelen de auteurs de ordening van kationen aan de sterkte van dit veld en aan de energiedrempel voor het verbreken van de binding. Ze tonen aan dat kationen die in de diffuse laag worden vastgehouden de lokale potentiaal op een manier verhogen die de reactie bevordert en het elektrische veld sterk houden, waardoor waterstofvorming wordt gestimuleerd. Daarentegen verminderen specifiek geadsorbeerde kationen het effectieve veld in de waterlaag waar de reactie plaatsvindt, wat het verbreken van de binding bemoeilijkt en de reactie vertraagt.
Verklaren van verwarrende experimentele trends
Door toe te staan dat de balans tussen diffuse en geadsorbeerde kationen verschuift met spanning, pH, kationgrootte en kation–oppervlakte-affiniteit, reproduceert het model een breed scala aan puzzelende gegevens. Zo zijn kaliumionen zwakker gehydrateerd en geneigd meer te adsorberen dan lithiumionen. Bij bescheiden spanningen lijken grootte- en positioneringseffecten kalium gunstiger te maken. Bij sterkere spanningen echter schermt dichte adsorptie van kalium het elektrische veld zo effectief af dat lithium de betere “helper” wordt, waardoor de activiteitvolgorde omkeert. Evenzo, wanneer de concentratie van lithiumzouten wordt verhoogd, domineren diffuse kationen en versnelt de reactie, maar het verhogen van natrium- of kaliumconcentratie bevordert geadsorbeerde kationen en vertraagt de reactie. Het aanpassen van hoe sterk kationen binden in het model bootst ook verschillen tussen elektrode-materialen en oplossing-pH na, wat experimenteel gedrag op goud en platina onder diverse alkalische omstandigheden verklaart.
Wat dit betekent voor toekomstige apparaten
Simpel gezegd onthult de studie dat opgeloste kationen een dubbele rol spelen bij waterstofproductie: ze kunnen watermoleculen aantrekken om hen te helpen uiteenvallen, of het oppervlak vullen en het elektrische veld dempen dat juist de reactie aandrijft. Welke kant ze laten zien hangt af van hun grootte, hoe stevig ze water vasthouden, hoe sterk ze aan de elektrode hechten en hoe geconcentreerd ze zijn. Dit eenduidige beeld helpt tientallen jaren aan verwarrende waarnemingen te verklaren en suggereert nieuwe ontwerpregels voor electrolyzers en verwante technologieën. In plaats van één "beste" kation te kiezen, kunnen ingenieurs mengsels en condities afstemmen zodat de meeste kationen zich op precies de juiste afstand van het oppervlak bevinden—sterk genoeg om het elektrische veld te versterken, maar niet zo gebonden dat ze het verstikken.
Bronvermelding: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Trefwoorden: waterstofontwikkelingsreactie, elektrische dubbele laag, alkalimetalkaationen, waterelektrolyse, elektrocatalyse