Clear Sky Science · pt
Desvendando os efeitos de duas faces dos cátions na eletrocatalise
Ajudantes de Duas Faces em Energia Limpa
A produção de combustível de hidrogênio limpo a partir da água frequentemente depende de reações em superfícies metálicas carregadas imersas em soluções salinas. Os átomos carregados positivamente dissolvidos, os cátions, costumam ser tratados como um pano de fundo passivo. Este artigo mostra que estão longe de ser passivos: os mesmos cátions que às vezes aceleram a produção de hidrogênio podem, sob condições ligeiramente diferentes, retardá‑la. Compreender essa dupla natureza é vital para projetar eletrólitos e outras tecnologias eletroquímicas melhores para um futuro de baixo carbono.
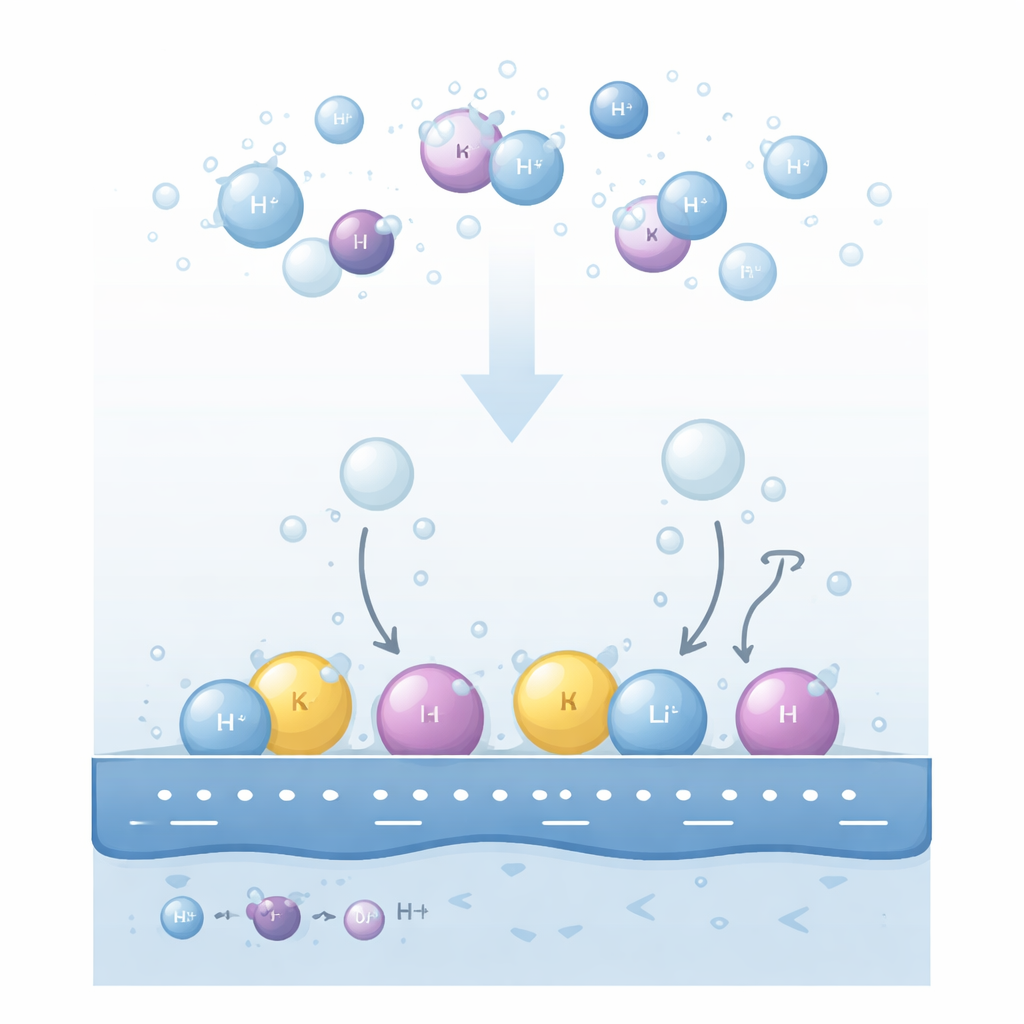
Por que os Íons do Sal Importam nos Eletrodos
Quando uma voltagem elétrica é aplicada a um eletrodo metálico em uma solução alcalina, moléculas de água próximas à superfície se rompem para formar gás hidrogênio. Experimentos mostram há muito tempo que tanto o tipo de cátion dissolvido (como lítio, sódio ou potássio) quanto sua concentração podem alterar dramaticamente a velocidade de produção de hidrogênio. Mais intrigante ainda, as tendências podem se inverter: em superfícies de ouro, uma ordem aparente de cátions aparece em voltagens moderadas, mas se inverte em voltagens mais fortes; mudar o pH da solução ou a concentração de cátions pode transformar um promotor aparente em um inibidor. Explicações existentes se concentraram em quão fortemente o hidrogênio se liga ao metal ou em quão facilmente espécies carregadas se afastam, mas essas ideias não conseguiram explicar de forma consistente todas as reversões observadas.
Dois Vizinhanças para os Cátions
Os autores propõem que a chave está em onde os cátions realmente residem na fina camada líquida próxima ao eletrodo. Eles distinguem duas vizinhanças principais. Alguns cátions permanecem totalmente envolvidos por moléculas de água e pairam um pouco afastados da superfície em uma região “difusa”. Outros, atraídos por uma forte carga negativa no metal, perdem parcialmente sua casca de água e se acomodam junto à primeira camada de água interfacial, formando uma camada compacta “especificamente adsorvida”. Essas duas populações de cátions reorganizam o campo elétrico local de maneiras opostas. Cátions difusos fortalecem o campo sentido pelas moléculas de água próximas, enquanto cátions adsorvidos parcialmente blindam a carga do metal e enfraquecem esse campo.
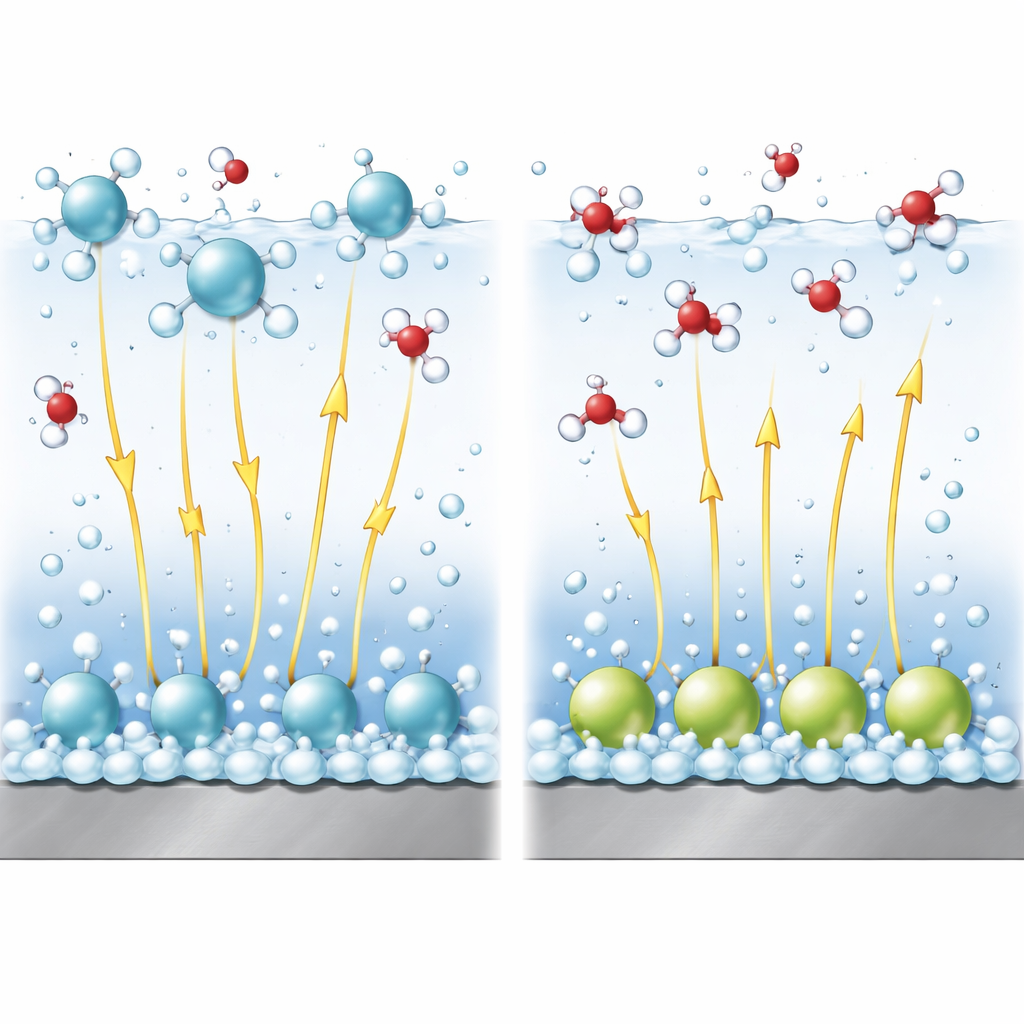
Campos Elétricos como Alavancas Invisíveis
Em soluções alcalinas, romper a água para produzir hidrogênio é mais difícil do que reduzir prótons simples. Uma parte crucial da reação é quebrar a ligação dentro de uma molécula de água. Campos elétricos fortes perto da superfície ajudam a alongar e romper essa ligação, como puxar as extremidades opostas de uma mola. Usando um modelo teórico refinado, os autores acoplam o arranjo dos cátions à intensidade desse campo e à barreira de energia para a quebra da ligação. Eles mostram que cátions mantidos na camada difusa tendem a elevar o potencial local de uma forma que favorece a reação e mantêm o campo elétrico forte, promovendo assim a formação de hidrogênio. Em contraste, cátions especificamente adsorvidos reduzem o campo efetivo na camada de água onde a reação ocorre, tornando a quebra de ligação mais difícil e desacelerando a reação.
Explicando Tendências Experimentais Confusas
Ao permitir que o equilíbrio entre cátions difusos e adsorvidos mude com a voltagem, pH, tamanho do cátion e afinidade cátion‑superfície, o modelo reproduz uma ampla gama de dados enigmáticos. Por exemplo, íons potássio são menos hidratados e mais propensos a se adsorver do que íons lítio. Em voltagens moderadas, efeitos de tamanho e posicionamento fazem o potássio parecer mais benéfico. Em voltagens mais altas, porém, a adsorção densa de potássio blinda o campo elétrico de forma tão eficaz que o lítio se torna o “ajudante” melhor, invertendo a ordem de atividade. De modo semelhante, quando a concentração de sais de lítio é aumentada, cátions difusos dominam e a reação acelera, mas aumentar a concentração de sódio ou potássio favorece cátions adsorvidos e retarda a reação. Ajustar quão fortemente os cátions se ligam no modelo também imita diferenças entre materiais de eletrodos e o pH da solução, correspondendo ao comportamento experimental em ouro e platina sob várias condições alcalinas.
O Que Isso Significa para Dispositivos Futuros
Em termos simples, o estudo revela que cátions dissolvidos desempenham um papel duplo na produção de hidrogênio: eles podem tanto puxar moléculas de água para ajudar na sua dissociação quanto lotar a superfície e abafar o próprio campo elétrico que impulsiona a reação. Que face eles mostram depende do tamanho dos cátions, de quão firmemente retêm água, de quão fortemente aderem ao eletrodo e de quão concentrados estão. Essa visão unificada ajuda a explicar décadas de observações confusas e sugere novas regras de projeto para eletrólitos e tecnologias relacionadas. Em vez de escolher um único cátion “melhor”, engenheiros podem ajustar misturas e condições para que a maioria dos cátions fique à distância certa da superfície — forte o bastante para reforçar o campo elétrico, mas não tão presa que o abafe.
Citação: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Palavras-chave: reação de evolução de hidrogênio, dupla camada elétrica, cátions de metais alcalinos, eletrólise da água, eletrocatalise