Clear Sky Science · it
Disinnescare gli effetti Janus dei cationi nell’elettrocatalisi
Aiutanti a doppia faccia nell’energia pulita
Produrre combustibile a idrogeno pulito dall’acqua spesso dipende da reazioni su superfici metalliche cariche immerse in soluzioni salate. Gli atomi carichi positivamente disciolti, o cationi, vengono di solito trattati come uno sfondo passivo. Questo articolo dimostra che non è affatto così: gli stessi cationi che talvolta accelerano la produzione di idrogeno possono, in condizioni lievemente diverse, rallentarla. Comprendere questa doppia natura è vitale per progettare elettrolizzatori e altre tecnologie elettrochimiche migliori per un futuro a basse emissioni di carbonio.
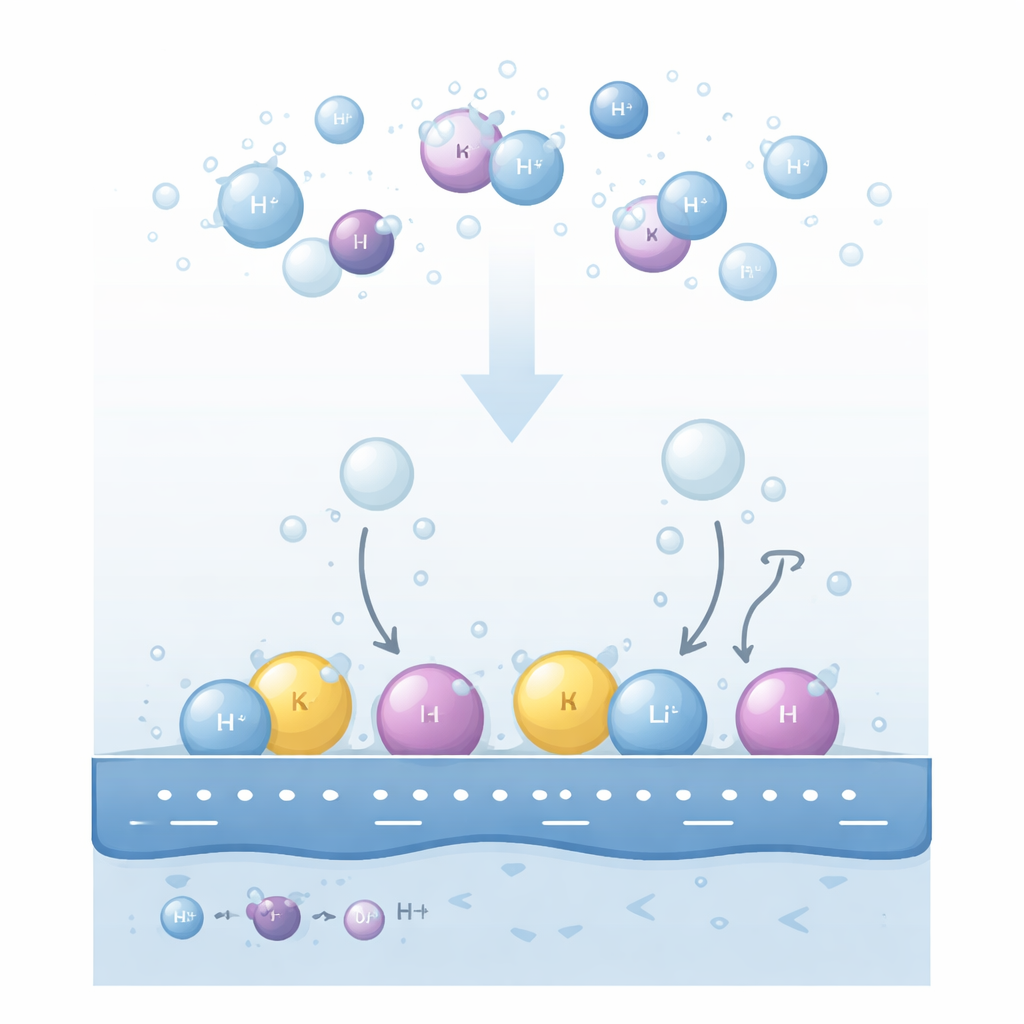
Perché gli ioni del sale contano agli elettrodi
Quando una tensione elettrica viene applicata a un elettrodo metallico in una soluzione alcalina, le molecole d’acqua vicino alla superficie si dissociano per formare gas idrogeno. Esperimenti hanno da tempo mostrato che sia il tipo di catione disciolto (come litio, sodio o potassio) sia la sua concentrazione possono cambiare drasticamente la velocità di produzione dell’idrogeno. Ancora più sconcertante, le tendenze possono invertire: su superfici d’oro, un ordine apparente di cationi compare a tensioni lievi ma si inverte a tensioni maggiori; cambiare il pH della soluzione o la concentrazione di cationi può trasformare un promotore apparente in un inibitore. Le spiegazioni esistenti si concentravano su quanto fortemente l’idrogeno si leghi al metallo, o su quanto facilmente le specie cariche si allontanino, ma queste idee non riuscivano a spiegare coerentemente tutte le inversioni osservate.
Due quartieri per i cationi
Gli autori propongono che la chiave risieda nel luogo in cui i cationi stanno effettivamente nello strato liquido sottile vicino all’elettrodo. Distinguono due neighborhood principali. Alcuni cationi rimangono completamente avvolti dalle molecole d’acqua e si trovano a una certa distanza dalla superficie in una regione «diffusa». Altri, spinti da una forte carica negativa sul metallo, perdono parzialmente il loro involucro d’acqua e si accostano alla prima barriera di acqua interfaciale, formando uno strato compatto «specificamente adsorbito». Queste due popolazioni di cationi riorganizzano il campo elettrico locale in modi opposti. I cationi diffusi rafforzano il campo percepito dalle molecole d’acqua vicine, mentre i cationi adsorbiti schermano parzialmente la carica del metallo e indeboliscono quel campo.
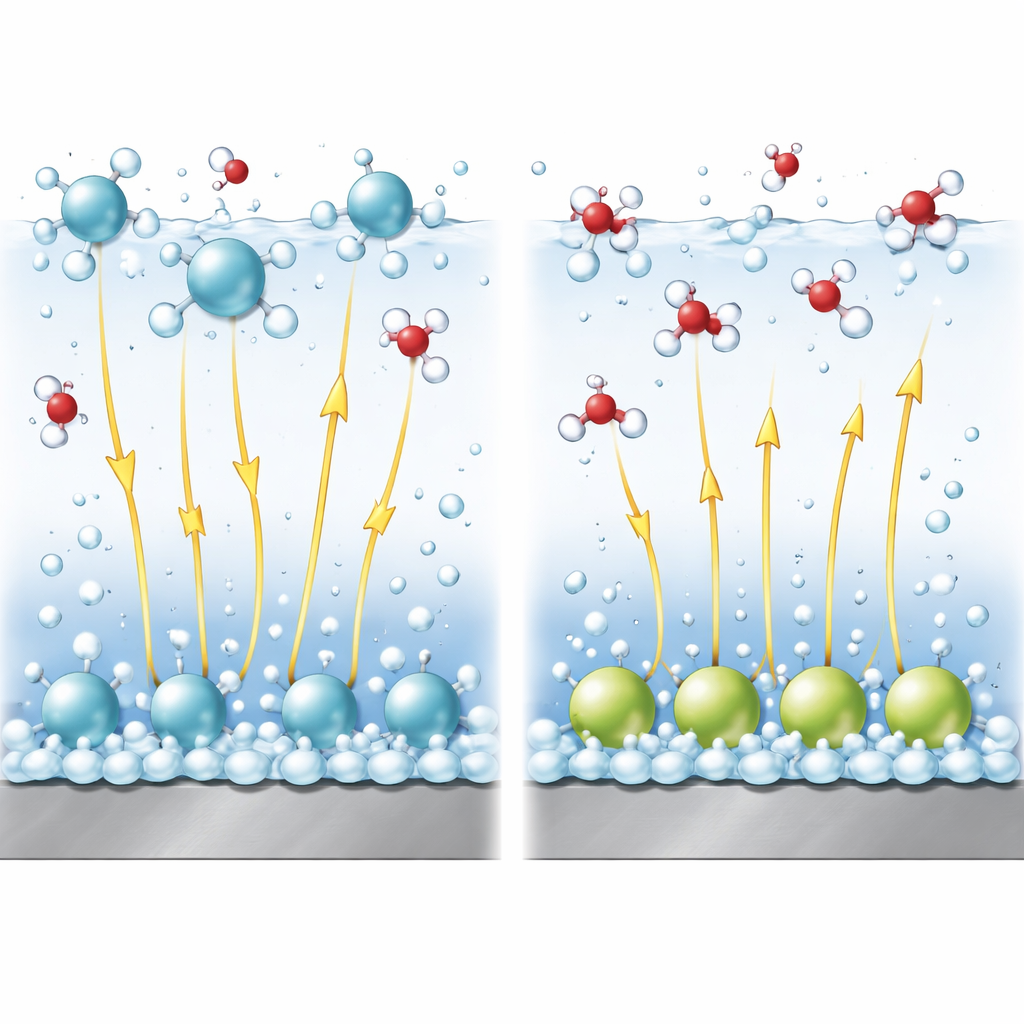
I campi elettrici come leve invisibili
In soluzioni alcaline, dissociare l’acqua per produrre idrogeno è più difficile che ridurre semplici protoni. Una parte cruciale della reazione è rompere il legame all’interno di una molecola d’acqua. Campi elettrici intensi vicino alla superficie aiutano a stirare e rompere questo legame, come tirare le estremità opposte di una molla. Usando un modello teorico raffinato, gli autori accoppiano l’assetto dei cationi all’intensità di questo campo e alla barriera energetica per la rottura del legame. Mostrano che i cationi trattenuti nello strato diffuso tendono ad alzare il potenziale locale in modo che favorisca la reazione e mantengano il campo elettrico forte, promuovendo così la formazione di idrogeno. Al contrario, i cationi specificamente adsorbiti riducono il campo efficace nello strato d’acqua dove avviene la reazione, rendendo più difficile la rottura del legame e rallentando la reazione.
Spiegare tendenze sperimentali confuse
Permettendo che l’equilibrio tra cationi diffusi e adsorbiti cambi con la tensione, il pH, la dimensione dei cationi e l’affinità catione–superficie, il modello riproduce un’ampia gamma di dati sconcertanti. Per esempio, gli ioni potassio sono meno idratati e più inclini ad adsorbirsi rispetto agli ioni litio. A tensioni moderate, effetti di dimensione e posizionamento fanno apparire il potassio più vantaggioso. A tensioni maggiori, però, l’adsorbimento denso del potassio schermando così efficacemente il campo elettrico che il litio diventa il «buon» aiutante, invertendo l’ordine di attività. Analogamente, quando la concentrazione di sali di litio aumenta, predominano i cationi diffusi e la reazione accelera, ma aumentare la concentrazione di sodio o potassio favorisce i cationi adsorbiti e rallenta la reazione. Regolare quanto fortemente i cationi si legano nel modello imita anche le differenze tra materiali dell’elettrodo e pH della soluzione, corrispondendo al comportamento sperimentale su oro e platino in varie condizioni alcaline.
Cosa significa per i dispositivi futuri
In termini semplici, lo studio rivela che i cationi disciolti giocano un doppio ruolo nella produzione di idrogeno: possono oppure tirare sulle molecole d’acqua per favorirne la dissociazione, oppure affollare la superficie e ovattare proprio il campo elettrico che guida la reazione. Quale lato mostrino dipende dalla loro dimensione, da quanto saldamente trattengono l’acqua, da quanto si attaccano all’elettrodo e da quanto sono concentrati. Questa visione unificata aiuta a spiegare decenni di osservazioni confuse e suggerisce nuove regole di progettazione per elettrolizzatori e tecnologie correlate. Piuttosto che scegliere un singolo catione “migliore”, gli ingegneri possono modulare miscele e condizioni in modo che la maggior parte dei cationi si collochi alla giusta distanza dalla superficie: abbastanza vicini da potenziare il campo elettrico, ma non così attaccati da soffocarlo.
Citazione: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Parole chiave: reazione di evoluzione dell’idrogeno, doppio strato elettrico, cationi degli alcoli alcalini, elettrolisi dell’acqua, elettrocatalisi