Clear Sky Science · sv
Att nysta upp de tvåsidiga effekterna av katjoner i elektrokatalys
Tvåsidiga hjälpare för ren energi
Att producera ren vätgas från vatten bygger ofta på reaktioner vid laddade metallytor som är nedsänkta i saltlösningar. De upplösta positivt laddade atomerna, katjonerna, behandlas ofta som en passiv bakgrund. Denna artikel visar att de är allt annat än det: samma katjoner som ibland snabbar upp vätgasproduktion kan under något andra förhållanden bromsa den. Att förstå denna dubbla natur är avgörande för att utforma bättre elektrolysörer och andra elektro-kemiska teknologier för en lågkoldioxidframtid.
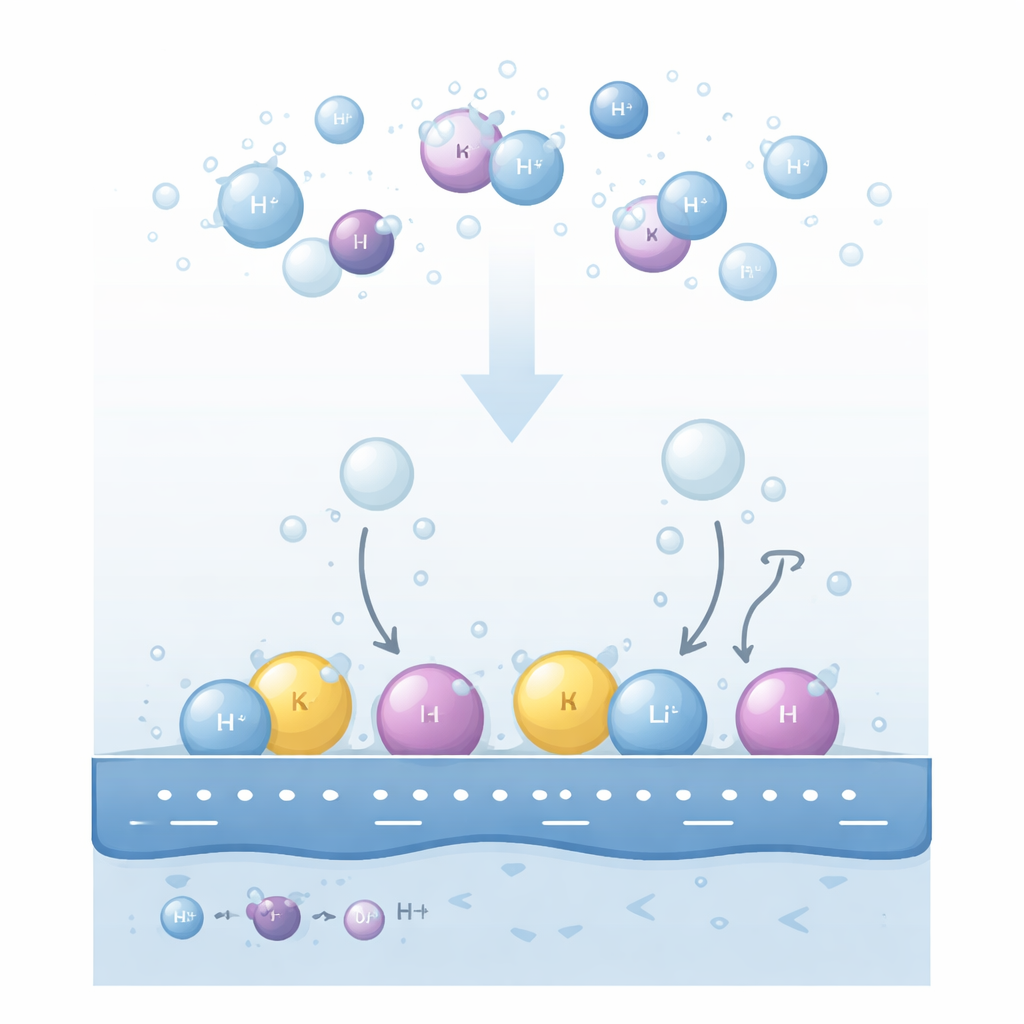
Varför saltjoner spelar roll vid elektroder
När en elektrisk spänning appliceras på en metallektrod i en alkalisk lösning splittras vattenmolekyler nära ytan för att bilda vätgas. Experiment har länge visat att både typen av upplöst katjon (till exempel litium, natrium eller kalium) och dess koncentration kan ändra hur snabbt vätgas bildas. Än mer förbryllande är att trenderna kan vända: på guldyta syns en ordning av katjoner vid låga spänningar men den inverteras vid starkare spänningar; att ändra lösningens pH eller katjonkoncentration kan förvandla en till synes främjande jon till en hämmande. Befintliga förklaringar fokuserade på hur starkt väte binder till metallen eller hur lätt laddade arter rör sig bort, men dessa idéer kunde inte konsekvent förklara alla observerade omsvängningar.
Två kvarter för katjoner
Författarna föreslår att nyckeln ligger i var katjonerna faktiskt befinner sig i det tunna vätskeskiktet intill elektroden. De skiljer mellan två huvudkvarter. Vissa katjoner förblir fullständigt omslutna av vattenmolekyler och svävar något bort från ytan i ett ”diffust” område. Andra, drivna av en stark negativ laddning på metallen, kastar delvis av sig vattenskalet och kryper ända fram till det första lagret av interfacialt vatten och bildar ett kompakt ”specifikt adsorberat” lager. Dessa två katjonpopulationer omarrangerar det lokala elektriska fältet åt motsatta håll. Diffusa katjoner förstärker fältet som vattenmolekyler i närheten upplever, medan adsorberade katjoner delvis skärmar av metallens laddning och försvagar det fältet.
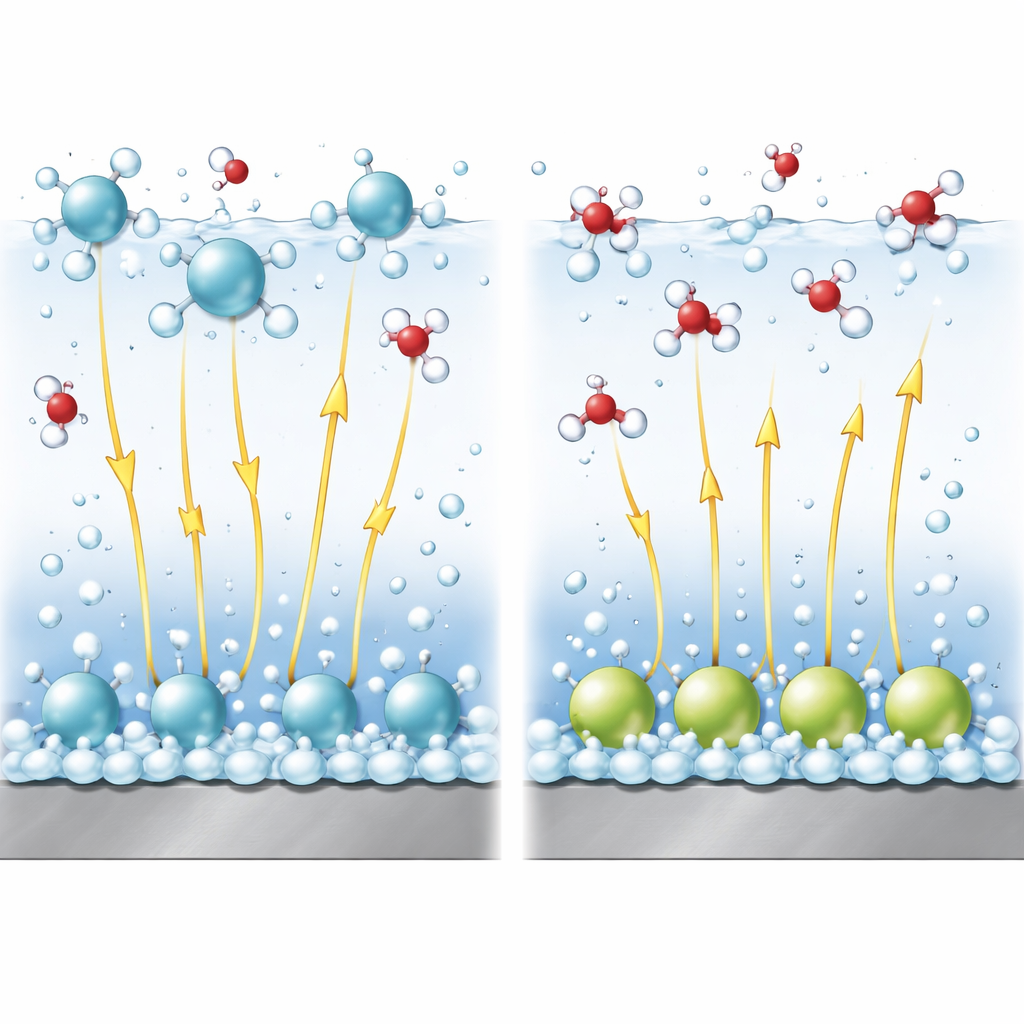
Elektriska fält som osynliga spakar
I alkalisk lösning är det svårare att dela vatten för att framställa vätgas än att reducera fria protoner. En avgörande del av reaktionen är att bryta bindningen inom en vattenmolekyl. Starka elektriska fält nära ytan hjälper till att töja och bryta denna bindning, ungefär som att dra i motsatta ändar av en fjäder. Med hjälp av en förfinad teoretisk modell kopplar författarna katjonernas arrangemang till styrkan i detta fält och till energibarriären för bindningsbrott. De visar att katjoner som hålls i det diffusa lagret tenderar att höja den lokala potentialen på ett sätt som gynnar reaktionen och behåller ett starkt elektriskt fält, vilket främjar vätgasbildning. Däremot minskar specifikt adsorberade katjoner det effektiva fältet i vattenlagret där reaktionen sker, vilket gör bindningsbrottet svårare och saktar ner reaktionen.
Förklaring av förvirrande experimentella trender
Genom att tillåta balansen mellan diffusa och adsorberade katjoner att skifta med spänning, pH, katjonstorlek och katjon–yt-affinitet återger modellen en rad förbryllande data. Till exempel är kaliumjoner svagare hydratiserade och mer benägna att adsorbera än litiumjoner. Vid måttliga spänningar gör storleksoch positionsskillnader att kalium verkar mer fördelaktigt. Vid starkare spänningar däremot skärmar tät adsorption av kalium det elektriska fältet så effektivt att litium blir den bättre ”hjälparen”, vilket vänder aktivitetsordningen. På samma sätt, när koncentrationen av litiumsalter höjs dominerar diffusa katjoner och reaktionen går snabbare, men att öka natrium- eller kaliumkoncentrationen gynnar adsorberade katjoner och saktar reaktionen. Att justera hur starkt katjoner binder i modellen efterliknar också skillnader mellan elektrodmaterial och lösningens pH och stämmer överens med experimentellt beteende på guld och platina i olika alkaliska förhållanden.
Vad detta betyder för framtida enheter
Enkelt uttryckt visar studien att upplösta katjoner spelar en dubbel roll i vätgasproduktion: de kan antingen dra i vattenmolekyler för att hjälpa dem att dela sig, eller tränga ihop ytan och dämpa det elektriska fält som driver reaktionen. Vilket ansikte de visar beror på deras storlek, hur tätt de håller i vatten, hur starkt de fäster vid elektroden och hur koncentrerade de är. Denna enhetliga bild hjälper till att förklara decennier av förvirrande observationer och föreslår nya designregler för elektrolysörer och närliggande teknologier. Istället för att välja en enda ”bästa” katjon kan ingenjörer anpassa blandningar och förhållanden så att de flesta katjoner hamnar på precis rätt avstånd från ytan — tillräckligt starka för att förstärka det elektriska fältet, men inte så fastsittande att de kväver det.
Citering: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
Nyckelord: väteutvecklingsreaktion, elektriskt dubbellager, alkalimetallkatjoner, vattenelektrolys, elektrokatalys