Clear Sky Science · ar
فك خيوط تأثيرات الأيونات ثنائية الوجوه في التحفيز الكهربائي
مُعينان ذو وجهين في الطاقة النظيفة
إنتاج وقود الهيدروجين النظيف من الماء يعتمد غالباً على تفاعلات عند أسطح معدنية مشحونة مغمورة في محاليل مالحة. تُعامل الذرات الموجبة المذابة، أو الكاتيونات، عادةً كخلفية غير فاعلة. يظهر هذا البحث أنها بعيدة عن ذلك: نفس الكاتيونات التي تُسرّع أحياناً إنتاج الهيدروجين قد تُبطئه تحت ظروف طفيفة الاختلاف. فهم هذه الطبيعة المزدوجة أمر حاسم لتصميم خلايا تحليل كهربائي ومحافظات كيميائية أفضل لتكنولوجيا منخفضة الكربون.
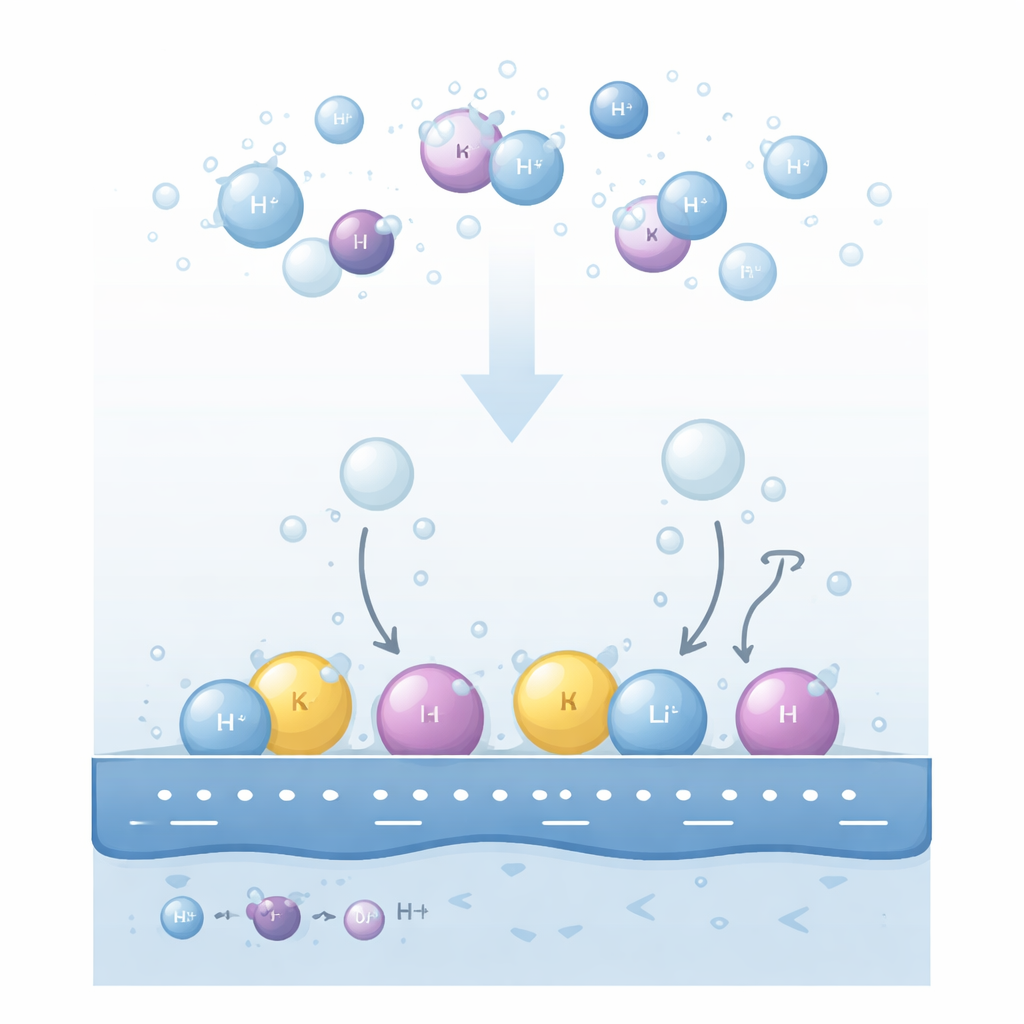
لماذا تهم أيونات الملح عند الأقطاب
عند تطبيق جهد كهربائي على قطب معدني في محلول قاعدي، تنشق جزيئات الماء قرب السطح لتكوّن غاز الهيدروجين. أظهرت التجارب منذ زمن أن نوع الكاتيون المذاب (مثل الليثيوم أو الصوديوم أو البوتاسيوم) وتركيزه يمكن أن يغيّرا بشكل كبير سرعة إنتاج الهيدروجين. والأكثر إرباكاً، أن الاتجاهات قد تنقلب: على أسطح الذهب، يظهر ترتيب معين للكاتيونات عند جهودة لطيفة لكنه ينقلب عند جهودة أقوى؛ تغيير الرقم الهيدروجيني للمحلول أو تركيز الكاتيون قد يحوّل محفزاً ظاهرياً إلى مثبط. التفسيرات القائمة ركزت على مدى ارتباط الهيدروجين بالمعدن، أو على سهولة تحرّك الشوارد المشحونة، لكن هذه الأفكار لم تستطع تفسير كل الانقلابات المرصودة باستمرار.
حارتان للكاتيونات
يقترح المؤلفون أن المفتاح يكمن في المكان الذي تعيش فيه الكاتيونات فعلياً داخل الطبقة السائلة الرقيقة المجاورة للقطب. يميزون بين حارتين رئيسيتين. تبقى بعض الكاتيونات مُحاطة بالكامل بجزيئات الماء وتطفو قليلاً بعيداً عن السطح في منطقة «مشتتة». أخرى، مدفوعة بشحنة سالبة قوية على المعدن، تتخلى جزئياً عن غلافها المائي وتلتصق بطبقة الماء البينية الأولى، مكونة طبقة «ممتزة خصوصياً» مدمجة. هاتان المجموعتان من الكاتيونات تعيدان ترتيب المجال الكهربائي المحلي بطرائق متعاكسة. الكاتيونات المشتتة تقوّي المجال الذي تشعر به جزيئات الماء القريبة، بينما الكاتيونات الممتزة تقلّص جزئياً شحنة المعدن وتضعف ذلك المجال.
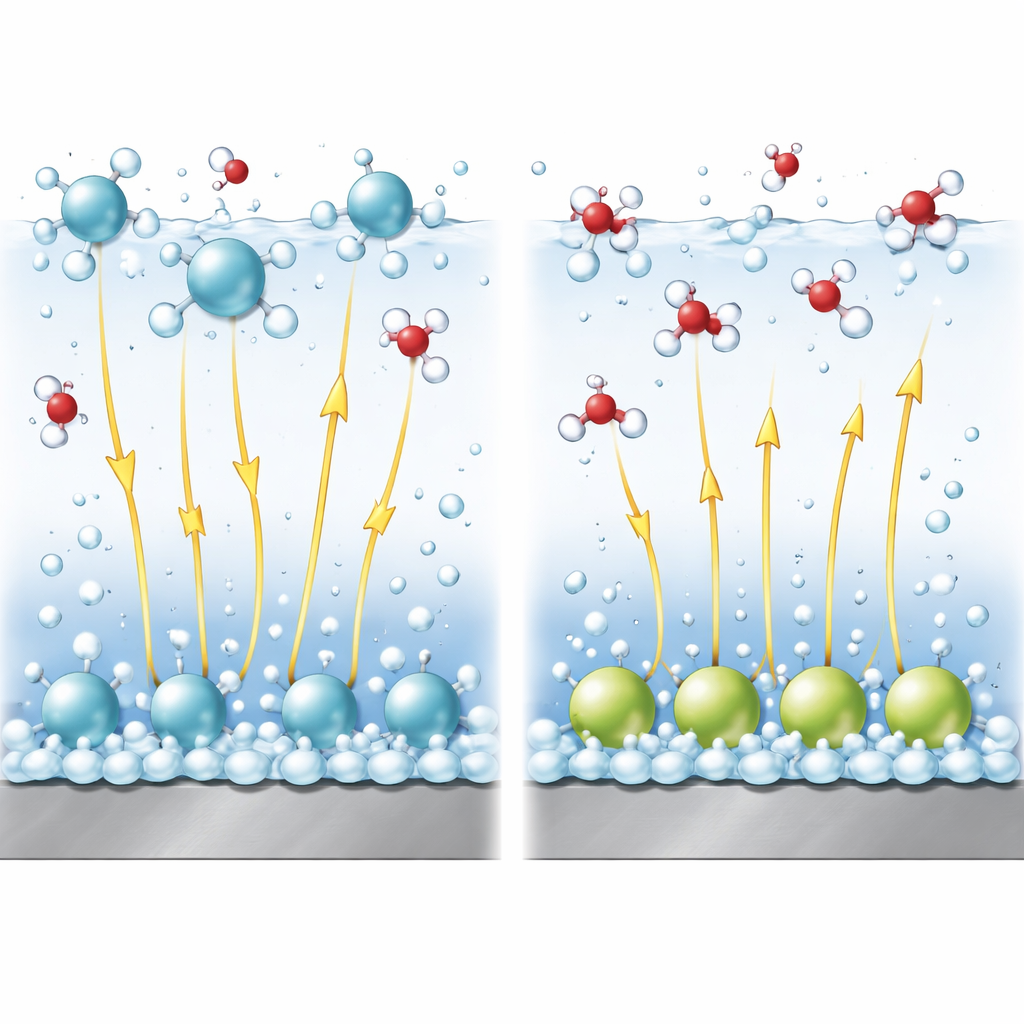
المجالات الكهربائية كرافعات غير مرئية
في المحاليل القاعدية، إنشقاق الماء لصنع الهيدروجين أصعب من اختزال البروتونات البسيطة. جزء حاسم من التفاعل هو كسر الرابطة داخل جزيء الماء. المجالات الكهربائية القوية قرب السطح تساعد على شد هذه الرابطة وكسرها، كجذب طرفي زنبرك متعاكسين. باستخدام نموذج نظري محسّن، يربط المؤلفون ترتيب الكاتيونات بشدة هذا المجال وبحاجز الطاقة لكسر الرابطة. يبينون أن الكاتيونات المحتجزة في الطبقة المشتتة تميل إلى رفع الجهد المحلي بطريقة تفضّل التفاعل وتحافظ على قوة المجال الكهربائي، وبالتالي تعزز تكوّن الهيدروجين. بالمقابل، تقلّل الكاتيونات الممتزة خصوصياً المجال الفعّال في طبقة الماء حيث يحدث التفاعل، مما يجعل كسر الرابطة أصعب ويبطئ التفاعل.
تفسير الاتجاهات التجريبية المحيرة
من خلال السماح لتوازن الكاتيونات المشتتة والممتزة بالتغير مع الجهد، الرقم الهيدروجيني، حجم الكاتيون، وألفة الكاتيون-السطح، يستنسخ النموذج مجموعة واسعة من البيانات المحيرة. على سبيل المثال، أيونات البوتاسيوم أقل ارتواءً بالماء وأكثر ميلاً للامتصاص من أيونات الليثيوم. عند جهودة متواضعة، تبدو تأثيرات الحجم والتموضع أن البوتاسيوم أكثر فائدة. لكن عند جهودة أقوى، يصبح امتزاز البوتاسيوم الكثيف فعّالاً جداً في حجب المجال الكهربائي فيصبح الليثيوم هو «المعين» الأفضل، فينعكس ترتيب الفاعلية. بالمثل، عندما يزداد تركيز أملاح الليثيوم، تهيمن الكاتيونات المشتتة ويتسارع التفاعل، بينما زيادة تركيز الصوديوم أو البوتاسيوم تُفضّل الكاتيونات الممتزة وتبطئ التفاعل. تعديل مدى ارتباط الكاتيونات في النموذج يحاكي أيضاً الفروقات بين مواد الأقطاب والرقم الهيدروجيني للمحلول، متطابقاً مع السلوك التجريبي على الذهب والبلاتين عبر ظروف قاعدية مختلفة.
ماذا يعني هذا لأجهزة المستقبل
بعبارات بسيطة، تكشف الدراسة أن الكاتيونات المذابة تلعب دوراً مضاعفاً في إنتاج الهيدروجين: فقد تسحب جزيئات الماء لمساعدتها على التفكك، أو تحتشد على السطح وتخمد المجال الكهربائي نفسه الذي يدفع التفاعل. الوجه الذي تظهره يعتمد على حجمها، وكمية الماء التي تحتفظ بها، ومدى التصاقها بالقطب، ومدى تركيزها. هذه الصورة الموحدة تفسر عقوداً من الملاحظات المربكة وتقترح قواعد تصميم جديدة لخلايا التحليل الكهربائية والتقنيات المرتبطة بها. بدلاً من اختيار كاتيون «أفضل» واحد، قد يقوم المهندسون بضبط الخلطات والظروف بحيث يتواجد معظم الكاتيونات على المسافة المناسبة من السطح — قوية بما يكفي لتعزيز المجال الكهربائي، لكن ليست ملتصقة لدرجة أنها تخنقه.
الاستشهاد: Zhu, X., Binninger, T., Koper, M.T.M. et al. Disentangling the Janus-faced effects of cations in electrocatalysis. Nat Commun 17, 3149 (2026). https://doi.org/10.1038/s41467-026-71126-3
الكلمات المفتاحية: تفاعل تطور الهيدروجين, الطبقة المزدوجة الكهربائية, أيونات الفلزات القلوية, تحليل الماء كهربياً, التحفيز الكهربائي