Clear Sky Science · tr
MYST asetiltransferazlarının hiyerarşik küçük molekül inhibisyonu
DNA üzerindeki küçük anahtarların kanser tedavisi için neden önemi var
Her hücrenin içinde, DNA üzerindeki kimyasal anahtarlar hangi genlerin açılıp kapandığını belirlemeye yardımcı olur. MYST asetiltransferazları adı verilen bir enzim grubu bu anahtarları ince ayarlar ve meme kanseri ile lösemi gibi kanserlerle ilişkilendirilmiştir. Bu çalışma, yeni ilaç moleküllerinin bu enzimleri kontrollü, adım adım nasıl açıp kapattığını inceliyor; bu da daha hassas kanser tedavileri tasarlamak ve devam eden klinik çalışmaları yorumlamak için ipuçları sunuyor.
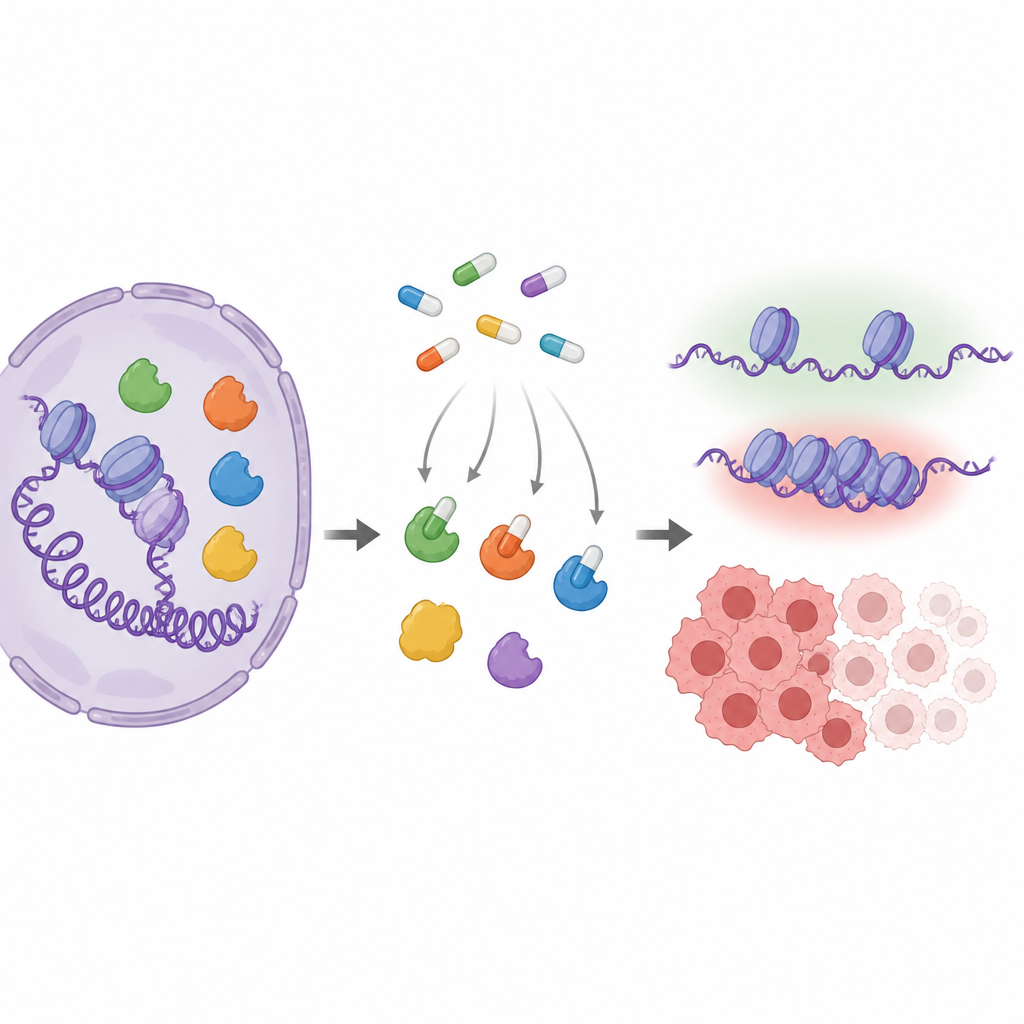
Gen etkinliğini ayarlayan kilit aktörler
MYST enzimleri, histon adı verilen proteinlere küçük kimyasal etiketler ekleyerek DNA paketlenmesini ince bir şekilde değiştirir. Bu paketleme, büyüme, onarım veya hormon yanıtı ile ilgili genlerin etkin olup olmayacağını belirlemeye yardımcı olur. Aile üyelerinden özellikle KAT6A ve KAT6B kanserlerde değişmiş veya fazla üretilmiş durumdadır; bu da onları çekici ilaç hedefleri yapar. İlaç şirketleri, bu enzimlerin aktif bölgesine uyan hap benzeri bileşikler geliştirdi, ancak farklı MYST enzimleri bu bölgede çok benzer göründüğü için hangi ilacın gerçek hücre içinde tam olarak hangi enzimleri hedeflediğini belirlemek zor olur.
Hangi ilacın hangi enzimi gerçekten hedeflediğini ölçmek
Yazarlar, önde gelen bir ilaç olan PF-9363 ve ilgili bileşiklerin MYST enzimleriyle nasıl etkileştiğini haritalamak için katmanlı bir test stratejisi kurdular. Önce, doğal yakıtlarını kullandıkları aynı cepte enzimleri yakalayan manyetik boncuklara bağlı bir "yem" molekülü kullandılar. Bir ilaç o cebi bloke ederse, enzim artık yeme yapışmaz. Hücrelerden elde edilen nükleer ekstraktlara artan ilaç dozları ekleyip ardından kitlenmeye devam eden proteinleri kütle spektrometrisi ile ölçerek açık bir hiyerarşi buldular: PF-9363 önce KAT6A ve KAT6B’yi yerinden eder, sonra KAT7’yi, ardından KAT8’i ve yalnızca en yüksek düzeylerde KAT5’i etkiler. Aynı desen, şu anda östrojen reseptör pozitif meme kanseri için denemelerde olan klinik ilaç PF-8144 için de görülüyor.
Gizli ortaklar ve net hücresel göstergeler bulmak
Enzim cebinin bloke edilmesi, yeme oturan bütün protein topluluklarının tutuşunu da zayıflattığı için ekip hangi diğer proteinlerin her MYST enzimiyle birlikte gittiğini görebildi. Bilinen kompleks üyeleriyle aynı doz deseninde yemden kaybolan proteinleri kümelendirerek ve bunu 3B yapı tahmini ve hücre deneyleriyle birleştirerek, özellikle KAT8 içeren NSL kompleksiyle bağlantılı olarak transkripsiyon faktörü FOXK2’yi önceden tanınmamış bir ortak olarak işaretlediler. Sonra canlı kanser hücrelerine geçip PF-9363 dozunu yükseltirken histonlardaki yüzlerce kimyasal işareti incelediler. Hangi MYST enziminin bloke edildiğini güvenilir şekilde bildiren küçük bir asetilasyon işareti seti belirlediler: KAT6A/B için histon H3 üzerinde bir işaret (H3K23Ac), KAT7 için H3 üzerinde bir diğer işaret (H3K14Ac), KAT8 için H4 üzerinde bir işaret (H4K16Ac) ve KAT5 için varyant histon H2A.Z üzerindeki işaretler. Bu işaretler gelişmiş kütle spektrometrisiyle veya standart antikor bazlı blotlarla ölçülebilir, bu da onları birçok laboratuvar için pratik kılar.
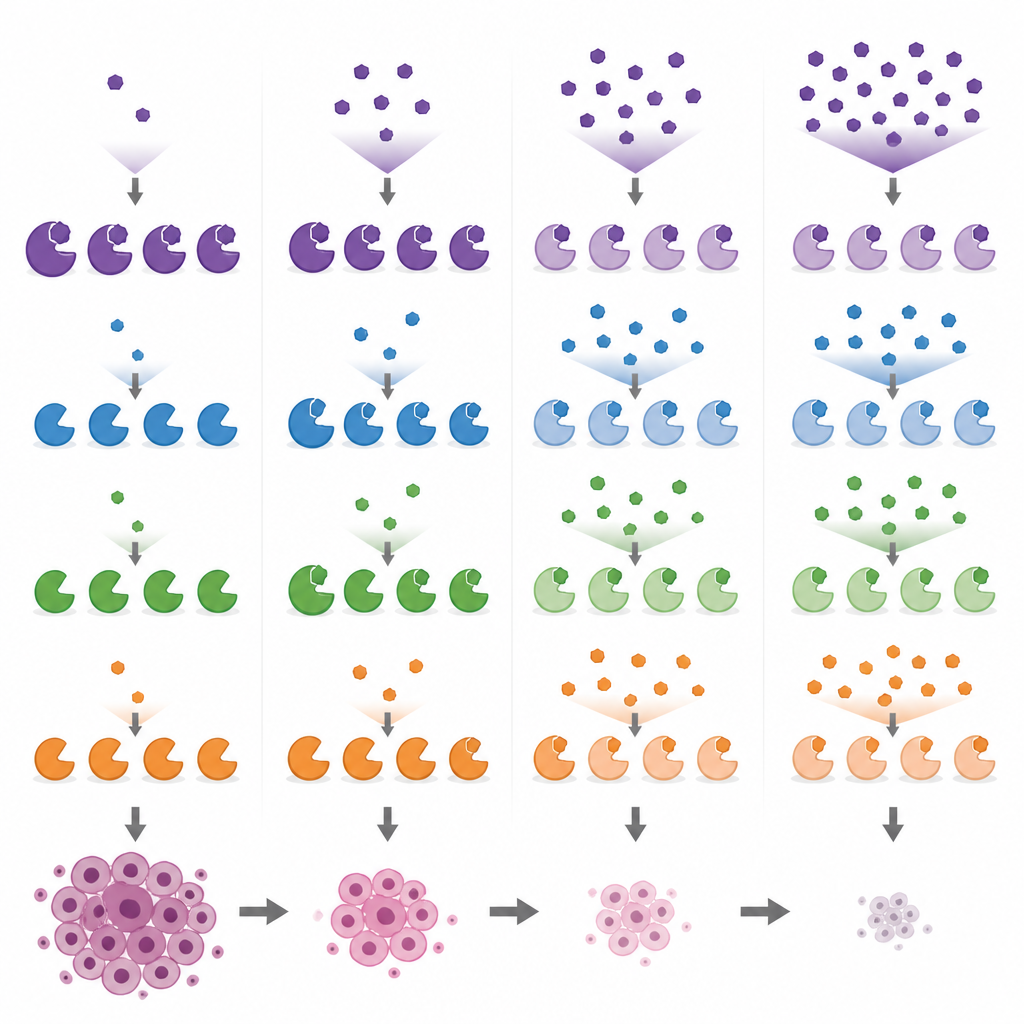
Popüler araştırma ilaçlarını ve yan hedeflerini karşılaştırmak
Bu biyobelirteç okumalarıyla donanmış olarak araştırmacılar, farklı doz aralıklarında meme kanseri hücrelerinde yaygın kullanılan birkaç MYST hedefleyici bileşiği karşılaştırdılar. PF-9363 ve klinik kuzeni PF-8144'ün ikisinin de aynı adım adım deseni izlediğini, nihayetinde daha yüksek dozlarda KAT8'i etkilediğini gösterdiler. Buna karşılık, WM-1119 yüksek konsantrasyonlarda bile KAT6A/B için son derece seçiciydi; WM-8014 ve WM-3835 ise önce KAT6A/B'yi, yalnızca sonra KAT7'yi engelliyordu. Test tüpü deneylerinde güçlü görünen MOZ-IN-3 isimli bir bileşik ise hücrelere iyi girmediği için hücrelerde az etki gösterdi. Bu karşılaştırmalar, tek bir enzim için özgün olarak pazarlanan bazı araçların aslında birkaç enzimi hedeflediğini ve bunun geçmiş ve gelecekteki deneylerin yorumlanmasını karmaşıklaştırabileceğini ortaya koyuyor.
Doz, enzim bağlantısı ve kanser hücresi büyümesi arasındaki ilişki
Ekip sonra bu katmanlı inhibisyon deseninin kanser hücrelerinin yanıtını şekillendirip şekillendirmediğini sordu. PF-9363'ü NCI-60 kanser hücresi paneli boyunca taramak, yalnızca KAT6A/B ve KAT7'yi bloke eden dozlara kısa maruziyetlerin büyüme üzerinde sınırlı etkileri olduğunu gösterdi. Güçlü, hızlı büyüme yavaşlamaları genellikle ancak KAT8'in—çoğu hücre için gerekli bir enzim—de etkinleştiği daha yüksek dozlarda ortaya çıktı. Özellikle KAT8'e bağımlı olan üçlü negatif bir meme kanseri hattında hücre sayısını küçülten doz, KAT8 ile bağlantılı histon işaretini tamamen baskılayan ve aynı zamanda KAT6A/B ile KAT7'yi de bloke eden doz ile eşleşti. Bu, bazı tümörler için bu ilaçların daha yüksek dozlarının yalnızca KAT6A/B üzerinden değil, daha geniş MYST inhibisyonu yoluyla etkili olabileceğini düşündürüyor.
Gelecekteki kanser ilaçları için bunun anlamı
Genel olarak çalışma, MYST enzimlerini hedefleyen küçük molekül engelleyicilerin birçok kinaz ilacı gibi davrandığını gösteriyor: düşük dozlarda ağırlıklı olarak tercih ettikleri hedefleri vuruyorlar, fakat doz arttıkça öngörülebilir bir sırayla yakından ilişkili diğer enzimlere yayılıyorlar. Her MYST üyesi için basit histon tabanlı okumalar sağlayarak ve popüler bileşiklerin nerede gerçekten seçici olduğunu açığa çıkararak çalışma, araştırmacıların ve klinisyenlerin dozu istenen enzim kapsamına göre eşleştirmeleri için bir araç takımı sunuyor. Bu, daha net laboratuvar çalışmaları tasarlamaya, klinik deneme sonuçlarını yorumlamaya ve nihayetinde gen kontrolünü kanser hücrelerinde yeniden şekillendirirken istenmeyen yan etkileri sınırlayan daha hassas terapilerin geliştirilmesine yardımcı olmalıdır.
Atıf: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Anahtar kelimeler: epigenetik enzimler, histon asetilasyonu, kanser ilacı hedeflemesi, kemoproteomik, lizin asetiltransferaz inhibitörleri