Clear Sky Science · sv
Hierarkisk hämning av MYST-acetyltransferaser med små molekyler
Varför små strömbrytare på DNA spelar roll för cancerbehandling
Inuti varje cell hjälper kemiska strömbrytare på vårt DNA till att bestämma vilka gener som slås på eller av. En grupp enzymer kallade MYST-acetyltransferaser finjusterar dessa omkopplare och har kopplats till cancerformer som bröstcancer och leukemi. Denna studie undersöker hur nya läkemedelsmolekyler kan dämpa eller stänga av dessa enzymer på ett kontrollerat, stegvis sätt, vilket ger ledtrådar för att utforma mer precisa cancerbehandlingar och för att tolka pågående kliniska prövningar.
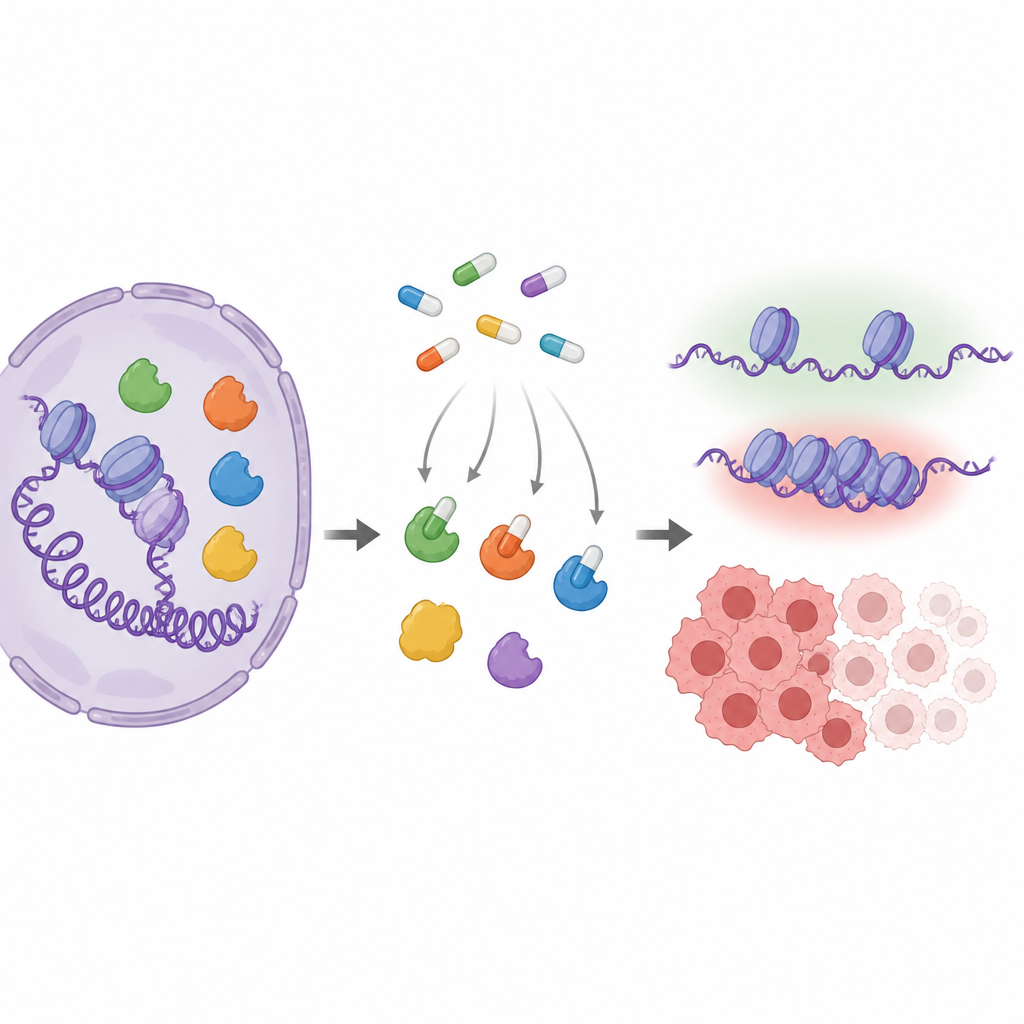
Nyckelspelare som stämmer av genaktivitet
MYST-enzymer förändrar subtilt hur DNA packas genom att fästa små kemiska märken på proteiner som kallas histoner. Denna paketering hjälper avgöra om gener som styr tillväxt, reparation eller hormonrespons är aktiva. Flera medlemmar i denna familj, särskilt KAT6A och KAT6B, är förändrade eller överproducerade i cancer, vilket gör dem till attraktiva läkemedelsmål. Läkemedelsföretag har utvecklat pillerlika föreningar som passar in i enzymernas aktiva säte, men eftersom de olika MYST-enzymerna ser mycket lika ut i detta säte är det svårt att veta exakt vilka som träffas av varje läkemedel inne i verkliga celler.
Mäta vilka enzymer varje läkemedel faktiskt träffar
Författarna byggde en flerskiktad teststrategi för att kartlägga hur en ledande substans, PF-9363, och relaterade föreningar interagerar med MYST-enzymer. Först använde de en "bete"-molekyl fäst vid magnetiska pärlor som fångar enzymer genom samma ficka där de använder sitt naturliga bränsle. Om ett läkemedel blockerar den fickan fäster enzymet inte längre vid betet. Genom att tillsätta ökande läkemedelsdoser till nukleära extrakt från celler och sedan mäta med masspektrometri vilka proteiner som fortfarande band till betet, fann de en tydlig hierarki: PF-9363 förflyttar först KAT6A och KAT6B, sedan KAT7, därefter KAT8, och först vid de högsta nivåerna KAT5. Samma mönster ses för det kliniska läkemedlet PF-8144, som nu prövas vid östrogenreceptorpositiv bröstcancer.
Hitta dolda partners och tydliga cellulära avläsningar
Eftersom blockering av enzymfickan också försvagar bindningen av hela proteinkomplex som sitter på betet, kunde teamet se vilka andra proteiner som följer med varje MYST-enzym. Genom att klustra proteiner som förlorades från betet med samma dosmönster som kända komplexmedlemmar, och sedan kombinera detta med 3D-strukturprediktion och cellexperiment, pekade de ut transkriptionsfaktorn FOXK2 som en tidigare oigenkänd partner, särskilt kopplad till KAT8-innehållande NSL-komplexet. Nästa steg var levande cancerceller där de undersökte hundratals kemiska märken på histoner när de ökade PF-9363-dosen. De identifierade en liten uppsättning acetyleringsmärken som pålitligt rapporterar vilket MYST-enzym som blockerats: en markering på histon H3 (H3K23Ac) för KAT6A/B, en annan på H3 (H3K14Ac) för KAT7, en på H4 (H4K16Ac) för KAT8, samt markeringar på varianthiston H2A.Z för KAT5. Dessa markörer kan mätas antingen med avancerad masspektrometri eller med vanliga antikroppsbaserade blottingmetoder, vilket gör dem praktiska för många laboratorier.
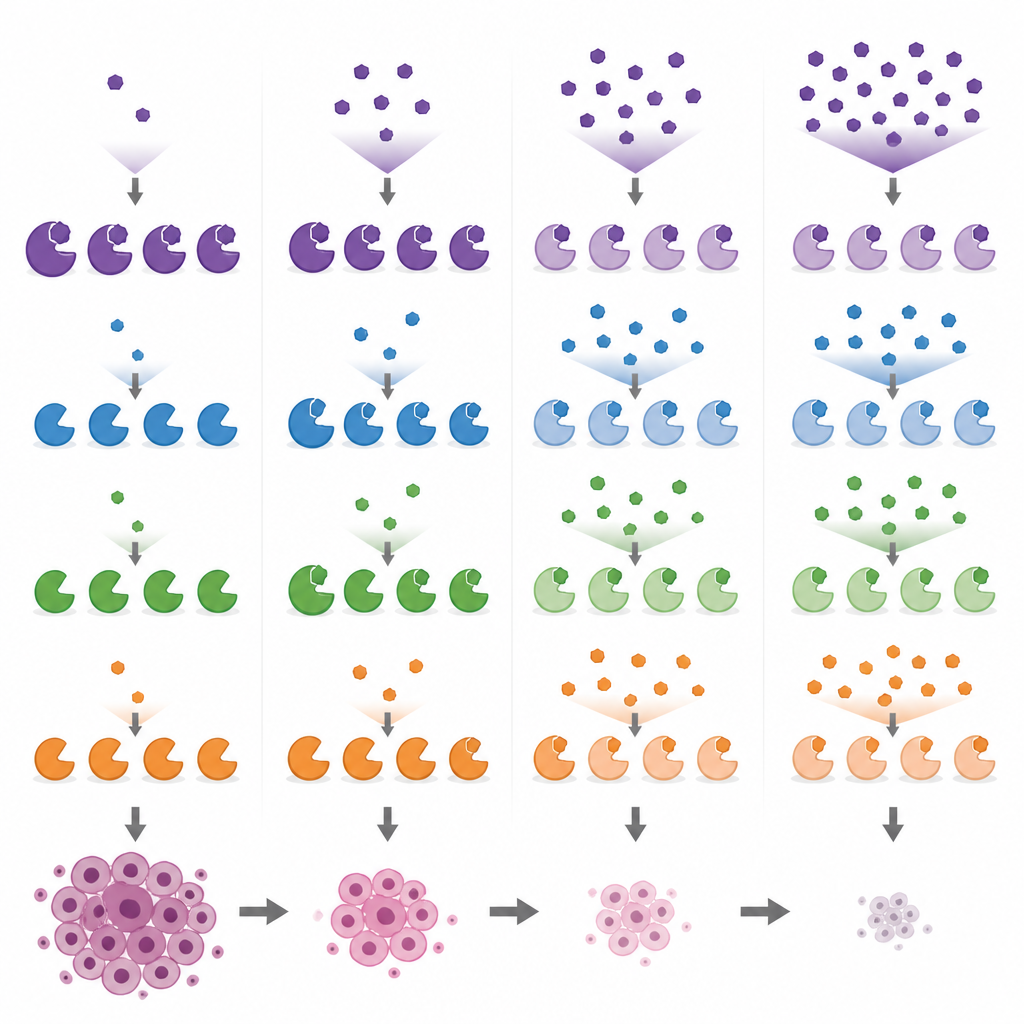
Jämförelse av populära forskningsläkemedel och deras sido-mål
Utrustade med dessa biomarköravläsningar jämförde forskarna flera vida använda MYST-riktade föreningar i bröstcancerceller över ett spektrum av doser. De visade att PF-9363 och dess kliniska kusin PF-8144 båda följer samma stegvisa mönster och så småningom påverkar KAT8 vid högre doser. Däremot visade WM-1119 sig vara mycket selektiv för KAT6A/B även vid höga koncentrationer, medan WM-8014 och WM-3835 hämmar KAT6A/B först och först därefter KAT7. En förening, MOZ-IN-3, som verkar potent i provrörsassay visade liten effekt i celler, troligen eftersom den inte tar sig in i dem väl. Dessa jämförelser avslöjar att vissa verktyg som marknadsförs som specifika för ett enzym faktiskt träffar flera, vilket kan försvåra tolkningen av tidigare och framtida experiment.
Koppla dos, enzymengagemang och cancercelltillväxt
Teamet undersökte sedan om detta flerskiktade hämningsmönster påverkar hur canceller svarar. Screening av PF-9363 över NCI-60-panelen av cancercellinjer visade att korta exponeringar för doser som endast blockerar KAT6A/B och KAT7 ger måttliga effekter på tillväxt. Kraftiga, snabba tillväxtsänkningar uppträdde i regel först vid högre doser där även KAT8, ett enzym som är viktigt för de flesta celler, engagerades. I en trippelnegativ bröstcancerlinje som särskilt är beroende av KAT8 matchade dosen som minskade cellantalet den dos som fullt ut undertryckte det KAT8-kopplade histonmärket samtidigt som KAT6A/B och KAT7 också blockerades. Detta tyder på att för vissa tumörer kan högre doser av dessa läkemedel verka genom bredare MYST-hämning snarare än genom KAT6A/B ensam.
Vad detta betyder för framtida cancerläkemedel
Sammantaget visar studien att småmolekylära blockare av MYST-enzymer beter sig mycket likt många kinasehämmare: vid låga doser träffar de främst sina föredragna mål, men när dosen ökar sprider de sig till närbesläktade enzymer i en förutsägbar ordning. Genom att tillhandahålla enkla histonbaserade avläsningar för varje MYST-medlem och genom att avslöja var populära föreningar verkligen är selektiva, erbjuder arbetet forskare och kliniker ett verktyg för att matcha dos med önskad enzymtäckning. Detta bör hjälpa till att utforma klarare laboratoriestudier, tolka kliniska prövningsresultat och i slutändan vägleda utvecklingen av mer precisa terapier som omformar genreglering i cancerceller samtidigt som oönskade biverkningar begränsas.
Citering: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Nyckelord: epigenetiska enzymer, histonacetylering, riktning av cancerläkemedel, kemoproteomik, hämmare av lysinacetyltransferaser