Clear Sky Science · de
Hierarchische Hemmung von MYST-Acetyltransferasen durch kleinmolekulare Inhibitoren
Warum winzige Schalter auf der DNA für die Krebsbehandlung wichtig sind
In jeder Zelle helfen chemische Schalter auf unserer DNA dabei zu entscheiden, welche Gene an- oder abgeschaltet werden. Eine Enzymgruppe namens MYST-Acetyltransferasen verfeinert diese Schalter und steht in Verbindung mit Krebsarten wie Brustkrebs und Leukämie. Diese Studie untersucht, wie neue Wirkstoffmoleküle diese Enzyme kontrolliert und schrittweise ein- oder ausschalten können, und liefert Hinweise für die Entwicklung präziserer Krebstherapien sowie für die Interpretation laufender klinischer Studien.
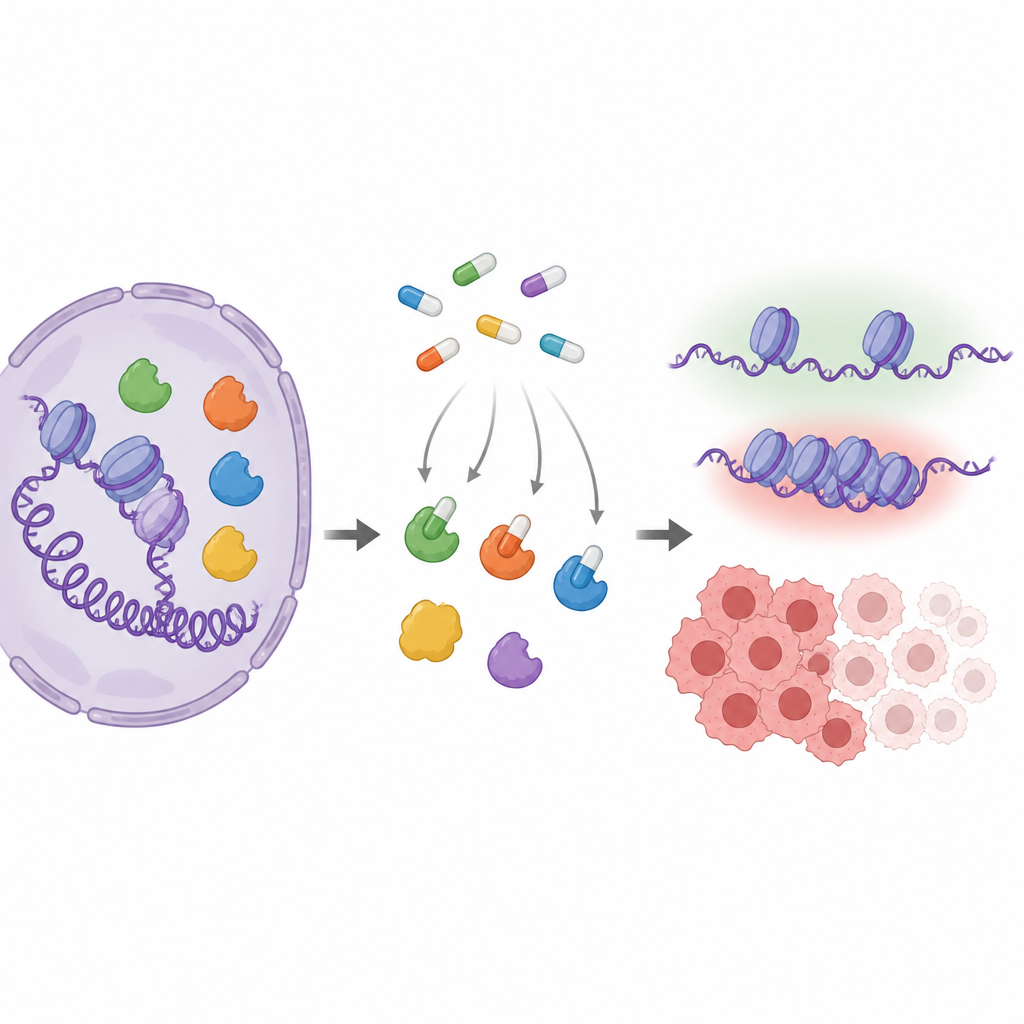
Wichtige Akteure, die die Genaktivität einstellen
MYST-Enzyme verändern auf subtile Weise, wie DNA verpackt ist, indem sie kleinen chemischen Gruppen an Proteine, die Histone genannt werden, anfügen. Diese Verpackung beeinflusst, ob Gene für Wachstum, Reparatur oder Hormonantwort aktiv sind. Mehrere Mitglieder dieser Familie, insbesondere KAT6A und KAT6B, sind in Krebs verändert oder überproduziert, was sie zu attraktiven Wirkstoffzielen macht. Pharmafirmen haben tablettenfähige Verbindungen entwickelt, die in die aktive Tasche dieser Enzyme passen. Da jedoch die verschiedenen MYST-Enzyme an dieser Stelle sehr ähnlich aussehen, ist es schwierig zu wissen, welche Enzyme ein Wirkstoff in echten Zellen tatsächlich trifft.
Messen, welche Enzyme ein Wirkstoff wirklich trifft
Die Autoren entwickelten eine gestufte Teststrategie, um abzubilden, wie ein führender Wirkstoff, PF-9363, und verwandte Verbindungen mit MYST-Enzymen interagieren. Zuerst nutzten sie ein „Köder“-Molekül, das an magnetische Beads gebunden ist und Enzyme über dieselbe Tasche anzieht, die sie mit ihrem natürlichen Cofaktor nutzen. Blockiert ein Wirkstoff diese Tasche, haftet das Enzym nicht mehr am Köder. Durch Zugabe steigender Wirkstoffdosen zu nuklearen Extrakten aus Zellen und anschließender Messung per Massenspektrometrie, welche Proteine noch am Köder banden, fanden sie eine klare Hierarchie: PF-9363 verdrängt zuerst KAT6A und KAT6B, dann KAT7, anschließend KAT8 und erst bei den höchsten Konzentrationen KAT5. Dasselbe Muster zeigt auch das klinische Präparat PF-8144, das derzeit bei östrogenrezeptorpositivem Brustkrebs geprüft wird.
Verborgene Partner finden und klare zelluläre Messgrößen
Weil das Blockieren der Enzymtasche auch den Zusammenhalt ganzer Proteinkomplexe schwächt, die am Köder sitzen, konnte das Team sehen, welche anderen Proteine mit jedem MYST-Enzym gemeinsam unterwegs sind. Durch das Clustern von Proteinen, die in demselben Dosis-Muster wie bekannte Komplexmitglieder vom Köder verloren gingen, und die Kombination dieser Daten mit 3D-Strukturvorhersagen und Zellversuchen, identifizierten sie den Transkriptionsfaktor FOXK2 als zuvor unerkannten Partner, insbesondere in Verbindung mit dem KAT8-haltigen NSL-Komplex. Anschließend untersuchten sie lebende Krebszellen und erfassten Hunderte chemischer Histonmarken bei steigender PF-9363-Dosis. Sie bestimmten eine kleine Gruppe von Acetylierungsmarken, die zuverlässig anzeigen, welches MYST-Enzym blockiert ist: eine Marke an Histon H3 (H3K23Ac) für KAT6A/B, eine weitere an H3 (H3K14Ac) für KAT7, eine an H4 (H4K16Ac) für KAT8 und Marken an der Variantenform H2A.Z für KAT5. Diese Marken lassen sich entweder mit hochauflösender Massenspektrometrie oder mit standardmäßigen Antikörper-basierten Blots messen, was sie für viele Labore praktisch macht.
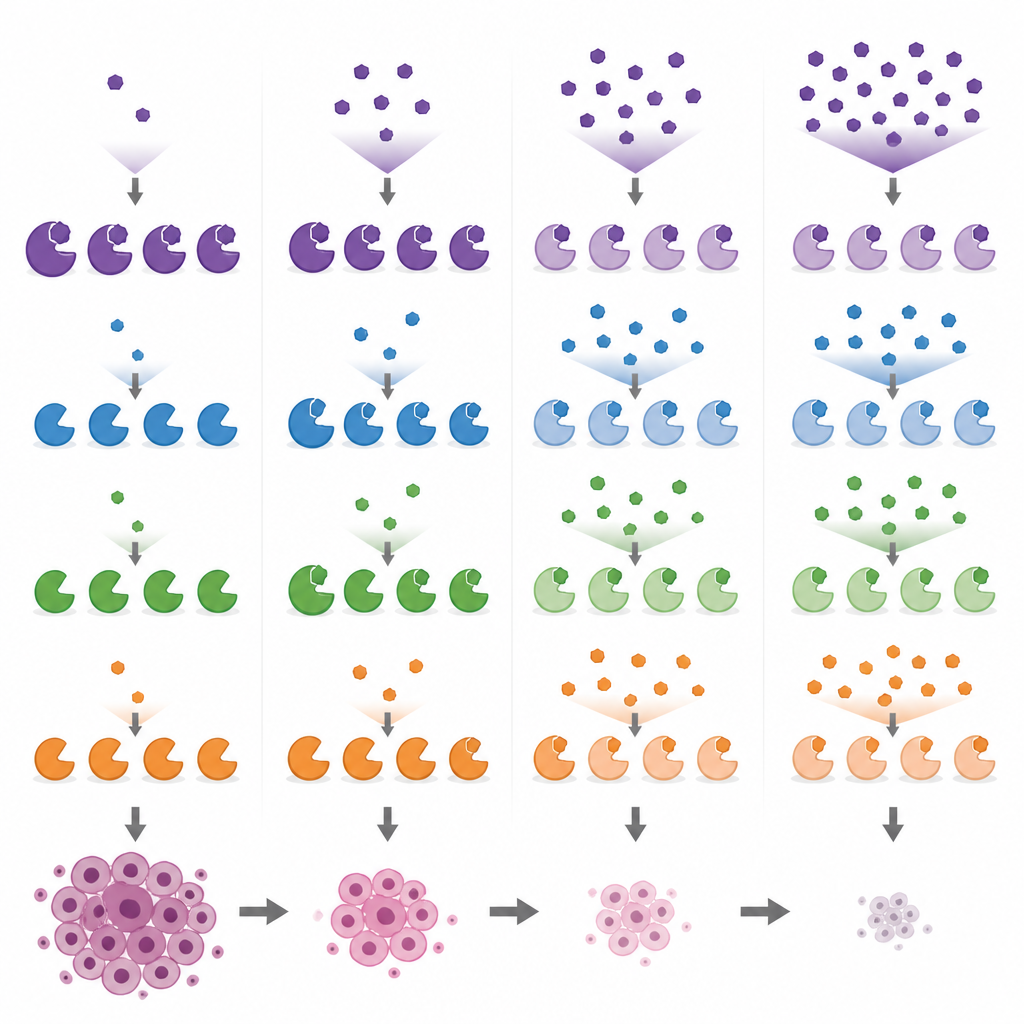
Vergleich populärer Forschungswirkstoffe und ihrer Nebenwirkungen
Ausgestattet mit diesen Biomarker-Auslesungen verglichen die Forscher mehrere in der Forschung häufig verwendete MYST-targetierende Verbindungen in Brustkrebszellen über ein Dosisfeld hinweg. Sie zeigten, dass PF-9363 und sein klinischer Verwandter PF-8144 beide dem gleichen schrittweisen Muster folgen und bei höheren Dosen schließlich auch KAT8 beeinflussen. Im Gegensatz dazu erwies sich WM-1119 als hochselektiv für KAT6A/B selbst bei hohen Konzentrationen, während WM-8014 und WM-3835 zunächst KAT6A/B hemmen und erst danach KAT7. Eine Verbindung, MOZ-IN-3, die in In-vitro-Tests potent erscheint, zeigte in Zellen kaum Wirkung, wahrscheinlich weil sie schlecht in die Zellen gelangt. Diese Vergleiche machen deutlich, dass einige als spezifisch für ein Enzym vermarktete Werkzeuge tatsächlich mehrere treffen, was die Interpretation früherer und zukünftiger Experimente verkomplizieren kann.
Verknüpfung von Dosis, Enzymbindung und Krebszellwachstum
Das Team fragte dann, ob dieses gestufte Hemmungsmuster die Reaktion von Krebszellen beeinflusst. Ein Screening von PF-9363 über das NCI-60-Panel von Krebszelllinien zeigte, dass kurze Expositionen bei Dosen, die nur KAT6A/B und KAT7 blockieren, nur moderate Wachstumswirkungen haben. Starke, schnelle Wachstumsverlangsamungen traten typischerweise erst bei höheren Dosen auf, bei denen auch KAT8 — ein für die meisten Zellen essentielles Enzym — gehemmt war. In einer triple-negativen Brustkrebszelllinie, die besonders von KAT8 abhängig ist, stimmte die Dosis, die die Zellzahl verringerte, mit der Dosis überein, die die KAT8-gekoppelte Histonmarke vollständig unterdrückte und zugleich KAT6A/B und KAT7 blockierte. Das legt nahe, dass bei einigen Tumoren höhere Dosen dieser Wirkstoffe über eine breitere MYST-Hemmung wirken könnten und nicht nur über KAT6A/B allein.
Was das für zukünftige Krebsmedikamente bedeutet
Insgesamt zeigt die Studie, dass kleinmolekulare Hemmstoffe der MYST-Enzyme sich ähnlich verhalten wie viele Kinasehemmer: Bei niedrigen Dosen treffen sie vorwiegend ihre bevorzugten Ziele, doch mit steigender Dosis breiten sie sich auf eng verwandte Enzyme in einer vorhersehbaren Reihenfolge aus. Indem sie einfache, histonbasierte Auslesungen für jedes MYST-Mitglied bereitstellt und aufzeigt, wo gängige Verbindungen tatsächlich selektiv sind, bietet die Arbeit Forschern und Klinikern ein Werkzeugset, um Dosis an die gewünschte Enzymabdeckung anzupassen. Das sollte helfen, Laborstudien klarer zu gestalten, klinische Studienergebnisse besser zu interpretieren und letztlich die Entwicklung präziserer Therapien zu lenken, die die Gensteuerung in Krebszellen umgestalten und gleichzeitig unerwünschte Nebenwirkungen begrenzen.
Zitation: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Schlüsselwörter: epigenetische Enzyme, Histonacetylierung, Targeting von Krebsmedikamenten, Chemoproteomik, Lysin-Acetyltransferase-Inhibitoren