Clear Sky Science · pt
Inibição hierárquica por pequenas moléculas das acetiltransferases MYST
Por que pequenos interruptores no DNA importam para o tratamento do câncer
Dentro de cada célula, interruptores químicos no nosso DNA ajudam a decidir quais genes são ativados ou silenciados. Um grupo de enzimas chamadas acetiltransferases MYST ajusta finamente esses interruptores e tem sido associado a cânceres como câncer de mama e leucemia. Este estudo explora como novas moléculas de fármaco podem regular essas enzimas de forma controlada e em etapas, oferecendo pistas para projetar tratamentos contra o câncer mais precisos e para interpretar ensaios clínicos em andamento.
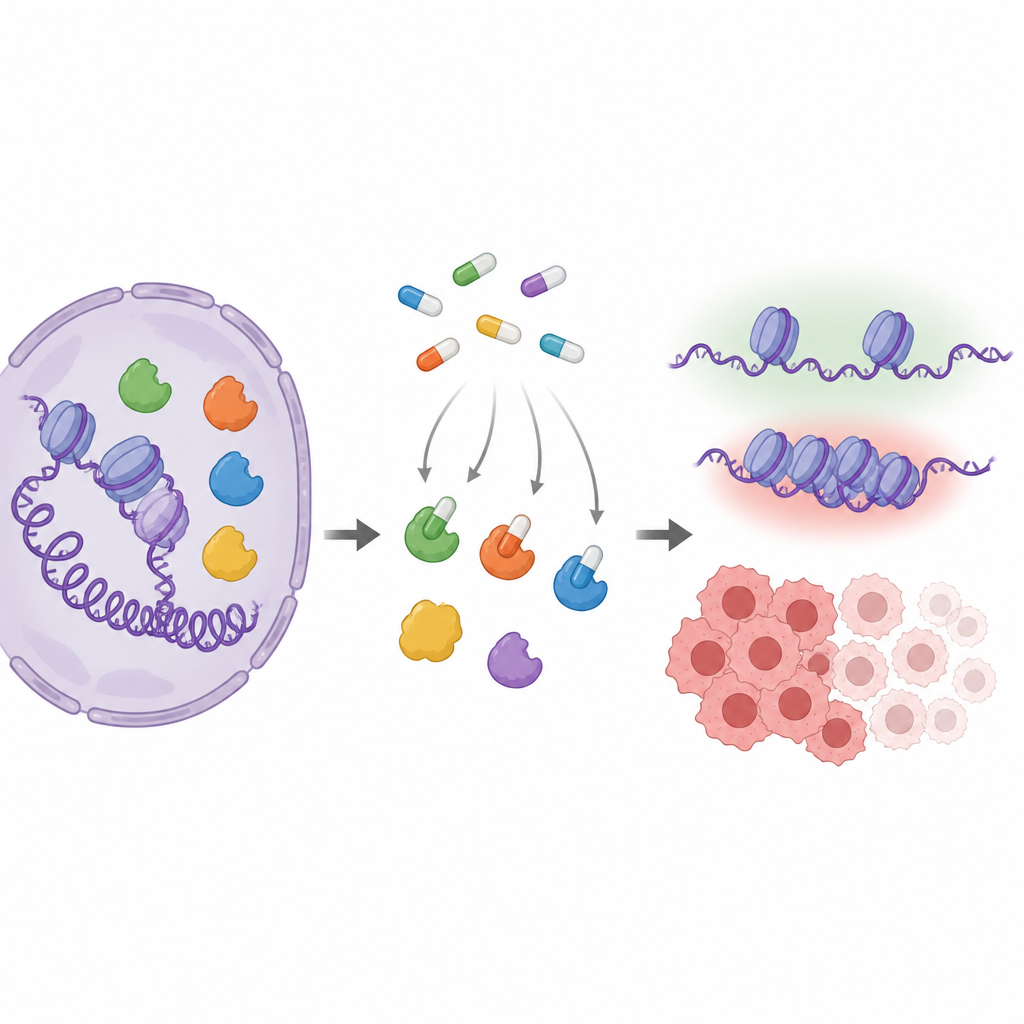
Principais atores que modulam a atividade gênica
As enzimas MYST alteram sutilmente como o DNA é empacotado adicionando pequenas marcas químicas a proteínas chamadas histonas. Esse empacotamento ajuda a decidir se genes envolvidos em crescimento, reparo ou resposta hormonal estão ativos. Vários membros dessa família, especialmente KAT6A e KAT6B, apresentam alterações ou superexpressão em cânceres, o que os torna alvos atrativos para fármacos. Empresas farmacêuticas desenvolveram compostos com forma de comprimido que se encaixam no sítio ativo dessas enzimas, mas como as diferentes MYSTs se parecem muito nesse sítio, é difícil saber exatamente quais enzimas cada fármaco atinge dentro de células reais.
Medindo quais enzimas cada fármaco realmente atinge
Os autores construíram uma estratégia de testes em camadas para mapear como um fármaco líder, PF-9363, e compostos relacionados interagem com as enzimas MYST. Primeiro, usaram uma molécula “isca” ligada a bolinhas magnéticas que captura as enzimas usando o mesmo bolso onde elas usam seu combustível natural. Se um fármaco bloqueia esse bolso, a enzima deixa de aderir à isca. Ao adicionar doses crescentes do fármaco a extratos nucleares de células e então medir, por espectrometria de massa, quais proteínas ainda se ligavam à isca, encontraram uma hierarquia clara: PF-9363 desloca primeiro KAT6A e KAT6B, depois KAT7, depois KAT8, e somente nos níveis mais altos KAT5. O mesmo padrão aparece para o fármaco clínico PF-8144, atualmente em ensaios para câncer de mama receptor de estrógeno positivo.
Encontrando parceiros ocultos e sinais celulares claros
Porque bloquear o bolso da enzima também enfraquece a associação de conjuntos proteicos inteiros que se prendem à isca, a equipe pôde ver quais outras proteínas viajam com cada enzima MYST. Ao agrupar proteínas que deixaram a isca com o mesmo padrão de dose de membros conhecidos do complexo, e então combinar isso com predição de estruturas 3D e experimentos celulares, identificaram o fator de transcrição FOXK2 como um parceiro previamente não reconhecido, especialmente ligado ao complexo NSL que contém KAT8. Em seguida, eles avançaram para células cancerosas vivas e examinaram centenas de marcas químicas em histonas enquanto aumentavam a dose de PF-9363. Identificaram um pequeno conjunto de marcas de acetilação que reportam de forma confiável qual enzima MYST foi bloqueada: uma marca na histona H3 (H3K23Ac) para KAT6A/B, outra em H3 (H3K14Ac) para KAT7, uma em H4 (H4K16Ac) para KAT8, e marcas na histona variante H2A.Z para KAT5. Essas marcas podem ser medidas tanto por espectrometria de massa avançada quanto por blotagens padrão com anticorpos, tornando-as práticas para muitos laboratórios.
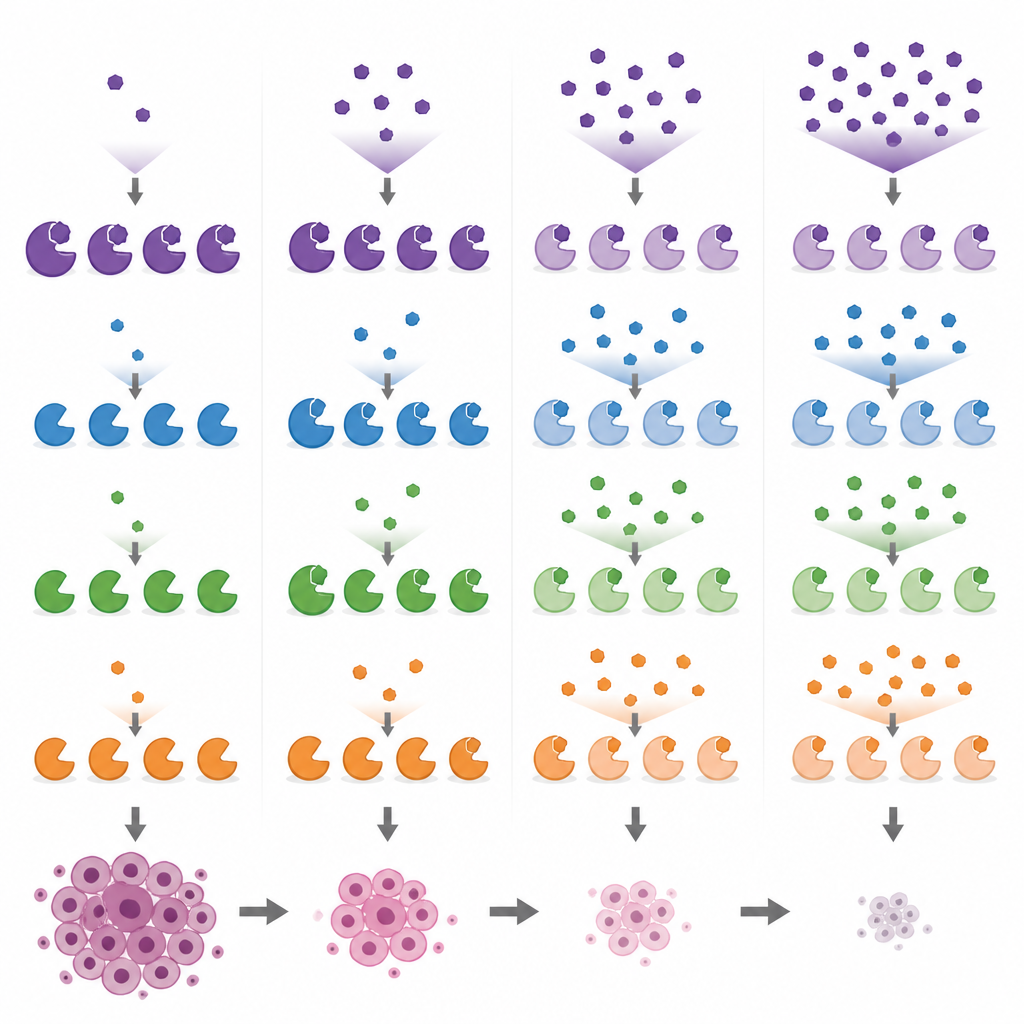
Comparando fármacos populares de pesquisa e seus alvos secundários
Munidos desses sinais biomarcadores, os pesquisadores compararam vários compostos amplamente usados que miram MYST em células de câncer de mama em uma faixa de doses. Demonstraram que PF-9363 e seu par clínico PF-8144 seguem ambos o mesmo padrão escalonado, eventualmente afetando KAT8 em doses mais altas. Em contraste, WM-1119 mostrou ser altamente seletivo para KAT6A/B mesmo em concentrações elevadas, enquanto WM-8014 e WM-3835 inibem primeiro KAT6A/B e somente depois KAT7. Um composto, MOZ-IN-3, que parece potente em ensaios de tubo de ensaio, mostrou pouco efeito em células, provavelmente porque não as penetra bem. Essas comparações revelam que algumas ferramentas comercializadas como específicas para uma enzima na verdade atingem várias, o que pode complicar a interpretação de experimentos passados e futuros.
Relacionando dose, engajamento enzimático e crescimento de células cancerosas
A equipe então perguntou se esse padrão de inibição em camadas molda a resposta das células cancerosas. Triagem de PF-9363 no painel NCI-60 de linhagens de células cancerosas mostrou que exposições curtas a doses que bloqueiam apenas KAT6A/B e KAT7 têm efeitos modestos sobre o crescimento. Lentidões fortes e rápidas no crescimento tipicamente surgiam apenas em doses mais altas onde KAT8, uma enzima essencial para a maioria das células, também estava comprometida. Em uma linhagem de câncer de mama triple-negative que depende especialmente de KAT8, a dose que reduziu o número de células coincidiu com a dose que suprimiu totalmente a marca histônica ligada a KAT8 enquanto também bloqueava KAT6A/B e KAT7. Isso sugere que, para alguns tumores, doses mais altas desses fármacos podem agir por meio de uma inibição mais ampla das MYST em vez de apenas KAT6A/B.
O que isso significa para futuros fármacos contra o câncer
No geral, o estudo mostra que bloqueadores por pequenas moléculas das enzimas MYST comportam-se de modo semelhante a muitos fármacos tirosina-quinase: em baixas doses eles atingem principalmente seus alvos preferidos, mas à medida que a dose sobe se estendem para enzimas intimamente relacionadas em uma ordem previsível. Ao fornecer leituras simples baseadas em histonas para cada membro das MYST e revelar onde compostos populares são verdadeiramente seletivos, o trabalho oferece a pesquisadores e clínicos um conjunto de ferramentas para casar a dose com a cobertura enzimática desejada. Isso deve ajudar a desenhar estudos de laboratório mais claros, interpretar resultados de ensaios clínicos e, em última instância, guiar o desenvolvimento de terapias mais precisas que reconfigurem o controle gênico em células cancerosas enquanto limitam efeitos colaterais indesejados.
Citação: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Palavras-chave: enzimas epigenéticas, acetilação de histonas, direcionamento de fármacos contra o câncer, quimoproteômica, inibidores de acetiltransferases de lisina