Clear Sky Science · fr
Inhibition hiérarchique par petites molécules des acétyltransférases MYST
Pourquoi de petits interrupteurs sur l’ADN comptent pour le traitement du cancer
À l’intérieur de chaque cellule, de petits interrupteurs chimiques sur notre ADN aident à décider quels gènes s’activent ou s’éteignent. Un groupe d’enzymes appelé acétyltransférases MYST affine ces interrupteurs et a été associé à des cancers tels que le cancer du sein et les leucémies. Cette étude examine comment de nouvelles molécules médicamenteuses peuvent moduler ces enzymes de façon contrôlée et progressive, offrant des pistes pour concevoir des traitements anticancéreux plus précis et pour interpréter les essais cliniques en cours.
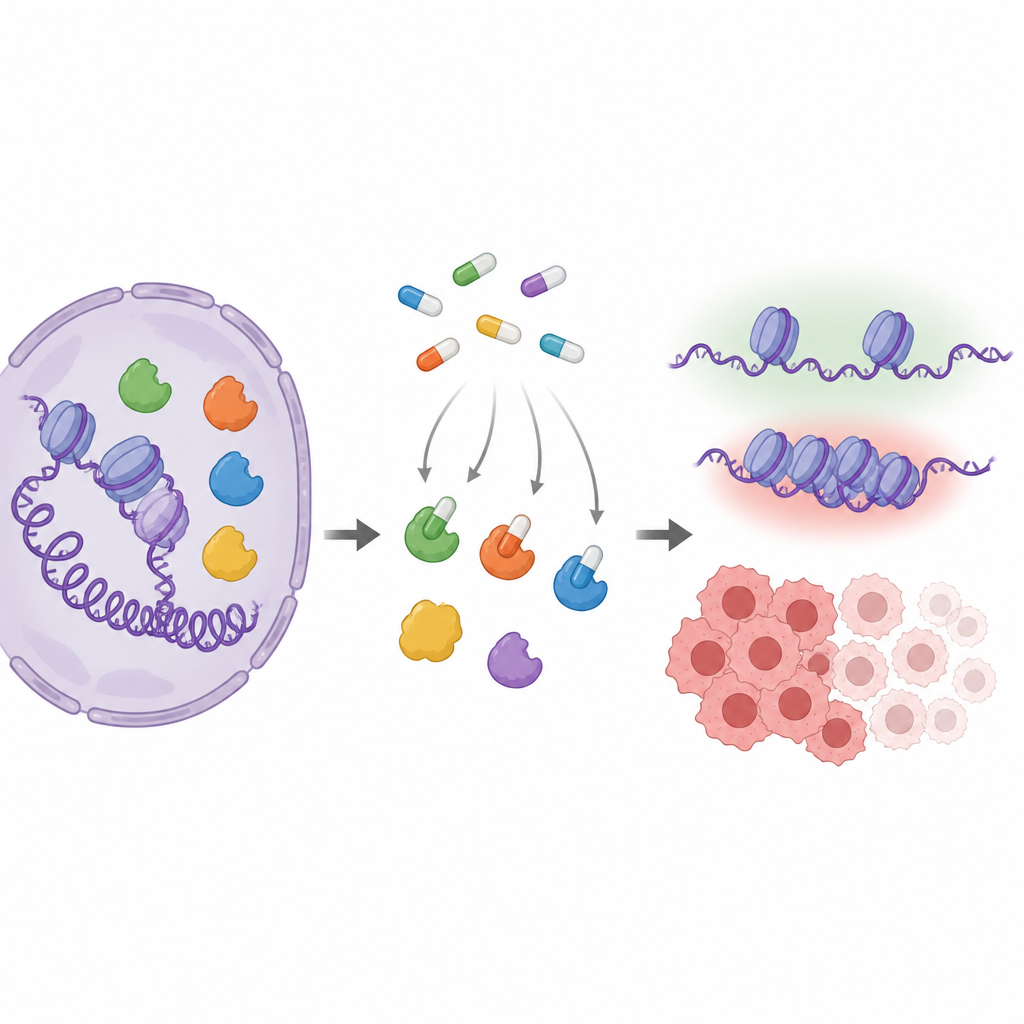
Acteurs clés qui règlent l’activité des gènes
Les enzymes MYST modifient subtilement l’emballage de l’ADN en ajoutant de petites marques chimiques aux protéines appelées histones. Cet emballage influe sur l’activité de gènes impliqués dans la croissance, la réparation ou la réponse hormonale. Plusieurs membres de cette famille, en particulier KAT6A et KAT6B, sont altérés ou surproduits dans les cancers, ce qui en fait des cibles médicamenteuses attractives. Les laboratoires pharmaceutiques ont développé des composés semblables à des pilules qui s’insèrent dans le site actif de ces enzymes, mais comme les différents MYST se ressemblent beaucoup à cet endroit, il est difficile de savoir exactement lesquels chaque médicament atteint dans les cellules réelles.
Mesurer quelles enzymes chaque médicament atteint réellement
Les auteurs ont mis au point une stratégie de test en couches pour cartographier comment un médicament phare, PF-9363, et des composés apparentés interagissent avec les enzymes MYST. D’abord, ils ont utilisé une molécule « appât » fixée sur des billes magnétiques qui capture les enzymes via le même creux où elles utilisent leur carburant naturel. Si un médicament bloque ce creux, l’enzyme n’adhère plus à l’appât. En ajoutant des doses croissantes de médicament à des extraits nucléaires puis en mesurant par spectrométrie de masse les protéines qui restaient liées à l’appât, ils ont trouvé une hiérarchie claire : PF-9363 déloge d’abord KAT6A et KAT6B, puis KAT7, ensuite KAT8, et seulement aux niveaux les plus élevés KAT5. Le même schéma apparaît pour le médicament clinique PF-8144, actuellement en essai pour le cancer du sein positif aux récepteurs œstrogènes.
Identifier des partenaires cachés et des mesures cellulaires claires
Parce que le blocage du creux enzymatique affaiblit aussi la tenue des assemblies protéiques entières qui se fixent à l’appât, l’équipe a pu voir quelles autres protéines voyagent avec chaque enzyme MYST. En regroupant les protéines qui disparaissaient de l’appât selon le même profil de dose que les membres de complexes connus, puis en combinant ces données avec la prédiction de structures 3D et des expériences cellulaires, ils ont signalé le facteur de transcription FOXK2 comme partenaire jusqu’alors non reconnu, particulièrement lié au complexe NSL contenant KAT8. Ensuite, en travaillant dans des cellules cancéreuses vivantes et en examinant des centaines de marques chimiques sur les histones au fur et à mesure de l’augmentation de la dose de PF-9363, ils ont identifié un petit ensemble de marques d’acétylation qui indiquent de façon fiable quelle enzyme MYST a été bloquée : une marque sur l’histone H3 (H3K23Ac) pour KAT6A/B, une autre sur H3 (H3K14Ac) pour KAT7, une sur H4 (H4K16Ac) pour KAT8, et des marques sur l’histone variante H2A.Z pour KAT5. Ces marques peuvent être mesurées soit par spectrométrie de masse avancée, soit par des immunoblotings standards, ce qui les rend pratiques pour de nombreux laboratoires.
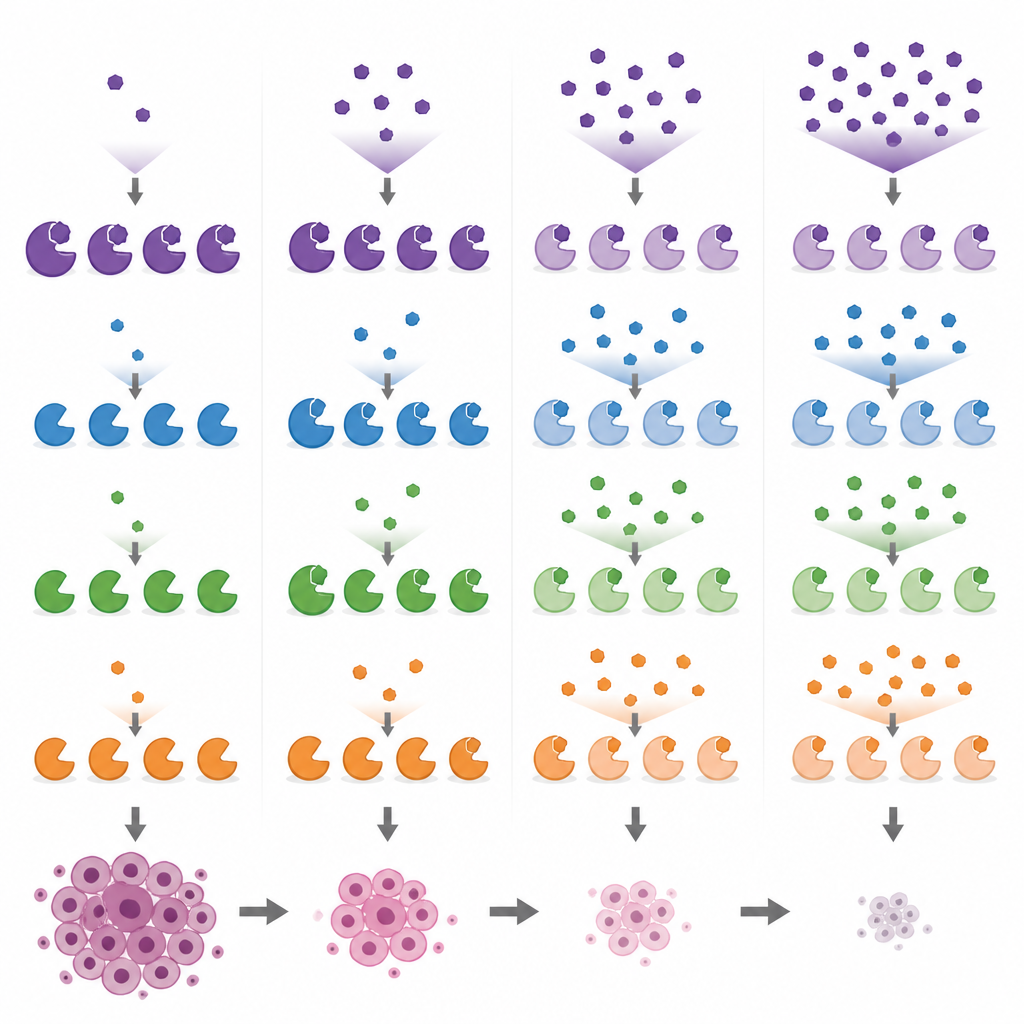
Comparer des médicaments de recherche populaires et leurs cibles secondaires
Armés de ces lectures de biomarqueurs, les chercheurs ont comparé plusieurs composés largement utilisés ciblant les MYST dans des cellules de cancer du sein à travers une gamme de doses. Ils ont montré que PF-9363 et son cousin clinique PF-8144 suivent tous deux le même schéma progressif, affectant finalement KAT8 à des doses plus élevées. En revanche, WM-1119 s’est révélé fortement sélectif pour KAT6A/B même à concentrations élevées, tandis que WM-8014 et WM-3835 inhibent d’abord KAT6A/B puis seulement ensuite KAT7. Un composé, MOZ-IN-3, qui paraît puissant dans des essais in vitro a montré peu d’effet dans les cellules, probablement parce qu’il y pénètre mal. Ces comparaisons révèlent que certains outils commercialisés comme spécifiques d’une enzyme frappent en réalité plusieurs cibles, ce qui peut compliquer l’interprétation d’expériences passées et futures.
Lier dose, engagement enzymatique et croissance des cellules cancéreuses
L’équipe a ensuite cherché à savoir si ce schéma d’inhibition en couches façonne la réponse des cellules cancéreuses. Le criblage de PF-9363 sur le panel NCI-60 de lignées cancéreuses a montré que des expositions courtes à des doses bloquant uniquement KAT6A/B et KAT7 ont des effets modestes sur la croissance. Des ralentissements marqués et rapides de la croissance apparaissaient généralement seulement à des doses plus élevées où KAT8, une enzyme essentielle pour la plupart des cellules, était également engagée. Dans une lignée de cancer du sein triple négatif particulièrement dépendante de KAT8, la dose qui a réduit le nombre de cellules correspondait à la dose qui supprimait complètement la marque d’histone liée à KAT8 tout en bloquant aussi KAT6A/B et KAT7. Cela suggère que, pour certains tumeurs, des doses plus élevées de ces médicaments peuvent agir via une inhibition plus étendue des MYST plutôt que par KAT6A/B seuls.
Ce que cela signifie pour les futurs médicaments anticancéreux
Globalement, l’étude montre que les bloqueurs de petites molécules des enzymes MYST se comportent de manière semblable à de nombreux inhibiteurs de kinases : à faibles doses ils touchent principalement leurs cibles préférentielles, mais à mesure que la dose augmente, ils s’étendent à des enzymes étroitement apparentées dans un ordre prévisible. En fournissant des lectures simples basées sur les histones pour chaque membre des MYST et en révélant où les composés populaires sont réellement sélectifs, ce travail offre aux chercheurs et cliniciens une boîte à outils pour accorder la dose à la couverture enzymatique souhaitée. Cela devrait aider à concevoir des études de laboratoire plus claires, à interpréter les résultats d’essais cliniques et, en fin de compte, à orienter le développement de thérapies plus précises qui remodèlent le contrôle des gènes dans les cellules cancéreuses tout en limitant les effets secondaires indésirables.
Citation: Chen, X., Castroverde, A., Perez, M. et al. Hierarchical small molecule inhibition of MYST acetyltransferases. Nat Commun 17, 4329 (2026). https://doi.org/10.1038/s41467-026-70574-1
Mots-clés: enzymes épigénétiques, acétylation des histones, ciblage médicamenteux du cancer, chimio-protéomique, inhibiteurs des acétyltransférases de lysine